Vorhofflimmern
Definition
Unkoordinierte Vorhofserregung mit einer Vorhoffrequenz von 300–600/min. Das Oberflächen-EKG zeigt eine absolute Arrhythmie und keine eindeutigen P-Wellen mit Andauern > 30 Sekunden. P-Wellen bzw. eine scheinbar organisierte Vorhofsaktivität kann bei fibrotisch veränderten Vorhöfen oder unter antiarrhythmischer Therapie (Amiodaron) erkennbar sein. Diese weisen dann eine andere Morphologie als z.B. bei typischem Vorhofflattern auf.
Epidemiologie
Die Prävalenz von Vorhofflimmern (VHF) liegt bei 1–2% der Gesamtbevölkerung und ist wesentlich altersabhängig (0.5% bei 40- bis 50-Jährigen, 5–15% bei über 80-Jährigen).
Ursachen
- Akut (meist reversibel): Hyperthyreose, Alkohol, Drogen (Kokain), akute Lungenembolie, Katecholamin getriggert (nach Operationen, bei Infekten), Myokardinfarkt
- Chronisch (häufig irreversibel): langjährige arterielle Hypertonie oder Diabetes, Klappenvitien
- Genetisch
Klassifizierung
- Erstdiagnostiziert: Erstmanifestation eines VHF
- Paroxysmal: selbstlimitierend oder Kardioversion < 7 Tage
- Persistierend: anhaltend > 7 Tage
- Lang anhaltend persistierend: anhaltend > 1 Jahr
- Permanent: keine eigentliche zeitliche Einteilung, sondern entspricht Behandlungsstrategie: VHF wird akzeptiert, keine (weiteren) Versuche einer Rhythmuskontrolle
- Valvulär: mittelschwere oder schwere Mitralklappenstenose (siehe Seite), mechanische Klappenprothese (siehe Seite)
- Therapie mit Vitamin K-Antagonist; DOAK kontraindiziert
Symptom Klassifikation
- EHRA 1: keine Symptome
- EHRA 2a: milde Symptome (Alltagsaktivität nicht beeinträchtigt)
- EHRA 2b: moderate Symptome (Alltagsaktivität nicht beeinträchtigt, jedoch Betroffene durch Symptome gestört)
- EHRA 3: schwere Symptome (Alltagsaktivität beeinträchtigt)
- EHRA 4: schwerste Symptome (Alltagsaktivität verunmöglicht)
Grundlegende Abklärungen
- Dokumentation Vorhofflimmern mit Ruhe-EKG
- Klinische Untersuchung: kardial kompensiert? Hämodynamisch stabil?
- Labor: Blutbild, Gerinnung, Leber-/Nierenfunktion, Elektrolyte, TSH
- TTE: strukturelle Herzerkrankung, Kontraindikation DOAK (Mitralstenose)? Volumen linker Vorhof?
- Evtl. Holter-EKG: Frequenzkontrolle? Pausen/Bradykardien?
- Begleitfaktoren: Aktivität, Alkoholkonsum, Adipositas, Einstellung arterielle Hypertonie, OSAS, Diabetes mellitus
Die wichtigsten Fragen
- Klassifikation: Paroxysmal oder persistierend? Beschwerden?
- Therapiestrategie: Frequenz- oder Rhythmuskontrolle?
- Andauern des VHF? Wenn sicher (möglichst dokumentiert) < 24h: Elektrische oder medikamentöse Kardioversion nach umgehendem Beginn einer Antikoagulation ohne weitere Abklärung möglich. > 24h oder unbekannt: Vor Kardioversion TEE/CT (intrakardiale Thromben?) oder therapeutische Antikoagulation über 3 Wochen zwingend.
- Thromboembolieprophylaxe indiziert? Siehe «Indikation zur oralen Antikoagulation» Seite
Vorgehen bei Vorhofflimmern auf Notfallstation
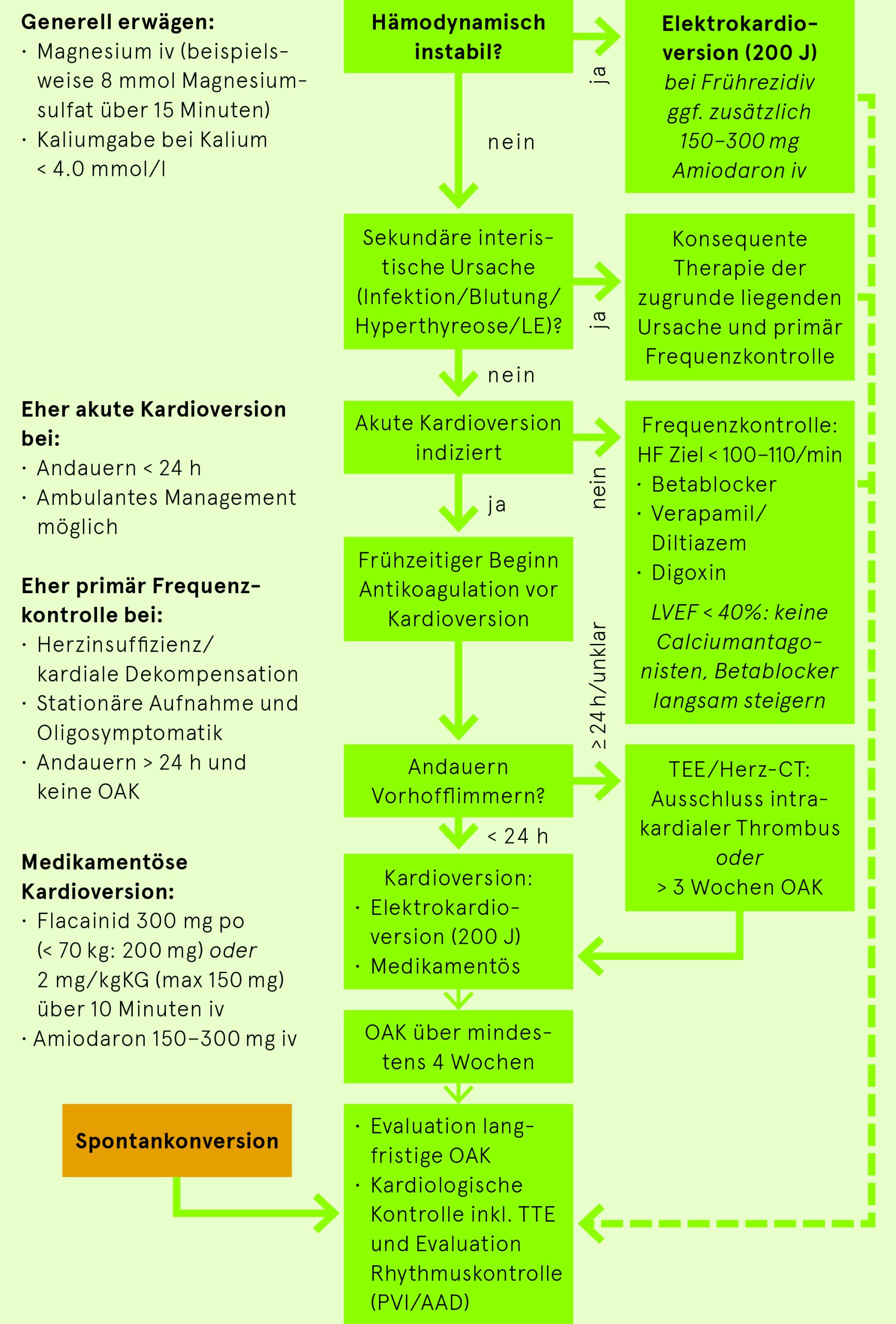
Frequenz- oder Rhythmuskontrolle
Alle grossen klinischen Studien zeigen bisher keinen klaren Überlebensvorteil einer Rhythmuskontrolle gegenüber einer Frequenzkontrolle, was durch aktuelle Studien aber zunehmend infrage gestellt wird. Es scheint jedoch, dass die frühe Rhythmisierung bei neu aufgetretenem Vorhofflimmern in Bezug auf die weitere kardiovaskuläre Morbidität Vorteile bringt. Zudem sind jüngere, symptomatische Patientinnen und Patienten in allen Studien unterrepräsentiert. Eine Rhythmuskontrolle ist im jüngeren Alter oder bei störender Symptomatik und bei neu aufgetretenem Vorhofflimmern sinnvoll (bei paroxysmalem Verlauf in erster Linie mittels Pulmonalvenenisolation). Bei diffusem Beschwerdebild/Unklarheit, ob Vorhofflimmern für die Symptome verantwortlich ist → «Vorhofflimmern-Ferien» siehe nächster Abschnitt.
Klinische Probleme
- Symptomkorrelation: Bei paroxysmalem VHF werden häufig Palpitationen bemerkt. Bei persistierendem VHF eher unspezifische Symptome (Leistungsintoleranz, Müdigkeit). Patientinnen und Patienten mit persistierendem VHF haben jedoch auch häufiger extrakardiale (Hypertonie, OSAS) und kardiale Erkrankungen (KHK, hypertensive Herzkrankheit usw.), sodass die klinische Relevanz von insbesondere normokardem VHF unklar ist. In dieser Situation empfehlen sich «Vorhofflimmer-Ferien»: Elektrokonversion, ggf. vorgängig Amiodaron-Therapie (Reduktion Rezidivwahrscheinlichkeit) und Reevaluation der Symptome im Sinusrhythmus (evtl. Ergometrie vor/nach EKV)
- Tachykardes VHF: kann zu einer linksventrikulären Dysfunktion führen
- Tachykardes VHF mit hypertensiven BD-Werten: im Alter schlecht toleriert; oft Ursache einer akuten Herzinsuffizienz (auch ohne relevante strukt. Herzerkrankung; diastolische Dysfunktion!)
- Bradykardes VHF: oft von Schwindel und Synkopen begleitet; Cave: Sonderform des Sick-Sinus-Syndroms: «Brady-Tachy-Syndrom» bei medikamentöser Therapie des vermeintlich nur tachykarden VHF (Betablocker-Augentropfen wirken auch systemisch!)
- Postoperativ erstmalig aufgetretenes VHF: Nach Herzchirurgie ist die Wertigkeit einer langfristigen Thromboembolieprophylaxe und/oder antiarrhythmischen Therapie unklar. Bei VHF nach nicht-herzchirurgischer Operation und bei als «sekundär» beurteiltem Vorhofflimmern (Fieber, Infekt, akuter Myokardinfarkt, etc.) richtet sich die Indikation zur Thromboembolieprophylaxe aber einzig nach dem CHA2DS2-VA Score und sollte nicht generell vorenthalten werden.
- Asymptomatisches VHF: relativ häufig von TIA und ischämischem Hirnschlag begleitet. Cave: nach Pulmonalvenenisolation (PVI) möglich (auch bei vormals symptomatischem Vorhofflimmern) → Thromboembolieprophylaxe nach PVI in Abhängigkeit des CHA2DS2-VA Scores weiterführen
Indikation zur oralen Antikoagulation (OAK)
Nach einer Kardioversion ist eine Thromboembolieprophylaxe mit vorzugsweise DOAK oder sekundär VKA immer für 4 Wochen (eingeschränkte Vorhofskontraktion: «Stunning») und nach einer Pulmonalvenenisolation (Endothelläsionen im linken Vorhof) für 3 Monate indiziert. Die Indikation für eine langfristige Thromboembolieprophylaxe mit vorzugsweise DOAK oder sekundär VKA richtet sich nach dem CHA2DS2-VA Score. Bei hypertropher Kardiomyopathie oder Amyloidose ist eine Thromboembolieprophylaxe unabhängig vom CHA2DS2-VA Score indiziert.
CHA2DS2-VA Score (max. 8 Punkte, Alter gibt 0, 1 oder 2 Punkte)
| Risikofaktor | Score |
| Herzinsuffizienz/LV-Dysfunktion
Art. Hypertonie Alter ≥ 75 Jahre Diabetes mellitus Stroke/TIA/andere Thromboembolie Gefässerkrankung (KHK, PAVK) Alter 65–74 Jahre |
1
1 2 1 2 1 1 |
| Maximaler Score | 8 |
Indikation zur oralen Antikoagulation gemäss CHA2DS2-VA Score

Direkte orale Antikoagulantien (DOAK)
Effizienz/Sicherheit, Indikation
- Mindestens gleich gute Effizienz im Vergleich zu Vitamin K-Antagonisten (VKA) d.h. Phenprocoumon (Marcoumar) bzw. Acenocoumarol (Sintrom)
- Verbesserte Sicherheit: weniger Hirnblutungen, weniger schwere und lebensbedrohliche Blutungen (im Vergleich mit VKA)
- Gleichwertige Indikation (Klasse I) zur Thromboembolieprophylaxe bei Vorhofflimmern wie VKA; grundsätzlich wird den DOAKs unter Beachtung der Kontraindikationen (schwere Niereninsuffienz, mechanische Herzklappe, mittel- oder hochgradige Mitralklappenstenose) der Vorzug gegeben
Zu beachten gilt
- Compliance kann die Wirksamkeit von DOAKs erheblich beeinträchtigen (kurze Halbwertszeit, kein Monitoring); aber Compliance auch bei Vitamin K-Antagonisten (VKA) nicht optimal
- Kombination mit Thrombozytenaggregationshemmern bei Patientinnen und Patienten mit Vorhofflimmern nach ACS und/oder Stenting: Siehe Kapitel «ACS», Grafik Seite
- Risiko für gastrointestinale Blutungen etwas erhöht bei Rivaroxaban 20 mg und Dabigatran 150 mg 2x/Tag
- Mittelschwere Niereninsuffizienz: regelmässige Kreatininkontrolle nötig (Dabigatran höchste Kumulationsgefahr da 80% renal eleminiert). Die Dosis gemäss Zulassung richtet sich nach der Kreatininclearence und nicht nach der eGFR.
- Schwere Niereninsuffizienz: kaum Daten (weder für DOAK noch für VKA); Apixaban und Edoxaban whs. die besten Optionen
- Quantifizierung des antikoagulatorischen Effektes (Anti-Faktor-Xa Aktivität) im Notfall (Blutung, Operation) möglich, aber nicht generell zur Therapiekontrolle
- Nach bariatrischer Chirurgie wenig Daten hinsichtlich Resorption von DOAK. Primär Verwendung von VKA oder von Apixaban unter Kontrolle der Anti-Faktor-Xa Aktivität
- Therapieoption im Falle einer Blutung siehe «Hämostasiologische Massnahmen» Seite
- Umstellung VKA auf DOAK: Beginn DOAK sobald INR ≤ 2
Blutungsrisiko: HAS-BLED Score (untersucht für Blutungsrisiko unter Warfarin)
HAS-BLED Score ≥ 3 = Blutungsrisiko erhöht. Patientinnen und Patienten sollten, wenn indiziert, dennoch antikoaguliert werden. Im Vordergrund steht eine optimale Kontrolle der modifizierbaren Blutungsrisikofaktoren (unkontrollierte arterielle Hypertonie, unter VKA optimales INR Monitoring oder Wechsel auf DOAK, Verzicht auf NSAR, Reduktion Alkoholkonsum).
Wenn die Antikoagulation wegen Blutungen nicht fortgeführt werden kann, steht für die Patientinnen und Patienten heute der kathetertechnische Vorhofsohrverschluss (LAA-Occlusion) zur Reduktion des Blutungsrisikos (langfristig keine Antikoagulation mehr) und Reduktion des Schlaganfallrisikos (Ausschalten des wichtigsten morphologischen Korrelats) zur Verfügung. Dies wird in örtlicher Betäubung im kurzstationären Aufenthalt durchgeführt. Es hat sich bewährt eine periinterventionelle transösophageale Echokardiographie (TEE) zur sicheren Device Platzierung durchzuführen, diese bedarf einer Intubationsnarkose. Zur Evaluation und Abklärung (meist Herz-CT, ggf. TEE) kann eine Zuweisung in die Sprechstunde für strukturelle Herzkrankheiten (SHD) erfolgen.
| Buchstabe | Klinisches Charakteristikum | Punkte |
| H | Art. Hypertonie | 1 |
| A | Abnorme Nieren*- und Leberfunktion** (je ein Punkt) | 1 oder 2 |
| S | Schlaganfall | 1 |
| B | Blutung | 1 |
| L | Labiler INR | 1 |
| E | Alter > 65 Jahre | 1 |
| D | Drogen und/oder Alkohol ( je ein Punkt) | 1 oder 2 |
| Max. 9 Punkte |
Vorgehen bei Indikation für Thrombozytenaggregationshemmung und oraler Antikoagulation
Bei stabiler KHK (keine Angina pectoris, keine akute Ischämie und/oder Stentimplantation < 12 Monate): OAK (DOAK, VKA) Monotherapie (siehe auch Kapitel Chronisches Koronarsyndrom Seite). Nach einem ACS/PTCA gemäss Leitlinien ACS (siehe Grafik Seite).
Medikamente zur Frequenzkontrolle
Betablocker
- po: z.B. Bisoprolol (Concor) 5–10 mg
- iv: z.B. Metoprolol (Beloc) langsam 1-mg-weise iv, Zieldosis 5 mg iv, dann auf po wechseln; in der Akutsituation Bolus 5 mg langsam iv, repetierbar alle 10 Min. bis max. 15 mg, KI: eingeschränkte LVEF
Ca-Antagonisten
(Wenn möglich immer po, da iv negativ inotrop) Cave: schlechte LVEF
- po: Diltiazem (Dilzem) po 3× 60 mg/Tag, später bis 2× 120 mg/Tag
- iv: falls nötig Diltiazem 0.25 mg/kg Bolus iv, evtl. wiederholen, Dauerinfusion 5–15 mg/Std. (Cave: Herzinsuffizienz)
- Isoptin immer po geben, max. Dosis 480 mg/Tag
Digoxin (bei Herzinsuffizienz)
- (0.25-) 0.5 mg Bolus iv, evtl. wiederholen, maximal 1 mg (in 3 Dosen), dann po weiter (Cave: Hypokaliämie, Niereninsuffizienz)
Kardioversion
Elektrische Kardioversion (EKV)
- Schnellste und effektivste Konversion des VHF
- Indiziert bei symptomatischen Patientinnen und Patienten mit Arrhythmiebeginn < 24 Std. oder suffizienter Antikoagulation ≥ 3 Wochen/TEE oder hämodynamischer Instabilität
- EKV (synchronisiert!) in Kurznarkose/Analgosedation mit 200 J (biphasisch)
Medikamentöse Kardioversion
- Primär oder wenn mit EKV kein Erfolg
- Alle unten angeführten Antiarrhythmika können bei nicht erfolgreicher EKV angewendet werden. EKV nach aufdosierter Medikamentengabe wiederholen
| Medikamente (Klasse) | Dosis | Erfolg | Kontraindikationen/Warnhinweise |
| Amiodaron (Cordarone) (III) |
|
ca. 70% |
|
| Flecainid (Tambocor) (Ic) |
|
ca. 80% |
|
Medikamente zur Rhythmuskontrolle
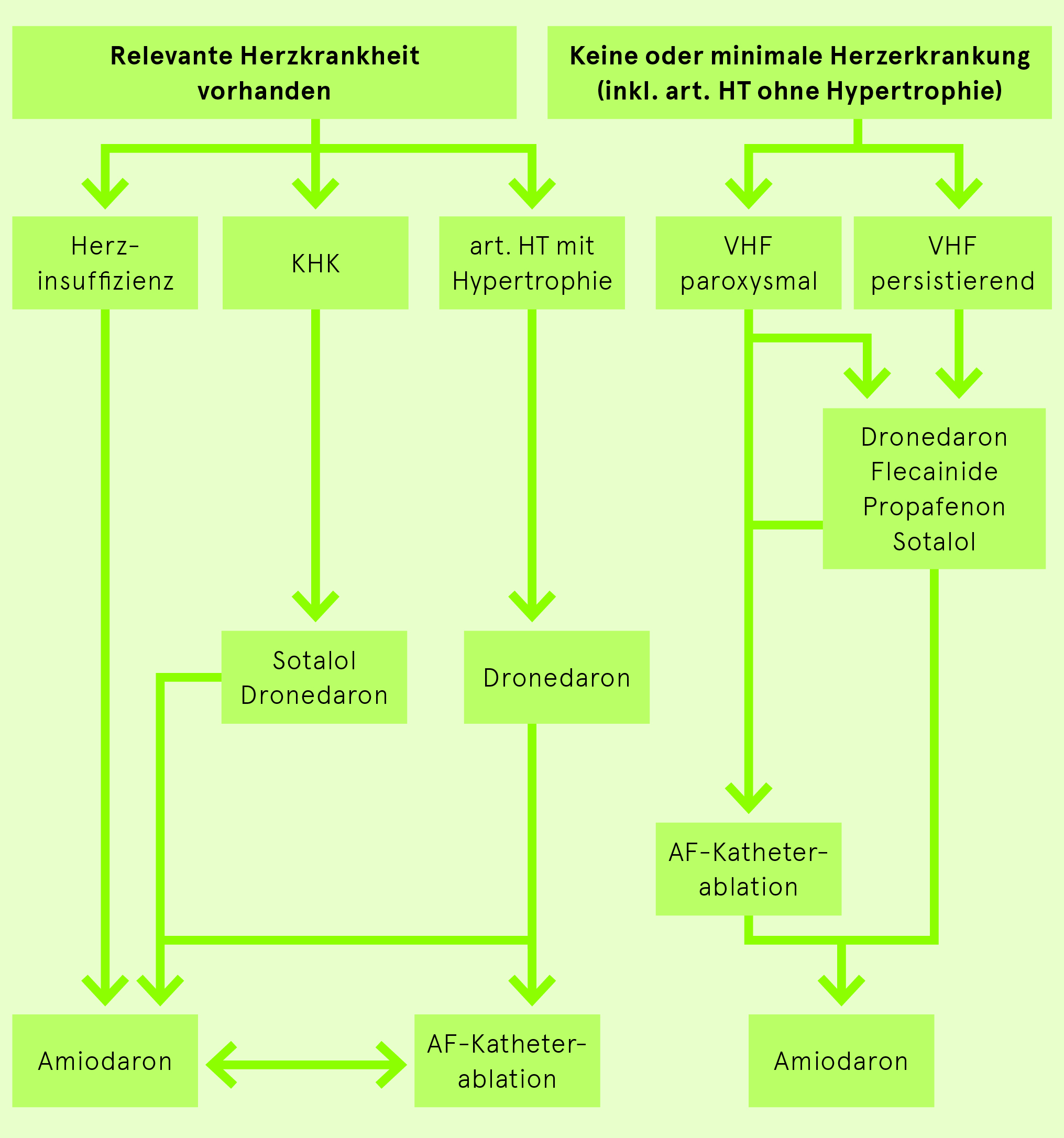
Keine strukturelle Herzerkrankung
- Betablocker
- Antiarrhythmika:
- Flecainid (Tambocor) 2× 50–150 mg po immer mit Betablocker kombinieren (Vorhofflimmern kann durch Flecainid in Vorhofflattern organisieren und 1:1 auf die Ventrikel übergeleitet werden, was hämodynamisch häufig schlecht vertragen wird bzw. Kammerflimmern induzieren kann).
- Dronedarone (Multaq) 2× 400 mg po. Komplexes Interaktionspotential (DOAK, Digoxin, Calciumantagonisten): Interaktionscheck. KI: kürzliche kardiale Dekompensation, NYHA III/IV, CrCl < 30ml/min, QTc>500ms
- Sotalol (Sotalex) 2× 80–160 mg po (Cave: Torsades-de-pointes bei Hypokaliämie und QTc-Verlängerung, Niereninsuffizienz)
Strukturelle Herzerkrankung
- Antiarrhythmika:
- Amiodaron (Cordarone). Regelmässige Kontrolle der Leber- und Schilddrüsenwerte, optimaler UV Schutz
- Sotalol (Sotalex) 2× 80–160 mg po (falls keine Herzinsuffizienz und keine Niereninsuffizienz vorhanden; Cave: erhöhtes Risiko von Torsades-de-pointes bei Hypokaliämie und QTc-Verlängerung)
- Dronedaron (Multaq) 2× 400 mg po. Komplexes Interaktionspotential (DOAK, Digoxin, Calciumantagonisten): Interaktionscheck. KI: kürzliche kardiale Dekompensation, NYHA III/IV, CrCl < 30ml/min, QTc > 500ms
Ablationsbehandlung bei Vorhofflimmern
Pulmonalvenenisolation (PVI)
- Symptomatisches Vorhofflimmern oder Nebenwirkungen der Antiarrhythmika-Therapie, Tachykardie induzierte Kardiomyopathie, gewisse Patientinnen und Patienten mit Herzinsuffizienz
- Grundsätzlich bessere Erfolgsrate bei paroxysmalem VHF (hier Empfehlung für vorderhand PVI gegenüber Antiarrhythmika) und je weniger strukturelle Herzerkrankung vorhanden
- Verschiedene Modalitäten: Radiofrequenzenergie (RFA), Cryoballonablation, Pulsed-field Ablation (PFA) mit unterschiedlichen Komplikationsspektren
- Langzeiterfolg etwa 70–80%; 20–30% der Fälle benötigen aber Zweit- oder Drittinterventionen; Komplikationsrate insgesamt 2–3%: Leistenkomplikationen (Hämatom, AV-Fistel, Pseudoaneurysma) 1–2%, Perikardtamponade 1-2%, Rest < 1%: TIA/Insult, Oesophagoatriale Fistel[1], Pulmonalvenenstenose[2]< 0.5%.
AV-Knoten-Ablation nach vorgängiger Schrittmacherimplantation
- Nach Implantation eines Schrittmachers wird der AV-Knoten abladiert. Geeignet für ältere Patientinnen und Patienten mit Nebenwirkungen der Antiarrhythmika-Therapie oder mit Tachykardie-Bradykardie-Syndrom (frequenzsenkende Medikamente sollen tachykarde Episoden verhindern, führen aber zu Bradykardien und AV-Überleitungsstörungen)
- Vorteil: Effektive Frequenzkontrolle; Antiarrhythmika können abgesetzt werden
- Nachteil: Schrittmacherabhängigkeit, dyssynchrones Pacing im RV, deshalb bei EF < 40% vor Knoten-Ablation CRT-Implantation nötig
Erhaltung des Sinusrhythmus bei VHF
Management von Risikofaktoren und Komorbiditäten
Ein breites Feld von Komorbiditäten ist mit Vorhofflimmernrezidiven und der Progression von paroxysmalem in ein persistierendes Vorhofflimmern assoziiert. Deshalb steht für eine erfolgreiche Vorhofflimmernbehandlung immer auch ein optimales Risikofaktorenmanagement im Vordergrund.
- Optimale Therapie einer arteriellen Hypertonie
- Optimale Herzinsuffizienztherapie
- Diabetes mellitus
- Adipositas
- Therapie obstruktives Schlafapnoesyndrom
- Körperliche Aktivität
- Reduktion Alkoholkonsum auf < 4 Standardgetränke pro Woche
Quellen/Links
- Hindricks G et al. 2020 ESC Guidelines for the diagnosis and management of atrial fibrillation. EHJ. 2021 Feb 1;42(5):373-498.
- Stiell I et al. CAEP Acute Atrial Fibrillation/Flutter Best Practices Checklist. CJEM 2018;20(3):334-342.
Dr. Florian Franzeck
Prof. Dr. Peter Ammann
Dr. Dr. Roman Brenner
Dr. Philipp Haager
Dr. Jörg Scheler
- Symptome Tage bis Wochen nach PVI: (bedingt durch Luftembolie, Mediastinitis) Fieber, Sepsis, unklarer Neurologie und Schluckbeschwerden. Hohe Letalität daher rasches Handeln: Computertomografie mit oralem und iv Kontrastmittel, KEINE Gastroskopie (Luftembolie!), Involvierung Rhythmologie, Chirurgie und Infektiologie:. Nüchtern lassen, hochdosiert PPI, antibiotische Breitbandtherapie. ↵
- Symptome oft Monate nach PVI: Leistungsintoleranz/Dyspnoe, Husten, Hämoptysen, pulmonale Infekte. ↵