Kardio-Onkologie
Definition
Krebspatienten haben ein erhöhtes Risiko für kardiovaskuläre Morbidität und Mortalität durch: Therapie-assoziierte Nebenwirkungen, gemeinsame Risikofaktoren (Nikotin, arterielle Hypertonie, Alter) und die unmittelbare Interaktion des kardiovaskulärem Systems mit dem hämatologischen und/oder somatischen Tumorleiden. Die Kardio-Onkologie widmet sich als Spezialgebiet dieser besonderen Patientenpopulation.
Empfehlungen europäisch, national
Im August 2022 ist die erste ESC Leitlinie Kardio-Onkologie veröffentlicht worden. Auch Schweiz-weit ist eine erste nationale Empfehlung hierzu erschienen, letztere als praktisches Booklet zum Nachschlagen in pdf-Format (siehe auch Links am Kapitelende).
Ziel
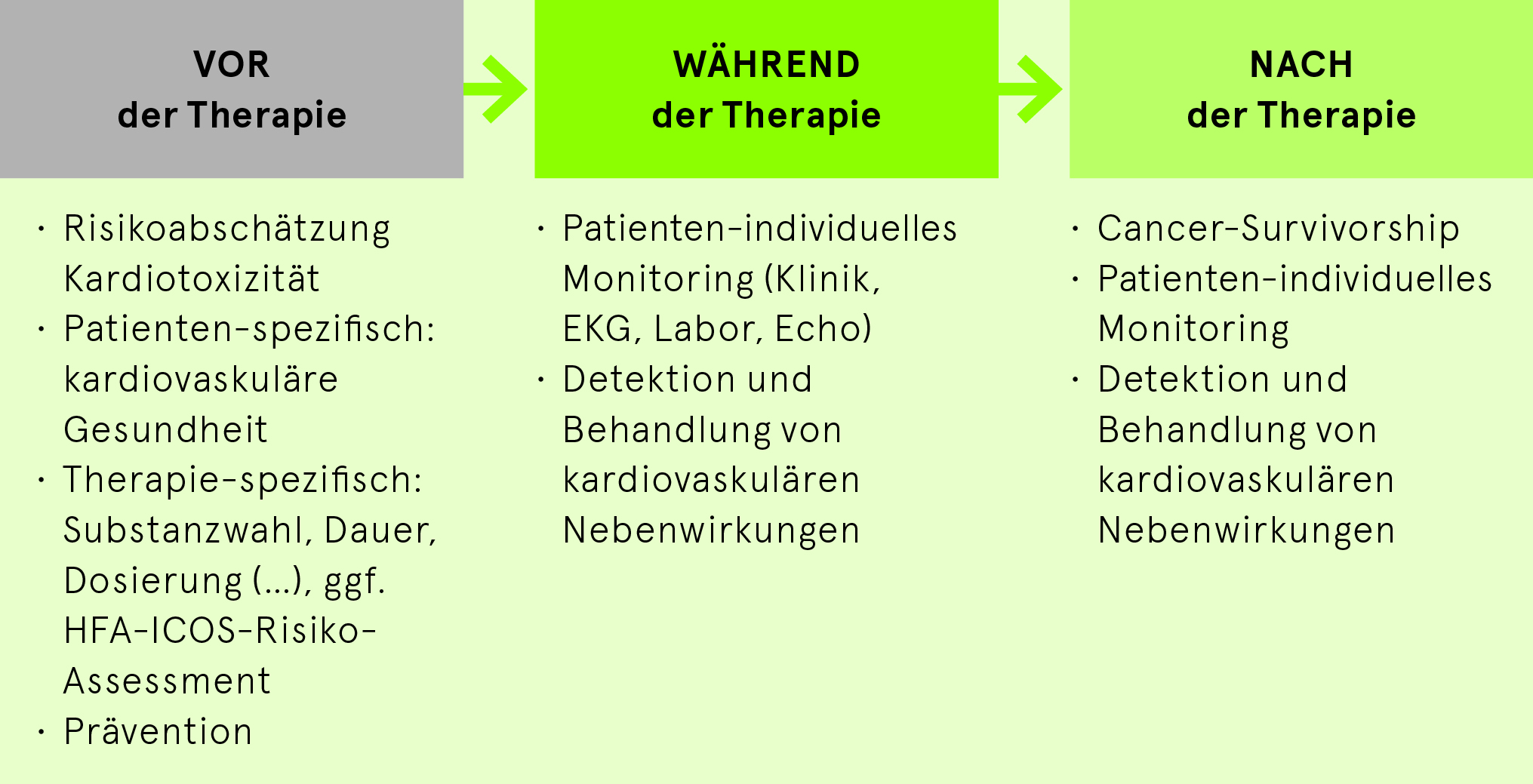
Zentrales Anliegen der Kardio-Onkologie ist es, die betroffenen, onkologischen Patienten während ihres gesamten onkologischen Behandlungspfades (vor, während und auch nach der Therapie) anhand einer sinnvollen Risikoabschätzung über ein Monitoring (Klinik, EKG, Echo, kardiale Biomarker) mit Prävention und Therapiemassnahmen optimal zu begleiten und zu überwachen; also vorausschauend und begleitend und nicht erst, wenn schon irreversible Schäden aufgetreten sind.
Kardiotoxizität spezifischer Tumortherapien
Für mehrere spezifische onkologische Therapien und Substanzen (siehe Tab. 1) liefern die genannten Literaturstellen konkrete Empfehlungen in der Betreuung von onkologischen Patienten im praktischen Alltag und mit welchen Strategien das Kardiotoxizitätsrisiko minimiert werden kann.
Kardiovaskuläre Nebenwirkungen
Das Spektrum möglicher kardiovaskulärer Nebenwirkungen (NW) ist breit. Eine häufig auftretende und relevante NW ist die Entwicklung einer linksventrikulären Dysfunktion, des weiteren kann es zu thromboembolischen Ereignissen, Herzrhythmusstörungen (u.v.m.) kommen. Bisweilen sind bei den kardio-onkologischen Patienten spezifische Therapiemassnahmen zu berücksichtigen. Kardiovaskuläre NW können früh oder auch erst Jahre nach der onkologischen Therapie auftreten, sie können asymptomatisch oder symptomatisch verlaufen. Ein langfristiges kardiologisches Follow-Up macht bei ausgewählten Patientengruppen Sinn (Cancer-Survivorship).
Quellen/Links
- ESC Leitlinien: https://doi.org/10.1093/eurheartj/ehac244
- Swiss Cardio-Oncology Booklet: https://www.heartfailure.ch/images/richtlinien/KONK-Booklet_Final__Version_1.1_06.2022.pdf
- HFA-ICOS-Risiko-Assessment: Lyon, A.R. et al. Baseline cardiovascular risk assessment in cancer patients scheduled to receive cardiotoxic cancer therapies: a position statement and new risk assessment tools . Eur J Heart Fail, 22: 1945-1960. https://doi.org/10.1002/ejhf.1920
Dr. Eva Scheler
Dr. Martin Fehr