Akutes Aortensyndrom
Grundsätzliches
- Das akute Aortensyndrom umfasst verschiedene, in Beziehung zueinanderstehende Aortenpathologien mit ähnlicher klinischer Präsentation und Therapie: die klassische Aortendissektion, das intramurale Hämatom (IMH), das penetrierende Aortenulkus (PAU) und die akute Aortenruptur (iatrogen oder traumatisch)
- Patho-Mechanismus: Intima-Ruptur mit Bluteintritt in die Media. Sonderform: lokalisiertes IMH bei Ruptur der Vasa vasorum, beim PAU führt eine Plaqueruptur zur Arrosion der Vasa vasorum mit lokalisiertem IMH
- Risikofaktoren: langjährige arterielle Hypertonie, Bindegewebserkrankungen (Marfan, Ehlers-Danlos, Loeys-Dietz), positive Familienanamnese, bikuspide Aortenklappe, Coarctation (Aortenisthmusstenose), entzündliche Gefässerkrankungen, Dezelerationstrauma, schwere Atherosklerose, PAU; selten: Kokain, Amphetamin, Schwangerschaft
- Die Einteilung der Aortendissektion erfolgt bezüglich Symptomdauer in hyperakut (< 24 h), akut (1 bis ≤ 14 Tage), subakut (14 Tage bis 90 Tage) und chronisch (> 90 Tage). Hinsichtlich der Lokalisation des intimalen Einrisses und der Ausdehnung der Dissektion in der Aorta werden Dissektionen unterschieden nach der Stanford Klassifikation: Aortendissektion Typ A mit Befall der Aorta ascendens, Aortendissektion Typ B ohne Befall der Aorta ascendens.
- Die Aortendissektion ist selten (Inzidenz: ca. 6/100’000 Pers./Jahr)
- Bei der Aortendissektion Typ A kommt es häufig (⅔ der Fälle) und früh zu Komplikationen: Perikardtamponade/ruptur, Myokardischämie (Kompression/Obliteration der Koronargefässe) oder Malperfusion aortaler Äste. Die Letalität ist in den ersten 48 Std. 1% pro Stunde und die 30-Tage-Mortalität nach operativer Behandlung liegt bei ca. 30%.
- Bei der unkomplizierten Aortendissektion Typ B beträgt die Letalität < 10% in den ersten 30 Tagen (unter maximaler intensivmedizinischer Therapie) aber bei komplizierter Form mit renaler Malperfusion, mesenteriale Ischämie, retrograde Dissektion oder gedeckte Ruptur steigt die Letalität bis auf 25%.
- IMH (10–25% der akuten Aortensyndrome): kann propagieren zu einer Aortenruptur oder einer akuten Dissektion. Regression ebenfalls möglich. Therapie analog Dissektion
- PAU (2–7% aller akuten Aortensyndrome): kann propagieren zu einem intramuralen Hämatom, Pseudoaneurysma, einer Aortenruptur oder einer akuten Dissektion. Der natürliche Verlauf ist aber gekennzeichnet durch das Grössenwachstum mit Ausbildung eines sakkulären oder fusiformen Aneurysmas. Therapie analog Dissektion, ggf. aggressiver aufgrund der hohen Rupturrate beim symptomatischen PAU
Akute Aortendissektion: Klinische Befunde
- Leitsymptom (85%): perakut einsetzender, reissender oder stechender, ggf. von proximal nach distal wandernder Thoraxschmerz. Falls Aorta ascendens betroffen, eher Thoraxschmerzen; falls Aorta descendens betroffen, eher Rückenschmerzen
- Hypertonie oder Hypotonie (Pseudohypotonie bei Befall der supraaortalen Äste, A-Dissektion mit Tamponade)
- BD-Differenz zwischen beiden Armen oder zwischen oberer und unterer Extremität
- Renale und/oder viszerale Ischämie
- Zerebrale und/oder spinale Ischämie
- Uni- oder bilaterale Beinischämie
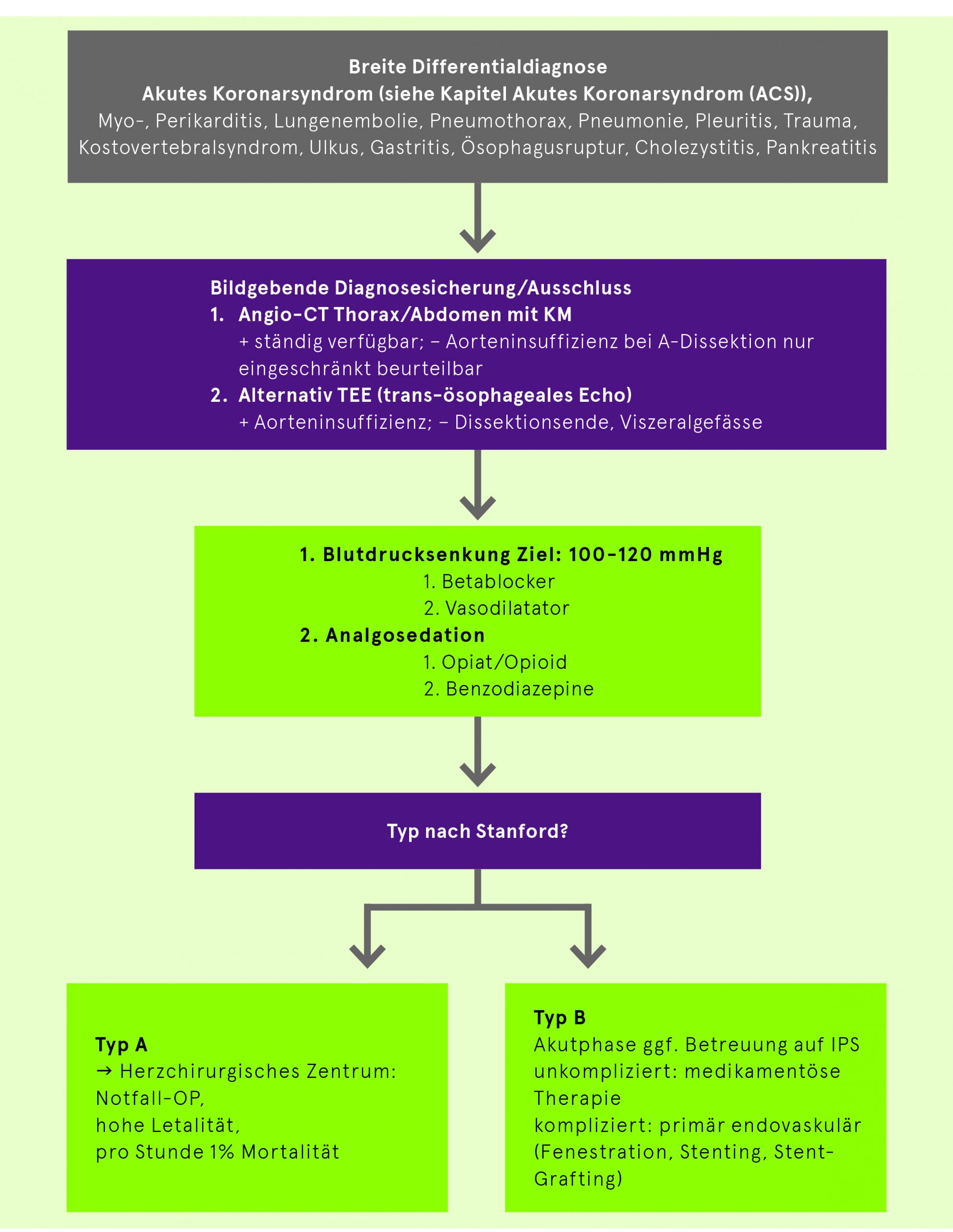
Algorithmus: Akutes Aortensyndrom siehe nachfolgende Grafik
Akutes Aortensyndrom
Akutmassnahme bei akuter Aortendissektion Typ B
- Initiale Therapie siehe Grafik«Akutes Aortensyndrom»
- Alle Patienten mit akuter Aortendissektion müssen in der Akutphase intensivmedizinisch überwacht werden.
- Medikamentöse Behandlung siehe nächster Abschnitt «Behandlung akuter und subakuter Aortendissektionen»)
- Engmaschige Kontrollen in der frühen Phase wegen erhöhtem Instabilitätsrisiko:
- CT-Angiografie bei Eintritt, 3–5 Tage nach Symptombeginn und vor Entlassung; erneute CT-Angiografie auch bei erneutem Schmerzereignis oder Zeichen einer Komplikation
- Klinisch und CT-angiografische Kontrolle nach 4-6 Wochen
- Weitere Kontrollen (immer mit Bildgebung) analog der chronischen Aortendissektion
Behandlungsempfehlungen in der akuten/subakuten Phase einer Aortendissektion Typ B
Unkompliziert
- Medikamentöse Therapie:
- Aggressives Senken des Blutdrucks und der Herzfrequenz (Ziel-Blutdruck systolisch 100 – 120 mmHg; Ziel-Herzfrequenz 60 – 80 bpm; Initialbehandlung mit Betablocker, Ca-Antagonisten, sekundär: ACE Hemmer, AT2-Rezeptorblocker)
- Ausreichende Analgesie
- Falls bildgebende oder klinische Risikofaktoren bestehen, kann auch bei einer unkomplizierten Aortendissektion Typ B nach Stanford eine endovaskuläre Behandlung evaluiert werden:
- Bildmorphologische Risikofaktoren:
- Max. Aortendurchmesser > 40 mm
- Durchmesser des falschen Aortenlumen > 20–22 mm
- «Entry»grösse > 10 mm
- «Entry» an der kleinen Aortenkurvatur gelegen
- Blutiger Pleuraerguss
- Bildgebende Malperfusion-Zeichen (ohne klinisches Korrelat)
- Klinische Risikofaktoren:
- Refraktäre arterielle Hypertonie (Bedarf an > 3 verschiedenen ausdosierten Antihypertensiva)
- Refraktäre Schmerzen > 12 h trotz adäquater Analgesie
- Wiedereintritt aufgrund der Dissektion
- Bildmorphologische Risikofaktoren:
Kompliziert
- Zeichen einer komplizierten Aortendissektion (und damit Instabilität und auch einer drohenden Ruptur):
- Neu aufgetretener hämorrhagischer Pleuraerguss oder periaortales Hämatom
- Aortaler Durchmesser ≥ 55 mm oder Zunahme > 4 mm in den ersten 90 Tagen
- Erneute Symptome (siehe Klinische Befunde) wie persistierende Schmerzen, unkontrollierte arterielle Hypertonie oder Malperfusion
- Bei einer komplizierten Aortendissektion Typ B nach Stanford muss ein invasives Vorgehen in Erwägung gezogen werden, präferentiell im Sinne einer endovaskulären Behandlung (Stentgraft, TEVAR) oder selten mit offenem Aortenersatz (wenn TEVAR kontraindiziert).
Chronische Aortendissektion (>90 Tage)
- Medikamentöse Therapie:
- Nachhaltige Blutdrucksenkung auf systolisch 100 – 120 mmHg (siehe akute Dissektion)
- Kardiovaskuläre Sekundärprophylaxe mit Thrombozytenaggregationshemmer (z.B. Aspirin cardio 100 mg/Tag) und Statin (für letztere bestehen Hinweise auf Reduktion der Grössenprogression von Aneurysmata), insbesondere bei Vorliegen atherosklerotischer Gefässveränderungen
- Regelmässige bildgebende Kontrollen wegen Aortendilatation (Aneurysmabildung) und Re-Dissektionen mittels CT- oder MR-Angiografie:
- Empfohlene Nachsorgeintervalle: 1, 6, 12 Monate nach Initialereignis, danach jährlich (sofern stabile Befunde).
- Wenn die Aorta über 2 Jahre grössenstabil bleibt, können die Kontrollintervalle verlängert werden.
- Evaluation hinsichtlich interventioneller/chirurgischer Therapie:
- Aortaler Durchmesser ≥ 55mm oder Zunahme > 10 mm/Jahr
- Erneute Symptome: Zeichen einer Malperfusion oder rezidivierende Schmerzen
Quellen/Links
- Isselbacher E, Preventzq O, Hamilton J et al. 2022 ACC/AHA Guideline for the Diagnosis and Managment of Aortic Disease. Circulation. 2022;146:00–00. https://doi.org/10.1161/CIR.0000000000001106
- Riambau V, Böckler D, Brunkwall J et al. Editor’s Choice – Management of Descending Thoracic Aorta Diseases. Eur J Vasc Endovasc Surg. 2017;53(1):4-52, https://doi.org/10.1016/j.ejvs.2016.06.005
- Erbel R, Aboyans V, Boileau C et al. ESC Guidelines on the diagnosis and treatment of aortic diseases. Eur Heart J. 2014;35(41): 2873–2926, https://doi.org/10.1093/eurheartj/ehu281
- Fattori R, Cao P, De Rango P et al. Interdisciplinary Expert Consensus Document on Management of Type B Aortic Dissection. J Am Coll Cardiol. 2013; 61(16)1:661-78, https://doi.org/10.1016/j.jacc.2012.11.072
PD Dr. Lukas Hechelhammer
PD Dr. Regula von Allmen
Dr. Alexander Poloczek
Prof. Dr. Hans Rickli