化學實驗(二)
實驗十八 簡易染料敏化太陽能電池製作
一、目的
利用天然染料花青素與二氧化鈦奈米粒子製作簡易的太陽能電池。
二、原理
太陽能電池和一般所說的電池不同,並沒有儲存能量的功能,而是將光能轉變為電能的裝置。目前最為廣泛使用的太陽能電池為矽基太陽能電池,但其他不同類型的太陽能電池亦在快速發展,其中染料敏化太陽能電池(dye-sensitized solar cell, DSSC)是利用有機染料分子吸收光能,透過如二氧化鈦奈米粒子的材料來轉移傳遞電子。染料敏化太陽能電池具有結構和製作方法簡單等優點,但液態電解質和有機染料的穩定度也是其大量生產和應用的挑戰。
本實驗將使用二氧化鈦奈米粒子和蔬果中的天然染料花青素(anthocyanin)製作染料敏化太陽能電池。電池的化學反應和結構如下:
anthocyanin + hν → anthocyanin*
anthocyanin* + TiO2 → e− (TiO2) + anthocyanin+
e− (TiO2) → TiO2 + e− 電池負極
anthocyanin+ + 3/2 I− → anthocyanin + 1/2 I3−
1/2 I3− + e− → 3/2 I− 電池正極
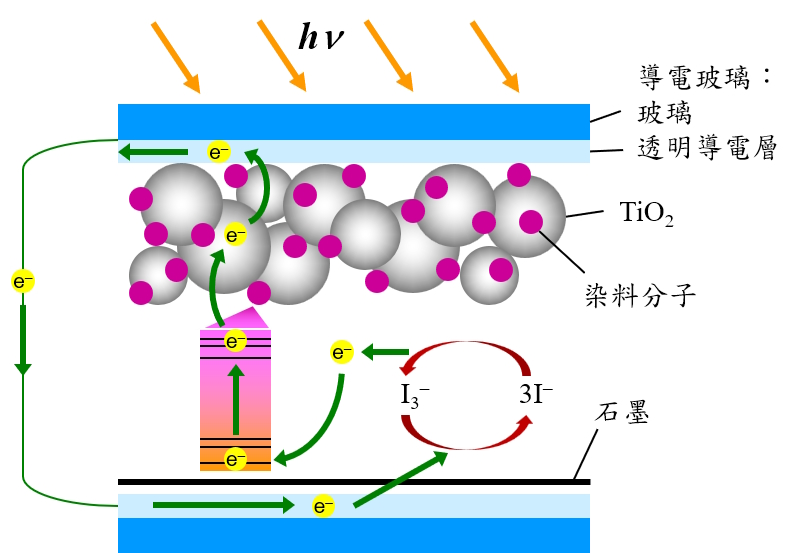
吸附在二氧化鈦奈米粒子上的花青素分子吸收光能被激發而釋放電子至具有半導體性質的二氧化鈦奈米粒子,電子再被傳導至由導電玻璃製作的電池負極,而花青素正離子則被電解質液中的碘離子還原,此過程中所消耗的碘離子,則由電池正極吸收電子而被還原。電池的淨反應為光能轉換為電能,沒有其他反應物的損失。
三、器材及藥品
器材:
燒杯、導電玻璃(兩片)、滴管、玻棒、加熱板、蠟燭、長尾夾、鱷魚夾、三用電表、3M®隱形膠帶
藥品:
二氧化鈦奈米粒子、0.1 mM HNO3、5% Triton X 100 介面活性劑、碘/碘化鉀/乙二醇電解液、紫紅或藍紫色水果果汁、乙醇
四、實驗步驟
二氧化鈦薄膜製備(於抽風櫥中進行,以下二氧化鈦糊配方可供四組實驗使用)
-
取 0.6 g 二氧化鈦奈米粒子置於研缽,緩慢滴入 2.0 mL 的 0.1 mM 硝酸水溶液,滴入過程中不斷攪拌使糊狀物均勻,但勿產生氣泡。
-
滴入 4 滴(約 0.2 ml)5% Triton X 100 介面活性劑,溫和攪拌均勻避免產生氣泡,靜置 15 分鐘。
-
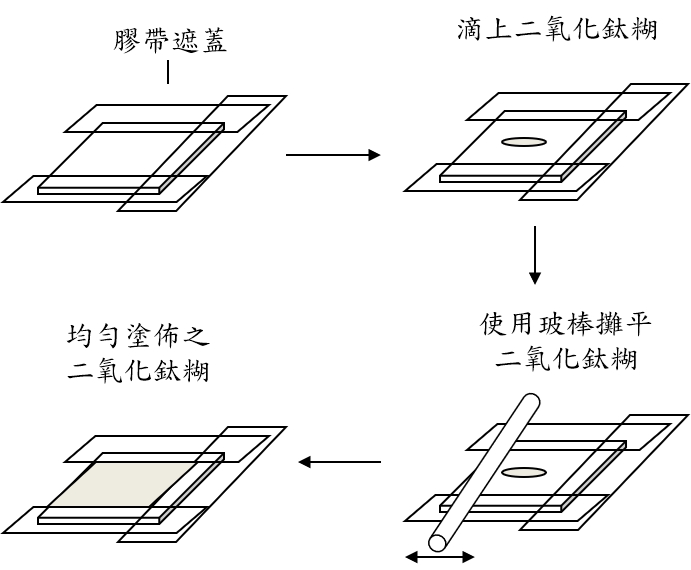
取一片導電玻璃,用乙醇和面紙進行清潔,將導電面(使用三用電錶確認)朝上放置,如圖所示使用膠帶遮蓋導電面三個邊約 5 mm。
-
使用滴管取二氧化鈦糊,滴在上述導電玻璃未遮蓋的導電面上,使用玻棒將二氧化鈦糊攤平,並移除多餘糊狀物,可以得到和膠帶厚度相等的糊狀物薄膜,靜置三分鐘。
-
小心撕去膠帶,將鋪有糊狀物薄膜的導電面朝上置於加熱板上,加熱將糊狀物烤乾後冷卻,可得二氧化鈦薄膜。
二氧化鈦薄膜染色與電池組裝
-
將步驟 5. 之導電玻璃浸入裝盛有果汁的燒杯內,浸泡 10-15 分鐘,使二氧化鈦吸附花青素,染色成為紫色。。
-
取出導電玻璃,使用滴管以少量水和乙醇小心洗去導電玻璃上多餘果汁,用面紙輕輕吸乾。
-
取另一片沒有二氧化鈦薄膜的導電玻璃,將導電面用蠟燭火焰燻黑。
-
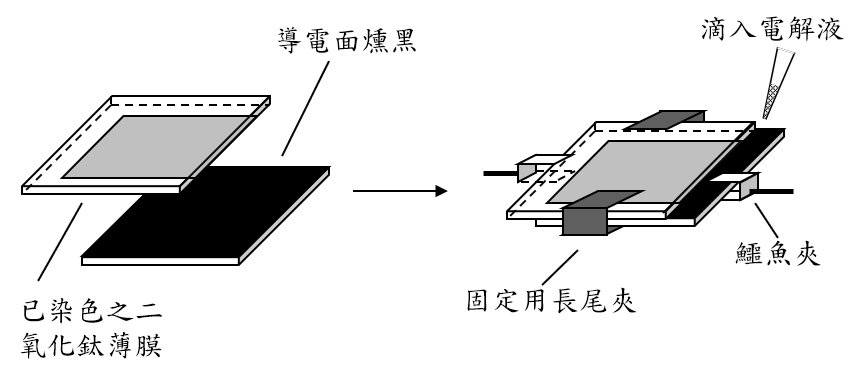
如下圖將分別有已染色二氧化鈦薄膜、已燻黑的兩片導電玻璃疊在一起(讓兩個導電面接觸),保留約 5 mm 不要重疊,供鱷魚夾與電位量測使用。
-
在兩片導電玻璃接觸縫隙間滴上 1 滴碘/碘化鉀/乙二醇電解液。用長尾夾固定兩片導電玻璃,輕輕拭去滲出的多餘電解液。
太陽能電池測試
-
將太陽能電池置於陽光或燈光下,直接使用三用電表測量兩電極間的電位差(最大輸出電壓)。
-
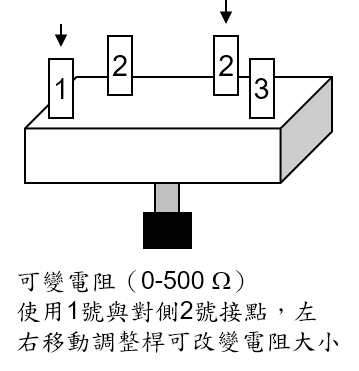
【選擇】如電路圖,使用可變電阻,測試在不同的負載下,電池所能提供的電位差與電流大小,並繪製「電位差/電流」關係圖。(本實驗製作之太陽能電池僅在製作非常良好且天候晴朗時能以一般三用電表測得電流)

導電玻璃回收
-
拆開電池,用乙醇洗去電解質溶液。用沾有乙醇的面紙輕輕拭去導電玻璃上的二氧化鈦薄膜與和炭黑。
五、實驗結果
電池最大輸出電位差: mV
【選擇】電池輸出的電位差與電流關係
| 電位差 | 電流 |
|
|
|
|
|
|
|
|
六、問題與討論
-
試由實驗結果計算所製作太陽能電池最大輸出功率,與每單位面積最大輸出功率?(若電流過小無法量測,本題列式說明即可)
-
實驗所使用的二氧化鈦是平均粒徑為數十奈米的粒子,和更大粒徑的粒子相比有何差異?
-
假設花青素分子吸收了綠色光(波長 530 nm),每吸收 100 個光子能使電池輸出 10 個電子,電位差為 0.2 V,試計算光能轉換為電能的效率。
