BINDEVEVSSYKDOMMER (REV 021-033)
59
Myositt (Dermatomyositt og Polymyositt)
Øyvind Palm and Jan Tore Gran
Kjennetegn på inflammatorisk polymyositt og dermatomyositt
Progredierende svakhet i proksimale muskler (lår, overarmer).
Dermatomyositt (DM) med typiske hud-forandringer.
Vedvarende økt CK i blodet.
Noen med utslag i myosittspesifikke antistoff (myositt-blot).
MR av lårmuskler viser bilateralt muskelødem.
Non-inflammatorisk myopati og inklusjonslegeme myositt utelukkes.
Diagnosen sikres ved biopsi fra affisert muskulatur.
Diagnosekoder ICD-10: M33.1 (Dermatomyositt), M33.2 (Polymyositt). J99.1 Lungemanifestasjon ved bindevevssykdom; G72.0 Legemiddelindusert myositt/myopati; G72.8 Kreft-assosiert (annen) myopati
Prosedyrekoder: 6-minutter gangtest: FYFX05. Intravenøs infusjon: WBGM00. Behandling med rituksimab: L01XC02. Infusjon med gammaglobulin: RPGM05. EKG: FPFE15
ATC koder (for legemiddelstatistikk): L04A A Immunsuppressive legemidler
Nøkkelord ved journalskriving
Diagnosen bygger på
- Debutalder, familiære tilfeller. Bruk av statiner
- Symmetrisk, progressiv, proksimal muskelsvakhet, mest i under-ekstremiteter
- Svake nakkemuskler (tendens til drop-head)
- Hud-affeksjon ved dermatomyositt, antisyntetase syndrom, MDA5-assosiert myositt (heliotropt eksantem, V-tegn over hals/thoraks, sjal-tegn over nakke. Gottrons tegn/papler, mekaniker-hender, ulcera)
- Dysfagi, dysmotilitet i øsofagus
- Lungemanifestasjon (antisyntetase syndrom, MDA5-assosiert myositt)
- Forhøyde muskelenzymer (maksimal CK og siste verdier) i serum: CK. ASAT, LD
- MR med ødem i lårmuskler
- EMG (hvis utført): patologisk som ved myositt
- Muskelbiopsi; Degenerasjon, regenerasjon, nekrose, fagocytose og interstitielle mononukleære infiltrater.
- Endomysial infiltrasjon ved polymyositt.
- Perimysial infiltrasjon ved dermatomyositt.
Hensikten med konsultasjonen
Definisjon
Myositt (idiopatisk inflammatorisk myopati, IIM) er en gruppe inflammatoriske revmatiske sykdommer. De kjennetegnes av inflammasjon og nekrose i tverrstripet muskulatur og har ukjent sykdomsårsak. Typiske symptomer er progredierende svakhet i proksimale muskler som lår, overarmer og nakke, ofte uten særlig smerte. I tillegg er dysfagi, eksantem (dermatomyositt) og andre ekstramuskulære manifestasjoner i lunge, hjerte og ledd vanlig (Lundberg IE, 2017; Dourado E, 2023). I blodprøver forventes kreatin kinase (CK) å være vedvarende forhøyet og mange har også utslag i antinukleære antistoff (ANA) med spesifikke subgrupper. Sykdommene deles vanligvis inn i fem grupper utenom overlapp-syndromer (Glaubitz S, 2020).
- Polymyositt (PM)
- Dermatomyositt (DM) (muskel- og hud-affeksjon) og juvenil dermatomyositt (JDM).
- Immunmediert nekrotiserende myopati (IMNM), inklusiv statin-indusert myopati deles inn i tre grupper: a) anti-HMGCA positiv type (statin-relatert hos ca. 50%), b) anti- SRP positiv type, c) antistoff negativ type.
- Antisyntetase syndrom (ASS) (med lungemanifestasjon)
- Inklusjonslegememyositt (IBM) (middelaldrende og eldre personer)
I tillegg kommer kreft-assosiert myositt (CAM), overlapp-syndromer (skleromyositt) og noen sjeldne undergrupper (andre, se sist i kapitlet).
Myositt/IIM skilles fra non-inflammatoriske myopatier på bakgrunn av ulik anamnese, sykdomsutvikling, histologi (inflammasjon-non-inflammasjon), forekomst/fravær av antistoffer og fravær/forekomst av nevrologiske manifestasjoner (Barohn RJ, 2014).
Historie
1863 og 1887: Polymyositt og dermatomyositt beskrives av Ernst Leberecht Wagener (Keitel W , 2015).
1916: Dermatomyositt assosieres med malignitet (Tiniakou E, 2015)
1975: Klassifikasjon av subtyper av Peter & Bohan (Leclair V, 2018)
1990: Syv myosittspesifikke antistoff beskrives (Mi2, SRP, Jo-1, PL-7, PL-12, EJ, OJ)
2017: EULAR/ACR kriterier (Leclair V, 2018)
Sykdomsårsaker
Etiologien til myositt-sykdommer vanligvis ukjent. De klassifiseres da som “idiopatiske” (uten kjent årsak). Man vet mer om disponerende faktorer (genetikk) og sykdomsutviklingen (patogenesen) med involvering immunologiske og miljømessige faktorer (Musaj J, 2024).
Autoimmunitet er sentralt i patogenesen. Kroppens eget immunsystem angriper og skader friskt muskelvev ved en feil. Dette involverer aktivering av ulike immunceller som T-lymfocytter, B-lymfocytter og makrofager som igjen medfører produksjon av autoantistoffer som er spesifikke for eller assosiert med undergrupper av myositt.
Statiner. IMNM kan i noen tilfeller trigges av statiner. Ofte foreligger også en genetisk disposisjon, men en klar familiær disposisjon er uvanlig (Dourado E, 2023).
Kreft. Ved visse former for myositt, spesielt dermatomyositt (DM), kan utløses i forbindelse med en underliggende kreftsykdom. Dette tyder på at malignitet kan frigjøre antigener som utløser en autoimmun reaksjon rettet mot muskler og hud (Oldroyd AGS, 2021).
Epidemiologi
Inflammatorisk myositt er en sjelden gruppe systemsykdommer med varierende epidemiologisk presentasjon.
Prevalensen av myositt estimeres til å være 6-10 tilfeller per 100 000 innbyggere, mens insidensen ligger på 0,5 til 8 nye tilfeller per million innbyggere per år. Det tilsvarer ca. 25 nye tilfeller i Norge årlig. Sykdommen rammer hyppigst individer i aldersgruppen 40-50 år og er noe vanligere blant kvinner (kvinne/mann-forhold på omtrent 2:1) (Dobloug C, 2015). Det er en trend til at andelen av diagnosen “polymyositt” er synkende. Dette skyldes bl. a. fremskritt innen immunserologi, slik at stadig flere tilfeller som tidligere ble klassifisert som polymyositt, nå kan klassifiseres til mer spesifikke subgrupper basert på nyere myositt-spesifikke autoantistoffer (Betteridge Z, 2016; Preger C, 2022).
| Myositt-subgruppe | Prevalens | Insidens (årlig) | Referanse: Hossain M, 2022; Schmidt J, 2018; Dobloug C, 2015 |
| Myositt (alle) | 14-21/100 000 | 11/million | |
| Polymyositt | 1-10/100 000 | 0,75/100 000 | |
| Dermatomyositt | 1-13/100 000 | 1-15/million | |
| IMNM | 0,1/100 000 | 0,1-1,5/million | |
| ASS | 1-9/100 000 | 0,56/100 000 | |
| IBM | 5-14/million voksne | – |
Symptomer og kliniske kjennetegn
Inflammatorisk myositt kan presentere seg med en rekke symptomer, noe som kan forsinke diagnostisering. I gjennomsnitt tar det 2,25 år fra symptomdebut til korrekt diagnose stilles (Namsrai T, 2022). Tidlige sykdomstegn som kan vekke mistanke om myositt inkluderer:
- Proksimal muskelsvakhet (reise seg fra huk, fra stol, gå opp trapper, løfte armene)
- Eksantem (dermatomyositt)
- Belastningsdyspne eller tørr-hoste (antisyntetase syndrom)
- Forhøyet kreatin kinase (CK) av uklar årsak hos eldre personer (spesielt ved inklusjonslegememyositt).
En grundig anamnese og målrettet utredning er avgjørende for tidlig diagnostikk.
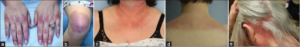
Dermatomyositt. 1) V-tegn på thoraks 2) Mekanikerhender 3) Gottrons papler over MCP, PIP og DIP-ledd 4) Sjal-tegn over nakke og skuldre. Illustrasjon: Mervi U, Indian J Derm, 2012. CC-BY-NC-SA 3.0
Generelle symptomer
Pasienter får ofte påvirket allmenntilstand med sykdomsfølelse, lett feber og vekttap. Artralgier er også vanlige, spesielt i tidlig sykdomsfase.
Muskler
Et kardinalsymptom ved myositt er progredierende muskelsvakhet. Denne utvikler seg vanligvis langsomt, over uker til måneder, og aldri akutt over dager. Nevrologiske symptomer som parestesier, tremor, fascikulasjoner og muskelspasmer er ikke typisk (Lilleker JB, 2017).
Proksimal symmetrisk kraftsvekkelse affiserer oftest lårmuskler, hofter, nakke skuldre. Dette merkes med vanskeligheter i dagligdagse aktiviteter som å reise seg fra en stol, gå i trapper, eller løfte armene over hodet. Inklusjonslegememyositt (eldre pasienter) affiserer imidlertid ofte også distale muskelgrupper.
Gangfunksjon: Svakhet i hoftemuskulaturen påvirker gangfunksjonen og debuterer nesten alltid før affeksjon av skulderbuen.
Smerte og stivhet er vanligvis beskjedne sammenlignet med graden av muskelsvakhet.
Nakke-ekstensorer: Kraftig affeksjon av nakkens strekkemuskler kan føre til “drop-head” (hodet faller fremover). Dette kan kreve differensialdiagnostisk avklaring mot tilstander nevrologiske sykdommer og amyloidose.
Svelgmuskulatur (faryngeale og øsofageale muskler): Muskler i svelget kan rammes hos omtrent 39% av pasientene (Lilleker JB, 2017). Det kan føre til betydelig dysfagi, nasal tale, heshet og nasal regurgitasjon, samt risiko for aspirasjon. Dette skyldes affeksjon av den tverrstripede muskulaturen i farynks og øvre øsofagus.
Ubehandlet forløp: Ubehandlet fører ofte myositt til progredierende muskelatrofi og betydelig fysisk funksjonstap.
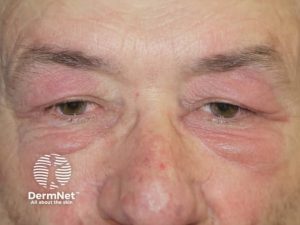
Dermatomyositt. Når myositt er ledsaget av hudforandringer, klassifiseres tilstanden som dermatomyositt (DM), alternativt antisyntetasesyndrom eller (sjelden) anti-MDA5 antistoff-myositt (hud-affeksjon og alvorlig lungemanifestasjoner). Hudsymptomene ved myositt kan være kløende, lysømfintlig og kan korrelere med myosittaktiviteten, men kan også debutere måneder før muskel-affeksjonen.
Selv om DM-utslett i ansikt eller hodebunn kan minne om kutan lupus, kan de differensieres ved hjelp av øvrige kliniske tegn og spesifikke autoantistoffer (Didona D, 2023).
Karakteristiske hudforandringer ved dermatomyositt inkluderer:
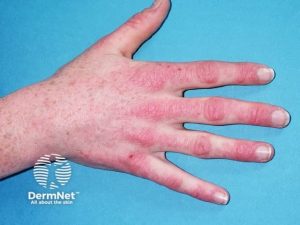
Gottrons tegn: Erythematøse – lilla forandringer på dorsalsiden av hendene, særlig over metakarpofalangeal- (MCP) og proksimale interfalangealledd (PIP), men kan også sees over albuer og knær. Dette er en veldig vanlig manifestasjon ved dermatomyositt.
Gottrons papler: Papulært (små knuter), erythematøst utslett, oftest over MCP-ledd, men kan strekke seg over dorsalsiden av hele fingrene (Ricceri F, 2015).
V-tegn er et erythematøst, lyssensitivt utslett som danner en V-form på hals og fremre bryst.
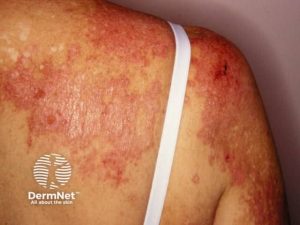
Sjal-tegn (Shawl sign): Erythematøst utslett på skuldre og øvre del av ryggen. Ca. 45% med DM angripes.
Hylster-tegn (Holster-sign): Rød-lilla, retikulært (nettformet) utslett lateralt på knær og lår, tilsvarende et område hvor et våpen-hylster ville sitte (Cooper S, 2015).
Poikiloderma: Består av en kombinasjon av telangiektasier, hudatrofi og hypo- eller hyperpigmentering. Dette ses ofte sammen med V-tegn, sjal-tegn og hylster-tegn.
Mekaniker-hender (maskinist-hånd): Flassende hud med sprekkdannelser på fingertuppene, spesielt på radialsiden av pekefingre og tomler. Symptomet sees hyppigst ved antisyntetase syndrom, men kan forekomme ved dermatomyositt.
Sjeldne hudmanifestasjoner
Subkutant ødem kan være assosiert med alvorlig sykdom. Det er vanligst ved juvenil dermatomyositt (JDM) og kan utvikle seg før muskelmanifestasjonene. Disse symptomene kan minne om kapillar lekkasje syndrom (capillary leak syndrome) og nyresvikt (proteinuri).
Nekrotiserende ulcera (vaskulitt sår) signaliserer alvorlig sykdom og kan være assosiert med anti-MDA5-positivitet (MDA5 syndromet; vennligst se nedenfor) og med koeksisterende lungesykdom og malignitet.
Neglesengsforandringer. Hos 30-60 % av pasientene ses hypertrofi av kutikula (mellom neglen og huden) og små hemoragiske infarkter i neglesengene. Kapillaroskopi vil ofte vise patologiske funn med megakapillarer og blødninger.
Kalsinose: Sees oftest hos barn og ungdom med juvenil dermatomyositt (JDM) (44% ved JDM vs 4% hos voksne); typisk lokalisert over trykkutsatte områder som knær og albuer (Lilleker JB, 2017).
Pannikulitt, vaskulitt sår og alopesi: Mindre vanlige hudkomplikasjoner.
Lipodystrofi: Kan være en komplikasjon til dermatomyositt og kan feiltolkes som lokalisert muskelatrofi. Andre årsaker til lipodystrofi er steroidinjeksjoner, HIV infeksjon, insulinresistens, polycystisk ovariesyndrom og systemisk lupus erythematosus (SLE).
Dermatomyositt sine dermatitis. En subgruppe med muskelsvakhet, økte muskelenzymer og typiske histologiske dermatomyositt-forandringer i muskelbiopsi, men uten de karakteristiske hudmanifestasjonene.
Interstitiell lungesykdom (ILD)
ILD kjennetegnes av tørr-hoste og dyspne, særlig tydelig ved belastning. For en tidlig diagnose er imidlertid bildediagnostikk viktig. HRCT er sensitiv og fortetninger i lungevevet kan påvises hos 10-80% av myosittpasienter, avhengig av subtype (Lilleker JB, 2017; Tansley SL, 2013; Chaudhry S, 2023). ILD er en betydelig årsak til morbiditet og økt mortalitet (30-40% av dødsfallene ved fibroserende lungesykdom). Screening kan derfor være viktig:
Screening for ILD ved sykdomsdebut og ved eventuelle lungesymptomer senere i forløpet kan være viktig. Pasientene som har høyest risiko er antisyntetasesyndrom-suspekte tilfeller (anti- Jo-1, -PL-7, -PL12, -EJ, -OJ, -KS,-Zo, Ha/YRS), men også ved anti-MDA5 (anti-MDA-relatert myositt), anti Ku og anti Pm/Scl (skleromyositt) og kliniske funn av mekanikerhender (antisyntetasesyndrom), artritt og ulcererende lesjoner (anti-MDA-relatert myositt) (Johnson SR, 2024).
Anamnese: Vanligste lungesymptom er dyspné ved belastning og tørrhoste. Røking kan være en risikofaktor i tillegg til disponerende antistoffer (Lilleker JB, 2017).
Lungefunksjonstester viser et restriktivt mønster med redusert gassdiffusjons-kapasitet (DLCO). FVC reduseres også, mens FEV1 i større grad forblir bevart. Dette medfører at en FEV1/FVC ratio >0,7 som tegn på restriktiv lungesykdom (til forskjell fra obstruktiv lungesykdom).
HRCT thoraks viser vanligvis et mønster som ved non-spesifikk interstitiell pneumoni (NSIP) med mattglassfortetninger (ground glass). Mindre vanlig er «usual interstitial pneumonia» (UIP) med utseende av «bikake mønster». UIP er irreversibel og medfører den dårligste prognosen.
Komplikasjoner. Lunge-manifestasjonene kan kompliseres av pulmonal hypertensjon, sjeldnere pneumo-mediastinum. ILD er sammen med malignitet og infeksjoner den vanligste årsaken til redusert overlevelse ved myositt (Marie I, 2001; Yamasaki Y, 2011).
Kardiale manifestasjoner påvises klinisk hos ca. 9% (Lilleker JB, 2017), men er histologisk til stede hos over 70% av pasientene hvis subkliniske tilfeller medregnes (Zhang L, 2012). Hovedmanifestasjon er myokarditt som kan resultere i hjertesvikt og arytmier (Hanna B, 2025). Arytmier oppstår som følge av påvirkning av det intrakardiale ledningssystemet og er forbundet med økt mortalitetsrisiko.
Ved langvarig myositt foreligger i tillegg økt risiko for tidlig utvikling av aterosklerose (Schwartz T, 2016). Denne er relatert til økt forekomst av tradisjonelle risikofaktorer som høy BMI, diabetes mellitus og dyslipidemi (Hanna B, 2025).
Screening for kardiale manifestasjoner er derfor aktuelt (Oldroyd, 2022; Drazner MH, 2025):
- EKG kan være nyttig som innledende, orienterende undersøkelse, men er ikke en sensitiv screeningmetode.
- Laboratoriediagnostikk med Troponin I på grunn av dens hjertemuskelsensitivitet (95%), til forskjell fra Troponin T som påvirkes av skjelettmuskelaffeksjon. (Shah M, 2023).
- Kardial MR (multiparametrisk kvantitativ MR) har også vist seg å være en god diagnostisk metode (Huang L, 2022).
- Ekkokardiografi kan bl. a. vurdere om tegn til kardial svikt foreligger.
Artritt er ofte assosiert med spesielle subgrupper av myositt, spesielt blant pasienter med anti-MDA5 positivitet, antisyntetase syndrom (ASS) og ved overlapp mot revmatoid artritt (RA) Ved fravær av anti-CCP-antistoff (som er assosiert med RA) er artrittene ved myositt vanligvis ikke erosive. Hos pasienter med antisyntetase syndrom og artritt påvises anti-CCP-antistoffer hos omtrent en tredjedel (Meyer A, 2015).
Malignitet/kreft
Malignitet/kreft kan ses hos ca. 13% av pasientene med myositt. Den økte risikoen relateres til myositt-subgrupper. Voksne med dermatomyositt har størst risiko (Lilleker JB, 2017). Se også avsnittet “Kreft-assosiert myopati” nedenfor.
Tabell. Kjennetegn til hjelp i diagnostikk av ulike myositter. Modifisert etter “Leitlinien für Diagnostik und Therapie in der Neurologi”, DGN, 2022 (dgn.org/leitlinien)
| Kjennetegn | Polymyositt | Dermatomyositt (DM) og JDM | Inklusjonslegememyositt | Immunmediert myositt | Antisyntetase syndrom |
| Kvinner: menn | 2:2 | 2:1 | 1:3 | kvinner>menn | kvinner>menn |
| Vanligste debutalder | alle aldre | DM: fra 16 år. JDM til 16 år | >45 år | vanligvis >18 år | vanligvis voksen alder |
| Forløp | akutt-subakutt | akutt-subakutt | kronisk >12 måneder | akutt-subakutt >80% | akutt-subakutt |
| Kraftsvikt/pareser | proksimal>distal | Proksimal>distal | Proksimal=distal, asymmetrisk. Kne-strekkere ≥hofte-fleksorer. Finger-fleksorer ≥ skulder-abduktorer. | proksimale underekstremiteter > overekstremiteter. Symmetrisk. | Proksimal >distal |
| CK | opp til 50x | normal til 50x | normal til 15x | opp til 50x | opp til 50x |
| EMG og MR | EMG: myopatisk i aktive faser. MR: Ødem, kontrastmiddel-opptak. Atrofi og fibrose/fettinnlagring i kroniske forløp. | EMG: myopatisk i aktive faser. MR: Ødem og kontrastmiddelopptak. Atrofi og fibrose/fettinnlagring i kroniske forløp. | EMG: myopatisk. I langt kommet stadium ses også kronisk nevrogene forandringer. MR: lite eller ingen aktivitetstegn, men tydelig bindevev/fettinnlagring. | EMG: myopatisk i aktiv fase. MR: Ødem og kontrastmiddelopptak. Ved kronisk forløp ses atrofi og fibrose/fettinnlagring. | EMG: Myopatisk i aktiv fase. MR: Ødem, kontrastmiddelopptak. Ved kronisk forløp ses atrofi og fibrose/fettinnlagring. |
| Dysfagi/ekstramuskulære manifestasjoner: hud, hjerte, lunger | Dysfagi mulig. Ikke hudmanifestasjon. Myokarditt mulig. Interstitiell lungesykdom (ILD) | Dysfagi mulig. Hudaffeksjon er typisk. Myokarditt sjelden. Lungesykdom særlig ved MDA5 antistoff. JDM: kalsinose. | Dysfagi typisk (2/3). Ikke hud-manifestasjon. Sjelden og mild kardial affeksjon. | Dysfagi mulig. Ikke hudmanifestasjon. Myokarditt mulig. Sjelden lungemanifestasjon. | Dysfagi er vanlig initialt. Mekanikerhender, Raynauds fenomen. Artritt. Lungemanifestasjon kan være alvorlig. Kardial manifestasjon mulig. |
| Kreft-assosiasjon | Uvanlig | hos voksne. Særlig ved TIF1γ og NXP-2 antistoff. | nei | Sjelden. HMGCR eller uten antistoff disponerer litt. | Nei |
| ILD | 20-80% | Klinisk 20%, HRCT 78%. MDA5 antistoff, alder >45 år, feber, artritt og høy CRP disponerer for aggressiv ILD | Nei | 4% | 20-80%. Kjernesymptom ved antisyntetase syndromet |
| Muskelbiopsi | Som immunmediert myopati eller uspesifikk myositt. Perivaskulær perimyseal/endomyseal inflammasjon. Endomyseale CD8+T-celler | Perifascikulær atrofi. Perivaskulær inflammasjon. Redusert kapillærtetthet, MHC-1 ekspresjon på perifascikulære fibre. | Inflammatorisk infiltrat, sarkoplasmatiske “rimmed vacuoles”, amyloid-avleiringer, inklusjonslegemer, Ragged red Fibers, COX negative fibre. | Nekrotiske og regenererende fibre, minimale celleinfiltrater | Som ved immunmediert myopati eller uspesifikk myositt. Perivaskulær perimyseal inflammasjon. Endomyseale CD8+ T-celler |
Undersøkelser
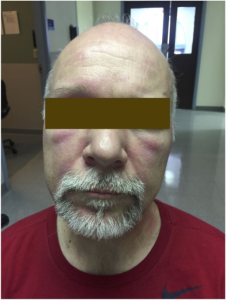
Myositt-diagnosen baseres på en kombinasjon av ulike undersøkelser. Tilstanden må skilles fra en rekke differensialdiagnoser (se avsnitt nedenfor), inklusiv non-inflammatoriske muskelsykdommer (myopatier).
Etter anamnese, klinisk undersøkelse og påvisning av høy CK, bør man bestemme hvilke antistoff som kan forventes. Utenom ANA-test er myositt-spesifikk “myositt-blott” aktuelt. Disse som tilbys av immunologiske laboratorier (Ashton C, 2021). Screening av øsofagus-funksjon, lunger og hjerte kan også være aktuelt.
Anamnese: Familie anamnese. Hvilke symptomer dominerer: svakhet, smerte eller stivhet? Når oppstår symptomene; I hvile, under eller etter fysisk anstrengelse (gå opp trapper, reise seg fra stol)? Debut alder? Hvor raskt har symptomene utviklet seg? Medikament forbruk (statiner, andre)? Symptomer på andre systemiske bindevevssykdommer? Foreligger symptomer fra lunger, hud, hjerte eller andre aktuelle organer?
Klinisk undersøkelse: Det gjøres helst en generell undersøkelse som omfatter hud, lunger, hjerte og andre organer. Muskulaturen vurderes spesielt; proksimal / distal, symmetrisk / asymmetrisk? Hypertrofi / atrofi? (Hypertrofi ses hos noen pasienter med muskeldystrofi). Fascikulasjoner? (Ses ved nevromuskulære tilstander).
-Test av muskelstyrke. Ved orienterende undersøkelse kan musklenes form og størrelse avdekke hypertrofi, atrofi, asymmetri, fascikulasjoner eller spenninger. Smerter ved palpasjon/lett trykk vurderes, samt tegn til kraftsvikt når pasienten reiser seg fra stolen og fra huk uten å støtte seg. Tilsvarende bør armene kunne eleveres over horisontalt nivå uten problemer, også mot lett motstand. Standardiserte tester kan være nyttige verktøy i oppfølging av pasienter, særlig for å vurdere behandlingseffekt og om behandlingsmål oppnås.
Fysioterapeuter kan teste direkte muskelstyrke og utholdenhet (Oldroyd AGS, 2020). Til test av myositt pasienter er der utviklet spesifikke tester; Muskelstyrke ad modum Kendall og FI2 test (Alexanderson H, 2006; Kendall HO, Kendall FP, Wadsworth GE. Muscles : testing and function. 2nd ed. ed. Baltimore: Williams and Wilkins; 1971).
-6-minutter gangtest gir en vurdering av fysisk gangfunksjon (antall meter tilbakelagt i løpet av 6 minutter rask gange). Ved kontroller over tid kan eventuell sykdomsprogresjon synliggjøres.
Laboratorieprøver. Generelt kan prøvene omfatte CRP, SR, Hb, leukocytter med differensialtellinger, elektrolytter, lever-, nyre- og thyreoidea-funksjonsprøver, kreatin kinase (CK), LD og glukose. ved mistanke om kardial manifestasjon kan troponin være aktuelt. Vær oppmerksom på at Troponin T kan øke ved myositt, også uten sikker hjertemuskelaffeksjon. Cortisol (morgenverdi) er aktuelt ved mistanke om binyre over- eller under-funksjon. Urin stiks: ved høy CK kan myoglobin slå ut som hemoglobin/blod.
-Muskelenzymer; CK, LD, ASAT. Disse er vanligvis forhøyet, men ikke alltid. Noen ganger finner man normal CK med moderat forhøyet LD. CK stammer fra muskelcellenes cytoplasma (sarkoplasma), og mesteparten utgjøres av isoenzymet CK MM. Nivået av CK ligger oftest mellom 2-20 ganger øvre normalverdi.
- CK- forhøyelse sees også ved mange andre tilstander som traume, eksessivt muskelarbeid, trening (overtrening: rabdomyolyse), infeksjoner, toksisk påvirkning og de non-inflammatoriske muskeldystrofiene. Hos ca. 0,7% friske er CK idiopatisk forhøyet (Lilleng H, 2011). Forhøyede CK -nivåer halveres ca. hver 24-36 timer dersom utløsende årsak er fjernet. Normalisering i løpet av 3-5 dager forventes, slik at noen dagers treningspause før prøvetakning anbefales.
- -Troponin I, troponin T; Troponin I er en mer følsom markør for hjerteaffeksjon enn Troponin T. -ANA, myosittspesifikke- og assosierte antistoffer; vennligst se immunologiske undersøkelser nedenfor:
Immunologiske undersøkelser. Myositt spesifikke antistoffer (MSA) er immunologiske tester som nesten utelukkende sees ved inflammatoriske myopatier. Dette til forskjell fra myositt-assosierte auto-antistoffer (MSA) som ofte forekommer også ved andre systemiske bindevevssykdommer. MSA har de siste 20-årene bidratt betydelig til diagnostikk, utredning og behandling av myositt. Omtrent 70% av pasientene med myositt har slike antistoffer. I noen tilfeller (ca. 30%) påvises flere antistoffer samtidig, noe som kan vanskeliggjøre spesifikk klassifisering av sykdommen. Årsaken er ofte overlappsyndromer eller at ELISA-testene som rutinemessig brukes ikke er helt spesifikke. Immunpresipitasjonstester (IIF) er mer arbeidskrevende, men spesifikke og multipositivitet for antistoffer påvises da sjelden (ca. 8%) (Loganathan A, EULAR, 2024; McMorrow FK, 2024).
Tabell 1. Oversikt over myositt-spesifikke antistoff (modifisert etter Lundberg I, 2021)
| Antistoff | Målantigen | Forekomst | Kliniske kjennetegn |
| Antisyntetase-antistoff | Antisyntetase syndrom; Proksimal myositt (PM eller DM), ILD, artritt, Raynauds, mekaniker hender og feber, Utslett på halsen. | ||
| -Anti-Jo-1 | Histidyl-tRNA-syntetase | 20% | Antisyntetase-syndrom |
| -Anti-PL-7 | Thronyl-tRNA-syntetase | 5-10% | Antisyntetase-syndrom |
| -Anti-PL-12 | Alanyl-tRNA-syntetase | <5% | Antisyntetase-syndrom |
| -Anti-EJ | Glycyl-tRNA-syntetase | 5-10% | Antisyntetase-syndrom |
| -Anti OJ | Isoleucyl-t-RNA-syntetase | <5% | Antisyntetase-syndrom |
| -Anti KS | Asparginyl-tRNA-syntetase | <5% | Antisyntetase-syndrom |
| -Anti-Zo | Phenylalanin-tRNA-syntetase | <1% | Antisyntetase-syndrom |
| -Anti Ha/YRS | Thyrosyl-tRNA-syntetase | <1% | Antisyntetase-syndrom |
| Immunmediert myopati (IMNM) | |||
| -Anti-SRP | Signalgjenkjenningspartikkel | 5-15% | Nekrotiserende myopati, høy CK, «hissig», hjerte |
| -Anti-HMG-CoA reduktase | HMG-CoA-Reduktase | 5-10% | Nekrotiserende myopati med høy CK, statin bruk |
| Dermatomyositt | |||
| Anti-Mi-2 | Mi-2α/Mi-2β. Proteiner i helikase-familien | 5-10% blant dermatomyositt (DM) | Typiske hudforandringer: panne og rundt øyne (heliotropt), sjal-tegn, V-tegn, Gottrons tegn og papler, Proksimal myositt. |
| Anti-TIF1-γ | Transcritional intermediary factor 1γ | 20% blant DM | Assosiert med malignitet. Klinisk manifestasjon: skalp eksem, periorbitalt ødem, heliotropt utslett, poikoderma (pigmentforandringer), ulcera og nekroser, kløe, lipodystrofi, dysfagi, myositt, Gottrons tegn og papler. Proksimal myositt. |
| Anti-NXP-2 | Nukleært matriksprotein | 25 (hos DM og Juvenil DM) | Assosiert med malignitet. Hos JDM; assosiert med kalsinose |
| Anti-MDA-5 | Melanom-differensieringsantigen 5 | Amyopatisk dermatomyositt: 50% | Amyopatisk (50%) DM; Alvorlig ILD, ulcerasjoner, alopeci, periorbitalt ødem, Gottrons tegn og papler, mekaniker hender, negleaffeksjon, pannikulitt. (MDA5-syndromet) |
| Anti-SAE | Small ubiquitin-like modifier activating enzyme | 5% blant DM | Hissig hudaffeksjon, dysfagi. Ikke relatert til malignitet |
| Inklusjonslegememyositt | |||
| Anti-cytosolic 5′-nucleotidase 1A (5NT1A) | Sensitivitet 30- 50% (referanse: Felice KJ, 2018), dessverre ikke helt spesifikt for IBM og ses også ved andre tilstander | Dysfagi, myositt kan være asymmetrisk. Distal myositt og atrofi ved håndledd og fingerfleksorer, kne-ekstensorer og ankel-dorsalfleksorer. | |
| Overlapp-syndromer (myositt-assosierte antistoff) | |||
| Anti-Ku, anti-I1 RNP, anti-Ro/SSA, anti-La/SSB, anti-Pm/Scl | Overlapp mot andre systemiske bindevevssykdommer | Ku: RA, Systemisk sklerose, myositt og overlappsyndromer. RNP: MCTD. Ro og La: Sjøgrens, subakutt kutan lupus. Pm/Scl: systemisk sklerose |
Bildediagnostikk
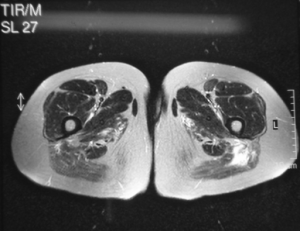
MR-undersøkelse.
Lårmuskulaturen undersøkes oftest, da det er størst sjanse for å se forandringer her.
-Muskel- og fascieødem tyder på inflammasjon, mens fettinfiltrasjon og atrofi tyder på kroniske forandringer.
-MR-bilder kan til en viss grad differensiere mellom poly- og dermatomyositt. Dermatomyositt er ofte preget av mer fascieødem (Pilania K, 2021).
-Ødem og fett-infiltrasjon er ikke spesifikt for myositt og kan sees også ved andre tilstander, for eksempel muskeldystrofier.
-MR av muskulatur brukes også til å å finne egnet sted for biopsi, da muskelinflammasjonen ofte er flekkvis fordelt.
Ultralyd med Doppler kan i noen tilfeller identifisere områder med muskelinflammasjon. Undersøkelsen er da nyttig for lokalisering av muskelbiopsi og for vurdering av behandlingsrespons (Conticini E, 2023).
Kapillaroskopi av neglefolder kan vise patologiske forandringer med megakapillærer og endret arkitektur. Dette kan minne om systemisk sklerose, spesielt ved tilstedeværelse av antistoffene MDA5 eller TIF-1-γ foreligger (Mugii N, 2023).
CT-undersøkelser. HRCT lunger tas for å utelukke lungeaffeksjon ved symptomer eller som screening. Konvensjonell CT-undersøkelse brukes ved mistanke om malignitet. Ved lunge-manifestasjon viser HRCT initialt et NSIP mønster, oftest lokalisert dorso-basalt bilateralt. Senere i forløpet kan fibrose og et UIP mønster forekomme. Utseende og lokalisering av lungevevsaffeksjonen kan gi indikasjoner på hvilken subtype myositt eller antistoffgruppe (antisyntetase, anti-MDA5, anti-SRP) pasienten tilhører (Laporte A, 2022). Vennligst les om lungesykdom i eget kapittel.
Røntgen øsofagus med svelging av barium kontrastmiddel kan kartlegge dysfunksjon ved svelging. Affeksjon av svelgemuskulatur (dysmotilitet) er ikke uvanlig ved myositt og alvorlig affeksjon regnes som er et dårlig prognostisk tegn. Dysmotilitet og svelgevansker kan øke risikoen for aspirasjon og pneumoni og medføre betydelige svelgevansker (dysfagi). De kan på sikt da medføre alvorlig vekttap og behov for sonde- eller PEG-ernæring. Det kan også være assosiert med malignitet (Lu X, 2014).
PET/CT kan vurderes for utelukke tegn til malignitet, særlig ved dermatomyositt hos voksne. Undersøkelsen kan også vise eventuell inflammasjon i lunger (Yildiz H, 2022).
Elektromyografi (EMG) kan skille mellom nevrogen (non-inflammatorisk) og inflammatorisk muskulær (myositt) skade. Blant annet måles insersjonsaktivitet som er elektrisk aktivitet utløst av nålestikket. Dette er redusert ved muskelcelletap og økt ved denervasjons-myopati, inflammasjon og metabolske prosesser. Abnorm spontan depolarisering er alltid et tegn på patologi. Ved myositt ses polyfasiske motor unit potentials (MUP), «sharp waves» og repetitive utladinger. Bruk av EMG i utredningen har avtatt og ofte erstattet av de andre metodene (Meyer H-J, 2018).
EKG er aktuelt ved mulig hjerte-manifestasjon.
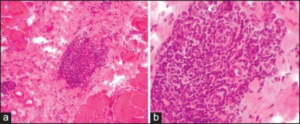
Muskelbiopsi
Biopsi ved myositt kan vise inflammasjon og nekrose, og kan dermed bidra til å skille mellom polymyositt, dermatomyositt og inklusjonslegeme myositt.
- Perimyseal inflammasjon (betennelse i bindevevet rundt muskelfibrene). Dermatomyositt (DM) kjennetegnes av perimyseal inflammasjon (se foto) med overvekt av CD4+ lymfocytter mellom celler og muskelfascikler. Perifasciculær atrofi (kapillærtap og ischemisk skade), redusert kapillartetthet og “membrane-attack-complex” deponering er typiske funn ved DM.
- Endomyseal inflammasjon (betennelse i bindevevet mellom muskelfibrene). Polymyositt (PM) har endomyseal inflammasjon med opphopning av lymfocytter som omgir og invaderer non-nekrotiske fibre, mest CD8+ cytotoksiske celler.
-Ved antisyntetase syndrom (ASS) finner man deponering av C5b-9 komplekser og inklusjoner av myofilament. Forandringene er lokalisert perifascikulært som ved DM (Stenzel W, 2015).
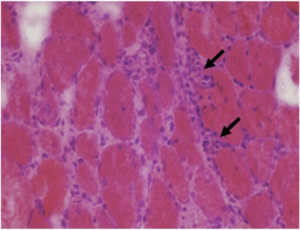
-Inklusjonslegeme myositt (IBM) har perimyseal inflammasjon med CD4+ lymfocytter i tillegg til ragged red fibers som tyder på mitokondrieskade. Filamenter opptrer både i cytoplasma og i nukleus og sees som inklusjoner i mikroskop. Ved elektronmikroskopi kan mikrotubulære filamenter som ved farging med Kongo rødt indikerer beta-amyloid protein ses. Det forekommer også vakuoler med amyloid innhold (rimmed vacuoles= vakuoler som er begrenset av en tykk vegg). IBM er også omtalt i eget kapittel
–Immunmediert nekrotiserende myopati (IMNM) har typisk histologi med uttalt nekrose og lite lymfocyttinfiltrasjon. Histologien ligner da rabdomyolyse og toksisk myositt.
Lungefunksjonstester. Lungefunksjons-tester med vurdering av FVC og FEV og gassdiffusjon (DLCO) gir en god vurdering av lungefunksjonen over tid. Vennligst les om lungefunksjonstester i eget kapittel
Malignitetsutredning: Vennligst se avsnittet om kreft-relatert myositt nedenfor
Diagnostiske kriterier/klassifikasjons kriterier
I 1975 publiserte Bohan og Peter (Bohan A, 1975) diagnostiske kriterier for myositt;
*Forutsetter at andre årsaker til myopati er ekskludert
- 1. Symmetrisk proksimal muskelsvakhet
- 2. Forhøyde muskelenzymer i serum (CK, aldolase, ASAT, ALAT, LD)
- 3. EMG med polyfasiske MUP, ”sharp waves” og repetitive utladninger
- 4. Muskelbiopsi; Degenerasjon, regenerasjon, nekrose, fagocytose og interstitielle mononukleære infiltrater
- 5. Typiske eksantem (som heliotropt eksantem, Gottrons tegn/papler)
- For å stille diagnosen DM må kriterium 5 være til stede
- Mulig PM/DM = 2 kriterier
- Trolig PM/DM = 3 kriterier
- Definitiv PM/DM = 4 kriterier
* Kriteriene forutsetter at andre årsaker til myopati er ekskludert.
Klassifikasjonskriterier EULAR/ACR 2017
Bohan og Peter kriteriene brukes til viss del fortsatt, men der det i 2017 ble publisert nye klassifikasjons kriterier (Lundberg IE, 2017).
Kriteriene deles opp i om det foreligger muskelbiopsi eller ikke. Poeng score på >9 viser høy sannsynlighet for myositt og kriteriene går deretter videre for å klassifisere undergrupper;
Kriteriene summerer score som bygger på følgende parametere med eller uten muskelbiopsi tilgjengelig.
Kalkulator for EULAR/ACR kriterier, vennligst se her
Med disse kriteriene oppnås en sensitivitet og spesifisitet på 90 %.
Spesielle myositt-undergrupper
Alle myositter med antisyntetase antistoffer (oftest anti-Jo-1, anti-PL7 eller anti-PL12) har høy forekomst av interstitiell lungesykdom. Opptil 30% av alle med polymyositt eller dermatomyositt kan defineres som ASS. Det foreligger oftest en triade med ILD, myositt og artritt. I tillegg har mange Raynauds fenomen, mekanikerhender (sprekkdannelse på fingre) og feber (Cavagna L, 2015). Vennligst les om ASS i eget kapittel.
Okulær/orbitalmyositt (øyemanifestasjoner)
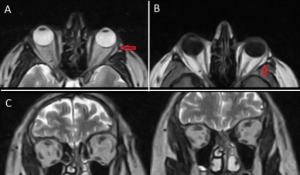
Ved myositt kan øye-manifestasjon forekomme i form av orbital myositt. Dette innebærer inflammasjon i de ekstraokulære musklene (øyemusklene).
Klinisk kan orbital myositt presentere seg med:
- Periorbital smerte: Smerter rundt øyet.
- Diplopi: Dobbeltsyn, som følge av nedsatt koordinasjon av øyemusklene.
- Øyelokksødem: Hevelse i øyelokkene.
Diagnostikk av orbital myositt baseres hovedsakelig på MR-undersøkelse av orbita som vil vise fortykkelse og inflammasjon i de affiserte øyemusklene. I enkelte tilfeller kan biopsi av muskelvevet være nødvendig for å bekrefte diagnosen og utelukke andre årsaker.
Orbital myositt kan ses ved en rekke andre inflammatoriske tilstander ut over idiopatisk myositt. I utredningen kan det være differensialdiagnostisk aktuelt å vurdere: thyreoidea-relatert oftalmopati, infeksjon, vaskulitt (inkludert Behcets sykdom), SLE, kreft, carotid-kavernøs fistel, IgG4-relatert sykdom, sarkoidose, Tolosa-Hunt syndrom og orbitalt lymfom (Pidro A, 2022).
Pasienter med mistenkt eller bekreftet orbital myositt bør følges opp av en oftalmolog for optimal behandling og monitorering av synsfunksjon.
Immunmediert nekrotiserende myopati (IMNM)
Pasienter med anti-HmGCoA-reduktase (HMGCR) eller SRP -antistoffer: Disse har ofte immunmediert nekrotiserende myopati (IMNM) som kan være en “hissig” form for myositt. I løpet av få uker kan IMNM da føre til betydelig muskelsvakhet, dysfagi og høy CK. Hjerteaffeksjon forekommer, spesielt ved anti-SRP, mens lungemanifestasjoner er sjeldnere. Histologisk ses nekrose uten inflammatoriske infiltrater ved IMNM. Dette bildet kan ligne cancer-assosiert myopati (Pinal-Fernandez I, 2018).
-
Anti-HmGCoA-reduktase-relatert myositt: Denne typen myositt er assosiert med statinbruk (kolesterolsenkende medikamenter), men kan også forekomme hos ca. 50% uten statinbruk.
- Seronegative IMNM og HMGCR myopatier: Disse pasientene har en mulig økt forekomst av kreft, og screening kan være aktuelt. (Yang H, 2017).
Behandlingen ved anti-SRP positiv myositt kan bestå av steroider og rituksimab. Mot anti-HmGCoA-reduktase-myositt brukes ofte IVIG i monoterapi.
Vennligst les også om statin-myopati i eget kapittel.
Kreft-assosiert myositt
Når myositt oppstår kort tid før eller etter kreftsykdom, er tilstandene ofte assosiert. Anti-TIF1γ og anti-NXP2 antistoff, som ofte sees ved dermatomyositt (Fiorentino DF, 2013), disponerer for kreft hos voksne. Anti-NXP2 antistoffer kan også påvises hos barn med juvenil dermatomyositt men da uten å være kreft-assosiert. Derimot kan antistoffene da være assosiert til kalsinose. Seronegative IMNM og HMGCR myopatier også medføre en viss økt risiko for kreft (Yang H, 2017).
Tabell: Risikofaktorer for malign sykdom ved myositt (Oldroyd AGS, 2023)
|
«Høy risiko» faktorer
|
«Middels risiko» faktorer
|
«Lav risiko» faktorer
|
|
|
Myositt subtype
|
|
|
|
|
Antistoffer
|
|
|
|
|
Kliniske trekk
|
|
Mannlig kjønn
|
|
Dermatomyositt (DM) er assosiert med malignitet når den oppstår hos voksne. Det er ikke uvanlig at kreft oppdages tre år før og etter debut av dermatomyositt (Dobloug GC, 2016). Internasjonale retningslinjer anbefaler årlig malignitet-screening i 3-5 år etter DM-diagnose hos voksne pasienter. Andre risikofaktorer for malignitet er høy alder, mannlig kjønn og dysfagi (Lu X, 2014). Bryst-, gynekologisk-, GI- og lungecancer er de vanligste typene kreft ved kreft-assosiert myositt (Yang, 2017).
Screening for kreftsykdom kan derfor være aktuelt hos voksne med myositt. Det gjelder spesielt ved kjente risikofaktorer som høy-moderat risiko ihht Tabell: Risikofaktorer for malignitet ovenfor. Anbefalt utredning kan inkludere (Oldroy AGS, 2023):
- Grunnleggende screening: Aktuell anamnese, klinisk undersøkelse, blodprøver med celletellinger, leverfunksjonsprøver, SR, CRP, proteinelektroforese, urin-analyser.
- Mer omfattende utredning kan også inkludere: PSA hos menn, Ca-125, Rtg, men helst CT thorax, CT hals, abdomen/bekken, alternativt PET-CT (ved høy risiko), Mammografi og gynekologisk undersøkelse (helst med supplerende ultralyd) og Hemofec
I tillegg til screening ved diagnose kan supplerende PET/CT, øvre og nedre gastroskopi, samt kontroll etter ett, to og tre år være aktuelt ved “Høy risiko”.
De vanligste tumorene assosiert med myositt er ovarial-, bryst-, lunge-, tarmkreft og lymfom (Dobloug GC, 2015). Vennligst les om malignitet ved revmatiske sykdommer i eget kapittel.
Anti-MDA5 myositt
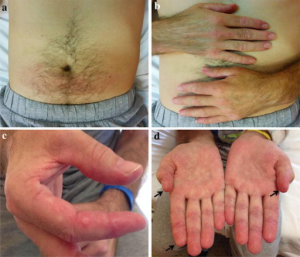
Pasienter med anti-MDA5 antistoff har mindre muskelaffeksjon (lavgradig myositt) sammenlignet med andre typer myositt. De kan imidlertid ha betydelig hudaffeksjon, inkludert nekrotiske sår. Mest alvorlig er at mange utvikler «rapid progressive lung disease», en raskt progredierende lungesykdom, som kan være meget alvorlig og vanskelig å behandle. Utvikling av pneumo-mediastinum forekommer som ytterligere komplikasjon og er et dårlig prognostisk tegn. Antistoffet MDA5 antas å spille en rolle i patogenesen ved å indusere type 1-interferon (Zhang SH, 2019)
Behandlingsalternativer i tillegg til steroider er rituksimab, JAK-hemmere, plasmaferese, intravenøse immunglobuliner og anti-fibrotiske legemidler (Mehta P, 2021: McPherson M, 2022).
Inklusjonslegeme myositt (IBM) skiller seg ut fra de andre myosittene. Den er dobbelt så hyppig hos menn og debuterer vanligvis etter 50 års alder. IBM har også en langsommere progresjon sammenlignet med andre myositter. Pasientene har dessuten ofte affeksjon av distal muskulatur (finger-fleksorer, tibialis anterior) og en asymmetrisk fordeling. Mange har symptomer fra en svekket svelgmuskulatur, mens interstitiell lungesykdom (ILD) er uvanlig. IBM reagerer dårlig på immunsuppressiv behandling. IBM er nærmere beskrevet i eget kapittel.
Infeksjons-indusert myositt.
Virus
Hepatitt E er endemisk i Asia og Afrika, men er sjelden i vår del av verden. Vanligvis er sykdomsbildet mildt, men tilfeller med alvorlig myositt er sett (Mengel AM, 2016). Også nevrogene smerter kan være en del av sykdomsbildet (Abravanel F, 2018). Inkubasjonstid er vanligvis 4-6 uker (Folkehelseinstituttet, 2019; Waquar S, 2021).
Andre. Hepatitt B og C, COVID-19, parvovirus, CMV med flere kan en sjelden gang indusere myositt (Narayanappa G, 2021; Saud A, 2021), men også polymyalgia revmatika-lignende sykdombilde (Ottavani S, 2022).
Bakterier, sopp og parasitter
Stafylokokker- og en rekke andre bakterier, sopp og parasitter kan medføre myositt, men er sjelden (Narayanappa G, 2021).
Svangerskap
Svangerskap hos kvinner med inflammatorisk myositt medfører en økt risiko for komplikasjoner. Det er rapportert økt forekomst av spontanaborter, dødfødsler og premature fødsler. Risikoen er særlig uttalt hos gravide med aktiv sykdom under svangerskapet.
På grunn av muskelsvakhet kan sectio være aktuelt for å gjennomføre fødselen på en trygg måte, spesielt om muskelkraften er betydelig redusert i bekken- og lårmuskulatur som er essensiell for en vaginal fødsel (Ito Y, 2021). For supplerende informasjon og anbefalinger henvises til info fra NKSR.
Differensialdiagnoser
Mange tilstander kan etterligne myositt, men en grundig vurdering (se “Undersøkelser” ovenfor) ovenfor vil vanligvis avgrense disse.
Hyppige differensialdiagnoser:
- Kroniske generaliserte muskelsmerter ved fibromyalgi: Ofte sett hos kvinner. Tilstanden kan ligne myositt da den også har utbredte muskelsmerter, men kjennetegnes primært av smerter i bindevev og muskelfester uten objektiv muskelsvakhet eller forhøyede muskelenzymer.
- Polymyalgia revmatika: Kan oppstå hos eldre personer (over 70 år) i løpet av dager. Sykdommen kan forveksles med myositt fordi den også gir uttalte muskelsmerter og stivhet, spesielt i skulder- og bekkenområdet, men uten signifikant muskelsvakhet eller forhøyede CK-verdier.
- Hypothyreose: Lavt stoffskifte kan gi muskelsvakhet, smerter og kramper som kan minne om myositt. det har sammenheng med at metabolismen i muskelcellene påvirkes.
- Tyreotoxikose: Høyt stoffskifte kan også føre til muskelsvakhet og tretthet. Symptomene kan ligne symptomene på myositt.
- Steroid-myopati: Kan oppstå ved langvarig bruk av kortikosteroider, særlig i høye doser. Tilstanden ligner myositt fordi den også fører til muskelsvakhet, spesielt i de proksimale musklene.
Sjeldne differensialdiagnostiske tilstander som kan kreve nærmere utredning ved “seronegativ” eller atypisk myositt er non-inflammatorisk myopati med late-onset muskeldystrofier og metabolske myopatier, samt Lambert-Eaton myasteni (ved malignitet), mitokondrie-myopatier, diabetisk myonekrose og infeksiøse myopatier (Harmann P, 2013). Immunmediert nekrotiserende myopati (IMNM) kan histologisk være vanskelig å skille fra rabdomyolyse eller toksisk myopati av annen årsak fordi det er lite eller ingen inflammasjonstegn i muskelcellene. Imidlertid vil mange ha antistoff i form av anti-HMGCR eller anti SRP.
Generelt bør distal muskelsykdom med manifestasjoner i fingerfleksorer (underarmer) og fotekstensorer (legger) eller fascikulasjoner tilsi utredning for inklusjonslegeme myositt, men også nevromuskulær sykdom som amyotrofisk lateralsklerose (ALS) og Charcot-Marie-Tooth sykdom.
Liste (alfabetisk) over differensialdiagnoser:
- ALS (amyotrofisk lateralskerose): En progressiv nevrodegenerativ sykdom som angriper motoriske nerveceller. Det kan føre til muskelsvakhet og atrofi og ligne på myositt. Likhet med myositt: Både ALS og myositt kan presentere med muskelsvakhet og lett forhøyet CK, men ALS kjennetegnes av distale affeksjoner, hyperrefleksi, muskelfibrillasjoner og spasmer, mens myositt oftere involverer proksimale muskler (Feldman EL, 2022).
- Amyloid myopati: En sjelden tilstand der amyloidproteiner avleires i musklene. Dette kan føre til muskelsvakhet, smerte og atrofi. Likhet med myositt: Kan gi muskelsvakhet og smerter, men amyloid myopati har ofte subkutane forandringer og proteinuri. Diagnosen kan bekreftes med biopsi (Kongorødt farging) (Parthiban GP, 2023).
- Carnitine-palmitoyl-transferase II mangel; En metabolsk sykdom som påvirker musklenes evne til å bruke fett som energikilde, noe som kan føre til muskelsmerter og -svakhet, spesielt etter trening. Likhet med myositt: Gir muskelsmerter, men utløses av aktivitet og mangler systemiske symptomer (Lehmann D, 2017).
- Diabetisk muskelsvinn (amyotrofi) og diabetisk muskelinfarkt: Komplikasjoner til diabetes som kan føre til akutt muskelsvakhet og smerte, ofte i låret. Likhet med myositt: Kan gi akutt muskelsvakhet, men oppstår hos pasienter med diabetes type 2 og har ofte asymmetrisk fokal affeksjon. EMG kan skille diabetisk amyotrofi fra myositt (Hernandez-Ochoa EO, 2017).
- Elektrolytt mangel: Ubalanse i elektrolytter som kalium, kalsium og magnesium kan føre til muskelsvakhet, smerter og kramper. Likhet med myositt: Kan gi muskelsvakhet og smerter, men korrigeres ved å gjenopprette elektrolyttbalansen.
- Eosinofil myositt: En sjelden inflammatorisk muskelsykdom med infiltrasjon av eosinofile i muskelvev. Multiorganaffeksjon, smerter og svakhet i proksimal muskulatur, Raynauds, vaskulitt i små blodårer, CK kan være forhøyet. Differensialdiagnoser er hypereosinofilt syndrom (IgE, eosinofile leukocytter > 1.5 × 109/L og hudaffeksjon) (Fermon C, 2022).
- Eosinofil fasciitt En sjelden tilstand som forårsaker inflammasjon og fortykkelse av muskelfascier. Likhet med myositt: Kan gi muskelsmerter og stivhet, men affiserer primært fascier og har typiske inndragninger i hud og underhud. CK er oftest normal (Mazilu D, 2023).
- Fibromyalgi. En kronisk smertetilstand karakterisert ved utbredte muskelsmerter, tretthet og søvnproblemer. Likhet med myositt: Gir muskelsmerter og tretthet, men mangler objektive funn som muskelsvakhet eller forhøyet CK.
- Glykogen lagringssykdom type V: McArdles sykdom/ fosforylase mangel. En metabolsk sykdom som påvirker musklenes evne til å lagre og bruke glykogen, noe som fører til muskelsmerter og kramper under trening. Likhet med myositt: Gir muskelsmerter, men utløses av aktivitet og er forbundet med spesifikke enzymmangler (Nascimento J, 2024).
- Glykogen lagringssykdom type II, Adult acid maltase mangel (Pompes sykdom); En metabolsk sykdom som fører til opphopning av glykogen i muskelceller, noe som kan forårsake muskelsvakhet og respirasjonsproblemer. Likhet med myositt: Kan gi muskelsvakhet, men har et karakteristisk klinisk forløp og påvises ved enzymmålinger og genetisk testing (Labella B, 2023).
- GVHD (graft versus host): En komplikasjon etter transplantasjon der donorceller angriper mottakerens vev, inkludert muskler. Likhet med myositt: Kan gi muskelsvakhet og inflammasjon, men oppstår etter transplantasjon og har spesifikke histologiske funn (Kvinge AD, 2022).
- HIV infeksjon. Kan forårsake muskelsvakhet og -smerter, enten direkte eller som følge av opportunistiske infeksjoner eller medikamenter. Likhet med (inklusjonslegeme-) myositt: Kan gi muskelsvakhet og forhøyet CK, men diagnostiseres ved HIV-test. Antall CD4 T-celler i blodet korrelerer dårlig med myopati-symptomer (Nelke C, 2022).
- Hypothyreose: Lavt stoffskifte kan føre til muskelsvakhet, smerter og stivhet. Likhet med myositt: Kan gi muskelsvakhet og smerter, men diagnostiseres ved blodprøver som viser høy TSH og lav f-T4.
- Inklusjonslegeme myositt; En inflammatorisk (lavgradig) muskelsykdom som oftest rammer eldre voksne og er karakterisert ved langsom progresjon og distal muskelsvakhet. Likhet med myositt: Gir muskelsvakhet, men har lavere CK, langsom progresjon, distal affeksjon, ingen antistoff (evt utenom Anti-cN1A) og typiske biopsifunn.
- IMNM (immun-mediert Nekrotiserende Myositt). En sjelden inflammatorisk muskelsykdom som kan være assosiert med statinbruk. Likhet med myositt: Gir muskelsvakhet og smerter, men kjennetegnes av nekrose i muskelbiopsi og kan ha HMGCR antistoff.
- Kalsinose: Avleiring av kalsium i hud og bløtdeler. Kan forekomme ved ulike tilstander, inkludert systemisk sklerose og juvenil dermatomyositt, men er ikke i seg selv en myositt. Likhet med myositt: Kan sees ved dermatomyositt, men er ikke spesifikt for myositt.
- Katapleksi. Plutselig tap av muskelkraft, ofte utløst av sterke følelser, som er et karakteristisk symptom ved narkolepisi og ikke forveksles direkte med myositt. Likhet med myositt: Involverer muskelsvakhet, men er episodisk og utløses av emosjoner (Mirabile VS, 2023).
- Kennedy sykdom (Spinal and bulbar muscular atrophy, SBMA): En genetisk sykdom som primært rammer menn og forårsaker muskelsvakhet og atrofi, spesielt i ansikts-, bulbar- og proksimale muskler. Likhet med myositt: Kan gi muskelsvakhet og forhøyet CK, men rammer spesifikke muskelgrupper og er assosiert med endokrine forandringer (Au KM, 2003).
- Lambert-Eaton syndrom: En autoimmun sykdom som ofte er assosiert med kreft og forårsaker muskelsvakhet, spesielt i proksimale muskler. Likhet med myositt: Gir muskelsvakhet, men har antistoff mot voltage-gated calcium kanal (VGCC) og karakteristiske EMG-funn (Kesner VG, 2018).
- Makro-CK. En tilstand der CK-enzymet binder seg til andre molekyler i blodet, noe som kan føre til falsk forhøyede CK-målinger. Likhet med myositt: Kan gi forhøyet CK, men er ikke assosiert med muskelsvakhet eller betennelse. Makroenzymer er normale enzymer (eller isoenzymer) som binder seg enten til immunglobuliner (IgG) = Type 1 eller lipoproteiner og andre substanser (Type 2) og dermed akkumuleres i serum. De er ikke frie enzymer, men forårsaker falsk forhøyede CK-målinger. Makro-CK ses oftest hos personer over 60 år. Makro-CK kan foreligge med- eller uten assosiert sykdom, inklusiv kronisk leversykdom og malignitet.
- Medikamentindusert myopati. Statiner. Smerter med eller uten forhøyet kreatin kinase (CK) i blod. Medikamentanamnese viktig. Høye kortikosteroid-doser (Prednisolon) over lang tid: Steroid myopati: CK normal. Andre: Amiodaronhydroklorid (Cordarone) mot hjerterytme forstyrrelser, Plaquenil, kokain, alkohol, kolkisin. Likhet med myositt: Kan gi muskelsvakhet og smerter, men forbedres ofte ved seponering av medikamentet (Wu M, 2024).
- Mitokondrie myopati: En gruppe sykdommer som påvirker mitokondriene, cellenes energifabrikker, noe som kan føre til muskelsvakhet, tretthet og andre symptomer. Likhet med myositt: Kan gi muskelsvakhet, men har ofte multisystemiske manifestasjoner og spesifikke biokjemiske og genetiske funn. Encefalomyopati, laktat acidose, slag-lignende symptomer kalles (MELAS). Se også MERRF nedenfor (Orsicci D, 2021).
- Muskeldystrofi: En gruppe genetiske sykdommer som forårsaker progressiv muskelsvakhet og atrofi. Likhet med myositt: Gir muskelsvakhet, men har et karakteristisk klinisk forløp og påvises ved genetisk testing og muskelbiopsi.
- Myastenia gravis: En autoimmun sykdom som forårsaker muskelsvakhet og tretthet, ofte i øyemuskler og andre ansiktsmuskler. Likhet med myositt: Gir muskelsvakhet, men har normal CK, karakteristisk EMG og antistoff mot acetylkolinreseptorer (Mishra AK, 2024).
- Myoklonisk Epilepsi med «Ragged Red Fibers» (MERRF). En mitokondriesykdom som forårsaker epilepsi, muskelsvakhet og andre nevrologiske symptomer. Likhet med myositt: Kan gi muskelsvakhet, men har karakteristiske nevrologiske funn og “Ragged Red Fibers” i muskelbiopsi. (Finsterer J, 2025).
- Parkinsons sykdom. En nevrodegenerativ sykdom som primært påvirker motorikk og forårsaker tremor, rigiditet og bradykinesi. Likhet med myositt: Kan gi muskelstivhet, men har karakteristiske nevrologiske funn (Slouma M, 2023).
- Periodisk paralyse: En gruppe sjeldne genetiske sykdommer som forårsaker episoder med muskelsvakhet eller paralyse. Likhet med myositt: Gir muskelsvakhet, men er episodisk og utløses av faktorer som stress eller inntak av karbohydrater (Hariri BA, 2024) .
- Polymyalgia revmatika. Forårsaker smerte og stivhet i skuldre og hofter, oftest hos eldre voksne. Likhet med myositt: Kan gi muskelsmerter og stivhet, men rammer primært skuldre og hofter, har høy SR og CRP, og normal CK.
- Post polio syndrom. Kan oppstå mange år (etter 15-30 år, ofte i 35-60 års alder) etter poliomyelitt og forårsaker muskelsvakhet, smerte og tretthet. Likhet med myositt: Gir muskelsvakhet, men oppstår hos personer med tidligere poliomyelitt (Punsoni M, 2023).
- Rabdomyolyse: Muskelceller brytes ned og frigjør myoglobin i blodet, noe som kan føre til nyreskade. Likhet med myositt: Kan gi muskelsmerter og forhøyet CK, men CK er svært høy over 10.000 (Obs! nyreskaderisiko) og utløses av skade, intoksikasjon eller kritisk sykdom. Rabdomyolyse og myalgi syndrom assosiert med RY1 mutasjon. Økt risiko for hypertermi. Kan ha moderat forhøyet CK og muskel-manifestasjoner
- Refsums sykdom. En sjelden genetisk sykdom som forårsaker nevrologiske symptomer, inkludert muskelsvakhet og atrofi. Likhet med myositt: Kan gi muskelsvakhet, men har karakteristiske nevrologiske (kronisk polynevropati med pareser, cerebellære symptomer med ataksi), oftalmologiske funn som retinitis pigmentosa og distal muskelatrofi (Waterham HR, 2021).
- Sarkoid myopati: En sjelden manifestasjon av sarkoidose der granulomer dannes i muskelvev. Likhet med myositt: Kan gi muskelsvakhet, men er ofte asymptomatisk og assosiert med sarkoidose i andre organer.
- Skleromyositt: En sykdom med overlappende symptomer mot systemisk sklerose som kan gi muskelsvakhet og hudforandringer. Likhet med myositt: Gir muskelsvakhet, men har også hudforandringer som ligner på systemisk sklerose.
- Spinal muskelatrofi: En gruppe genetiske sykdommer som forårsaker progressiv muskelsvakhet og atrofi, spesielt i proksimale muskler. Likhet med myositt: Kan gi muskelsvakhet, men har karakteristiske kliniske funn og påvises ved genetisk testing (Ørstavik K, 2020)
- Statinmyopati: En bivirkning av statiner som kan forårsake muskelsmerter og svakhet. Likhet med myositt: Kan gi muskelsmerter, men forbedres ofte ved seponering av statinene (Somagutta MKR, 2022).
- Steroid-myopati; En bivirkning av langvarig bruk av kortikosteroider som kan forårsake muskelsvakhet. Likhet med myositt: Gir muskelsvakhet, men har normal CK og forbedres ofte ved reduksjon av steroiddosen (Wu M, 2024).
- Subaraknoidal-blødning: Kan forårsake muskelsvakhet, men er akutte nevrologiske hendelser med karakteristiske kliniske funn. Likhet med myositt: Kan gi muskelsvakhet, men er et akutt nevrologisk problem med fokal affeksjon.
- Trichionose: En parasittinfeksjon som kan forårsake muskelsmerter, feber og eosinofili. Likhet med myositt: Kan gi muskelsmerter og forhøyet CK, men er assosiert med inntak av rått kjøtt og eosinofili.
- Viral myositt: En sjelden komplikasjon av virusinfeksjoner som kan forårsake muskelsmerter og svakhet. Ofte rask sykdomsutvikling, kan være begrenset til få muskelgrupper. Effekt av antiviral behandling. Likhet med myositt: Kan gi muskelsmerter og svakhet, men er ofte selvbegrensende og assosiert med en akutt virusinfeksjon. Influensa A and B, H1N1 virus, Coxsackie-virus, Epstein-Barr-virus, herpes simpleks-virus, parainfluensa, adeno-virus, echovirus, cytomegalo-virus (CMV), meslinger-virus, varicella zoster, Human immunodeficiency virus (HIV), parvovirus-B19, Dengue feber.
Behandling
Behandlingsmål ved myositt
Redusere muskelinflammasjon: Normalisere muskelenzymer (spesielt CK) og redusere eller normalisere inflammasjonsmarkører.
Gjenopprette eller bevare muskelstyrke og funksjon, f eks for å utføre daglige aktiviteter.
Forhindre eller behandle ekstramuskulære manifestasjoner: Dette kan innebære å kontrollere eksantem ved dermatomyositt, behandle og stabilisere interstitiell lungesykdom (ILD) og kardiale manifestasjoner, håndtere dysfagi og identifisere og behandle eventuell kreft (spesielt ved dermatomyositt hos voksne). Å redusere symptomer og forbedre livskvalitet, samt minimere medikamentelle bivirkninger er også viktige mål.
Behandlingsstrategier er i stor grad empirisk basert og individualiseres basert på grad av muskelinvolvering, ekstramuskulære manifestasjoner, myosittspesifikke antistoffer (MSA), alder og komorbiditet og myositt-subtype.
Non-farmakologisk behandling
I tillegg til farmakologisk intervensjon, er individualisert fysioterapi med fokus på muskelrehabilitering og styrketrening avgjørende. Fysisk aktivitet kan fremme mitokondriell funksjon, angiogenese, muskelhypertrofi og redusere inflammasjon.
Individuelt tilpasset: Treningen skal være skreddersydd til den enkelte pasients sykdomsaktivitet, muskelstyrke, smerte og utmattelsesnivå. En fysioterapeut med erfaring innen revmatologi er behjelpelig.
Styrketrening startes med lav belastning og økes gradvis. Fokus kan være på proksimale muskler (skuldre, hofter, lår) som ofte er hardest rammet. Studier viser at styrketrening er trygt og kan bidra til å forbedre muskelstyrke og funksjon, selv blant pasienter med aktiv sykdom når de er under medikamentell kontroll.
Utholdenhetstrening: Gange, sykling og svømming er blant aerobe aktiviteter som kan forbedre kardiovaskulær helse og redusere fatigue. Selv moderat til høy intensitet kan være gunstig, forutsatt at pasienten er hjerte- og lungefrisk og får veiledning. Anbefalt trening kan inkludere relativt hard ergometersykling (60-70% av VO2max), moderat aerob trening fem dager i uken og målrettet styrketrening (30-40% av max) av affiserte muskelgrupper (Alexanderson H, 2018; van Thillo A, 2019).
Tøyning og bevegelighetstrening kan være viktig for å bevare leddenes bevegelighet og forhindre kontrakturutvikling.
Medikamenter
Glukokortikoider (Prednisolon)
Glukokortikoider (prednoisolon, metylprednisolon) er førstevalget i en akutt fase. Dosering individualiseres og basertes på alvorlighetsgraden hos den enkelte pasient. Ofte veldes prednisolon 0,5-1 mg/kg/dag med gradvis nedtrapping (f. eks hver 2-4 uke) avhengig av klinisk respons og kreatin kinase (CK)-nivåer. Data tyder på at 60-80% av pasientene med polymyositt forbedre muskelfunksjonen under behandlingen (Postolova A, 2023). Ved raskt progredierende interstitiell lungesykdom (ILD), spesielt ved antisyntetase syndrom, ved alvorlig myokarditt eller alvorlig dysfagi, velges ofte metylprednisolon (SoluMedrol) 500-1000 mg/dag intravenøst de første tre-fem dagene. Behandlingen med kortikosteroider avsluttes så raskt som mulig, helst innen 3-6 måneder (Postolova A, 2023), men tar ofte 1-3 år.
DMARDs initieres ofte samtidig med glukokortikoider for å redusere steroiddosen (Miller SA, 2015). Førstevalg er ofte metotreksat, alternativt azathioprin eller mykofenolatmofetil. Andrevalg inkluderer intravenøst immunglobulin (IVIG), ciklosporin A og takrolimus. IVIG er aktuell som først-linje-valg ved anti HMGCR myositt (Allenbach Y, 2018 /ENMC).
Rituksimab har vist en responsrate på 70% for myosittgruppene samlet, hvorav 13 % av pasientene oppnådde komplett remisjon. Analyse av subgrupper har vist til dels høyere responsrater: IMNM: 86 %, antisyntetasesyndrom: 70 %, Polymyositt: 69 %, dermatomyositt: 67 % og Juvenil dermatomyositt: 60 %. de vanligste bivirkningene er infusjonsreaksjoner (18,5 %) og infeksjoner (12,4 %) (Rojas LO, 2025).
Rituksimab kan også være effektiv ved myosittassosiert ILD og kardiovaskulære eller kutane manifestasjoner (Andersson H, 2015: Maher TM, 2023). Ved anti-SRP-relatert myositt kan rituksimab være første-linjebehandling (Allenbach Y, 2018 /ENMC).
Det er gjort en metaanalyse basert på over 90 behandlede pasienter i ulike studier. Den konkluderer med at JAK-hemmere har et potensial i behandlingen av dermatomyositt og polymyositt, spesielt med hensyn til hudlesjoner og behandlingen har få forventede bivirkninger. Funnene antyder at JAK-hemmere kan bli et verdifullt behandlingsalternativ (Ma C, 2024).
CAR T-celle behandling (Chimeric Antigen Receptor T-cell therapy)
Forskning på CAR T-cellebehandling for autoimmune sykdommer, inkludert myositt, har vist lovende resultater i enkelte, tidlige studier og kasusrapporter. Behandingen er imidlertid krevende og med risiko for alvorlige bivrikninger. CAR T-cellebehandling vurderes derfor primært for pasienter med alvorlig myositt som ikke har respondert tilstrekkelig på konvensjonelle behandlinger, inkludert biologiske legemidler som rituksimab (Müller F, 2024; Lundberg IE, 2024;
Intravenøst immunglobulin (IVIG)
IVIG kan være effektivt ved polymyositt og dermatomyositt (Aggarwal R, 2022). Dette er andre-linje behandling som brukes ved refraktære tilfeller, inkludert ved spesifikke autoantistoffprofiler (f. eks. anti-SRP, anti-HMGCR), alvorlige organmanifestasjoner som dysfagi eller ILD, blant eldre pasienter, i svangerskap og ved intoleranse eller kontraindikasjon mot standardbehandling. Effekten av IVIG ved inklusjonslegememyositt er mer omdiskutert og generelt dårligere sammenlignet med de andre myositt-subgruppene (Lundberg IE, 2021; Hoa SA, 2007 Allenbach Y, 2018). Bivirkninger inkluderer infusjonsreaksjoner og økt tromboembolisk risiko.
Nintedanib (antifibrotisk medikasjon)
Nintedanib er en tyrosinkinasehemmer som hemmer utviklingen av lungefibrose. Studier ved myositt-assosiert lungesykdom viser lovende, men foreløpig (2025) begrensede resultater. Behandlingen kan vurderes ved myosittassosiert fibrotisk ILD (Flaherty KR, 2019). Samarbeid med pulmonolog er essensielt.
Pneumocystis jirovecii-profylakse:
Trimetoprim+sulfonamid (Bactrim) anbefales ved intensiv immunsuppresjon, spesielt ved samtidig lungesykdom (Liu L, 2023). Doseringen kan være to tabletter daglig som tilsvarer 160 mg trimetoprim og 800 mg sulfametoksazol (160/800 mg).
Behandlingsvarighet og spesielle hensyn
- Den medikamentelle behandlingen av myositt er individuell og varer vanligvis 1-3 år eller lenger.
- Intensiv immunsuppresjon er indisert ved ekstramuskulære manifestasjoner (kardial, pulmonal, dysfagi).
- Ved myositt-relatert ILD kan mykofenolat, alternativt: azathioprin, rituximab, calcineurin-hemmere (ciclosporin, takrolimus) være aktuelle (i den rekkefølgen). Andre muligheter er JAK-hemmer eller cyclofosfamid. Glukokortikoider brukes vanligvis initialt, men er ikke ønskelige på lengre sikt. Hvis behandlingssvikt kan internt skifte av medikamentene (“switch”) eller tilleggsmedikasjon (“add on”) bli aktuelt. Nintedanib og IVIG er da supplerende medikamenter som kan brukes (Johnsom SR, 2024). Alvorlige, non-responsive, progredierende tilfeller bør vurderes for lungetransplantasjon.
- Rituksimab som førstelinjebehandling bør vurderes ved immunmediert nekrotiserende myopati (IMNM) med anti-SRP-antistoffer og alvorlig klinisk forløp, ellers som andrelinje-behandling.
- Ved anti-MDA-5 antistoff og lungemanifestasjon kan kombinasjonsbehandling være aktuelt: glukokortikoider + rituximab (alternativt cyclofosfamid, IVIG, mykofenolat, calcineurinhemmer, eller JAK-hemmer i tillegg til glukokortikoidene). Ved raskt progredierende anti-MDA-5 lungesykdom kan “trippel-behandling” med glukokortikoider og to av de nente DMARDs være nødvendig (Johnsom SR, 2024).
- Kardial manifestasjon med myositt (grad C-D) kan behandles immunsuppressivt med metylprednisolon (7-14 mg/kg over 3 dager) etterfulgt av prednisolon 1 mg/kg/d. IVIG kan vurderes. Hjertesvikt og arrytmi behandles. Begrenset fysisk aktivitet over 3-6 måndeder anbefales også. I svært alvorlige tilfeller vurderes hjertetransplantasjon (Drazner MH, 2025).
- Alvorlig dysfagi behandles med kortikosteroider (0,5-1 g/dag i 3-5 dager) som første-linje-behandling. IVIG brukes ofte i refraktære tilfeller (Oldroyd, 2022), men enkelte anbefaler IVIG også som alternativ første-linje-behandling .
Forebyggende tiltak mot komplikasjoner
- Forebygg opportunistiske infeksjoner (f eks pneumocystis jiroveci)
- Vurder osteoporoserisiko
- Følg opp kardiovaskulær risiko
- Planlegg ev. svangerskap når sykdommen er godt kontrollert og stabil
- Vurder pasientens psykiske helse og livskvalitet.
Prognose
1/3 del av myositt pasientene har monofasisk sykdomsforløp, 1/3 har profylasisk sykdomsforløp og den siste 1/3 del har et kronisk forløp. Overlevelse er avhengig av alder, diagnostisk «delay », ev malignitet, og ILD. Fem-års overlevelse er ca. 95%, 10-års overlevelse 90 % (Danieli MG, 2014).
Mortaliteten ved myositt er funnet å være fire ganger høyere enn i den generelle befolkningen. Første året etter debut er denne enda høyere (opp til 10 x økt). Årsakene er kreft, kadiovaskulær sykdom og lungemanifestasjoner (Dobloug GC, 2018).
I listen nedenfor er lenker til kapitler der andre myopatier er beskrevet:
- Antisyntetase syndrom
- Inklusjonslegeme myositt (IBM)
- Non-inflammatoriske myopatier ( Infeksiøs myositt, toksisk myopati, sekundær myopati til systemisk sykdom, muskeldystrofier. kongenitale myopatier, metabolske myopatier, mitokondrie myopatier. Idiopatiske myopatier.
- Juvenil dermatomyositt
Retningslinjer, anbefalinger og prosedyrer
- Johnson SR, 2024 (ACR: screening for pulmonal komplikasjon)
- Oldroyd AGS, 2023 (malignitetsscreeing ved myositt)
- Revmatologisk forening/Legeforeningen 2020
- Allenbach Y, 2018; ENMC anbefalinger for IMNM
- Lundberg IE, 2017: EULAR Klassifikasjon av myositt
Litteratur
- Musai J, 2024 (antistoff og patogenese)
- Sarwar A, 2023 (polymyositt)
- Halilu F, 2022 (antistoff ved myositt)
- Qudsiya Z, 2023 (dermatomyositt)
- Cheeti A, 2023 (autoimmune myopatier)
- Schmidt J, 2018 (diagnose og behandling)
- McGrath ER, 2018(diagnose og behandling)
- Lilleker JB, 2017 (kliniske manifestasjoner)
- Malik A, 2016 (diagnose og behandling)
- Betterige Z, 2015 (myositt-spesifikke antistoff)
Teksten er basert på aktuell faglitteratur. Den er skrevet og gjennomgått av forfatterne. I bearbeidelsen har vi brukt kunstig intelligens i noen avsnitt.