ANDRE SYKDOMMER (REV 063-REV 077)
169 Infeksjoner; erysipelas, gastroenteritt, hepatitt, multiresistente mikrober, nekrotiserende fasciitt, opportunistiske infeksjoner, pneumoni, sepsis, sårinfeksjoner, urinveisinfeksjoner, zoster-infeksjon, pneumoni, erysipelas, nekrotiserende fasciitt, hepatitt, opportunistiske (REV 169, REV 170, REV 171, REV 172, REV 173, REV 174, RE 175, REV 176, REV 177, REV 178, REV 179, REV 180, REV 181, REV 182, REV 183, REV 184, REV 185)
Øyvind Palm
ICD-10 koder: vennligst se under diagnosene nedenfor
Prosedyrekoder: Leddpunksjon: TN_10. UL veiledet leddpunksjon: NXA10K. Mikroskopi av leddvæske: NXFT05. Utredning av kroniske sår: QXFX30. Intravenøs infusjon: WBGM00
En grundig forståelse av infeksjonssykdommer er avgjørende for revmatologer for å kunne tilby optimal behandling og omsorg til pasientene våre. Det er avgjørende for revmatologer å ha en grundig forståelse av infeksjonssykdommer av flere grunner:
-
Inflammatoriske revmatiske sykdommer og behandlingen av disse kan øke risikoen for infeksjoner: Pasienter med revmatiske sykdommer, spesielt de som behandles med immunsuppressive medisiner (csDMARDs, tsDMARDs, bDMARDs og kortikosteroider) som gir en sekundær immunsvikt og økt risiko for å utvikle infeksjoner (Fragoulis G, 2022).
-
Infeksjoner kan etterligne revmatiske sykdommer: Enkelte infeksjoner kan presentere seg med symptomer som ligner på revmatiske sykdommer, noe som kan føre til feildiagnostisering. Eksempler er borreliose (artritt), parvovirus B19 (artralgi og artritt), HIV (artralgi, artritt), hepatitt B og C (artralgi og artritt, Sjøgrens syndrom) og endokarditt (vaskulitt i små kar).
-
Infeksjoner kan utløse eller forverre revmatiske sykdommer: Enkelte infeksjoner, som for eksempel parvovirus B19 eller Epstein-Barr-virus, kan utløse eller forverre revmatiske sykdommer (for eksempel juvenil SLE) hos predisponerte individer (Mahroum M, 2024).
Definisjon
Infeksjonssykdommer forårsakes av bakterier, virus, sopp eller parasitter. Til langt utpå 1900-tallet var epidemier og infeksjonssykdommer de dominerende folkesykdommene i Norge. Mange døde av barnesykdommer, tuberkulose, influensa og andre infeksjoner. Årsaker til at infeksjoner har blitt et mindre folkehelseproblem er høyere levestandard med innføring av moderne kloakksystemer, trygg drikkevannsforsyning, bedre ernæring, bedre boliger og mindre trangboddhet, godt smittevern, vaksiner, antibiotika og andre antimikrobielle midler. Likevel rammer infeksjonssykdommer et stort antall mennesker i Norge hvert år, men de er sjelden livstruende. De gir først og fremst akutt sykdom med lite helsetap over tid. Det er beregnet at infeksjonssykdommene utgjorde 0,7 % av det totale helsetapet og 6 % av dødsfallene i Norge i 2013. Den store majoriteten av infeksjonsdødsfallene er forårsaket av nedre luftveisinfeksjoner og skjer hos personer over 70 år (Folkehelseinstituttet, 2019). Man kan skille vanlige infeksjoner fra opportunistiske infeksjoner.
Opportunistiske infeksjoner skiller seg fra vanligere infeksjoner ved at de er uvanlige, men lettere oppstår hos immunsupprimerte personer og da kan forløpe mer alvorlig sammenlignet med hos immunkompetente personer. Eksempler på opportunistiske infeksjoner er herpes zoster, cytomegalovirus (CMV), Epstein-Barr virus (EBV), nocardiosis, pneumocystis jirovecii pneumonia, histoplasmose, herpes simplex og tuberkulose (tbc). Opportunistiske infeksjoner er nærmere omtalt nedenfor i dette kapitlet og tuberkulose i et eget kapittel.
Skåringsverktøy
Skåringsverktøy tildeler poeng til forskjellige kliniske funn, som for eksempel symptomer, tegn, laboratorieverdier og risikofaktorer. Poengsummen brukes deretter til å kategorisere pasienten i en risikogruppe eller til å veilede behandlingsbeslutninger.
Fordeler med skåringsverktøy er forbedring av objektiviteten i beslutningstakingen, hjelp til å til å identifisere pasienter med høy risiko for komplikasjoner og bidra til å optimalisere bruken av antibiotika.
Ulemper med skåringsverktøy er at de ikke alltid nøyaktige og kan gi feil resultater, de kan være tidkrevende å bruke og kan være vanskelig å tolke. Det er derfor viktig å bruke skåringsverktøy i samråd med klinisk skjønn og annen relevant informasjon.
Eksempler på skåringsverktøy ved infeksjon:
- CURB-65-skår: brukes for å vurdere risikoen for død hos pasienter med sepsis.
- NEWS-skår: brukes for å vurdere risikoen for organdysfunksjon hos pasienter med sepsis.
- NEWS er nærmere omtalt i kapitlet om akuttmedisinske tilstander ved vaskulitt.
- SOFA-skår: brukes for å vurdere organdysfunksjon hos pasienter med sepsis.
- IDSA-retningslinjer: brukes for å veilede behandlingen av ulike infeksjonssykdommer.
Sepsis og septisk sjokk er omtalt i avsnittet om sepsis nedenfor i dette kapitlet.
Smittevern
Læringsmål REV 172. Revmatologen skal ha kunnskap om smitteverntiltak ved særlig smittsomme lungeinfeksjoner.
Pneumoni smitter via luftveissekret i form av dråpe- og kontaktsmitte. Smittevern er også avhengig av hvilke bakterier som foreligger og lokale prosedyrer.
Generelle smitteverntiltak omfatter: Hyppig vask av hendene grundig med varmt vann og såpe. Hoste eller nyse i albuen eller i et papirlommetørkle som en kaster umiddelbart etterpå. Holde avstand til personer som er syke. Holde seg hjemme fra jobb eller skole hvis en er syk. Vaksiner mot influensa og pneumokokker.
Spesifikke smitteverntiltak ved dråpesmitte er bruk munnbind når en er i kontakt med andre personer. Ved kontaktsmitte bør en vaske og desinfisere overflater som ofte berøres. Personer med smittsomme lungeinfeksjoner kan være smittsomme i ulik tid, avhengig av infeksjonen. Isolasjon kan være nødvendig for å forhindre spredning av smitte.
- Vennligst se også avsnittet om Pneumoni nedenfor i dette kapitelt.
Smittevern ved gastroenteritt; Vask hendene ofte og grundig med varmt vann og såpe. Desinfiser overflater som ofte berøres. Unngå unødvendig nærkontakt med personer som er syke.
Smittehåndtering: Personer med gastroenteritt bør isoleres fra andre personer. De bør bruke eget toalett og håndkle. Sengetøy og klær bør vaskes i varmt vann og desinfiseres. Overflater som ofte berøres bør desinfiseres regelmessig.
- Vennligst les også i avsnittet om gastroenteritt i dette kapitlet.
Pasienttiltak. Pasienter med Clostridium difficile enterokolitt bør isoleres i enerom med eget toalett. De bør bruke håndsprit før og etter kontakt med andre personer, bruke engangshansker ved kontakt med kroppsvæsker, plassere skitne klær i en lukket beholder og vaske hendene grundig med varmt vann og såpe etter toalettbesøk.
Helsepersonell bør bruke engangshansker og vernefrakk ved kontakt med pasienten eller pasientens omgivelser. De bør vaske hendene grundig med varmt vann og såpe etter kontakt med pasienten eller pasientens omgivelser og overflater som ofte berøres bør desinfiseres regelmessig.
Varighet av isolasjon: Isolasjon bør opprettholdes til diaréen har stoppet i minst 48 timer.
Generelle smitteverntiltak mot hepatitt omfatter hyppig vask av hendene ofte med varmt vann og såpe. En bør unngå å dele mat og drikke, personlige gjenstander som tannbørster, barberhøvler og håndklær med andre. En bør bruke kondom ved sex og ta vaksiner mot hepatitt A og B.
Spesifikke smitteverntiltak:
-Hepatitt A: En bør unngå å spise mat og drikke som kan være forurenset med avføring, vaske frukt og grønnsaker grundig før en spiser dem og koke skalldyr grundig.
-Hepatitt B: En bør unngå kontakt med blod og andre kroppsvæsker fra personer med hepatitt B. Vær forsiktig med piercing og tatoveringer. Gravide kvinner med hepatitt B bør få behandling for å forhindre smitte til barnet.
– Hepatitt C: En bør unngå kontakt med blod og andre kroppsvæsker fra personer med hepatitt C, være forsiktig med piercing og tatoveringer, ikke dele sprøyter eller annet utstyr for injeksjonsbruk.
– Hepatitt E: En bør unngå å spise mat og drikke som kan være forurenset med avføring, vaske frukt og grønnsaker grundig før en spiser dem. Kjøtt kokes grundig.
- Vennligst les om hepatitt i eget avsnitt nedenfor i dette kapitlet.
- Supplerende informasjon også via Smittevernveilederen fra Folkehelseinstituttet og lokale metodebøker.
Aktuelle Infeksjoner (alfabetisk)
Erysipelas
Læringsmål REV 178. Revmatologen skal selvstendig kunne vurdere utredning og behandling samt differensialdiagnoser ved erysipelas/cellulitt.
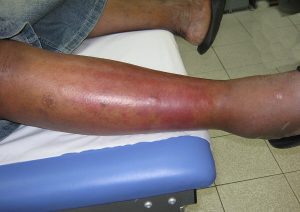
ICD-10: A46
Definisjon. Erysipelas er en hudinfeksjon, men kan involvere det overfladiske lymfesystemet. Erythemet er skarpt begrenset, elevert og oftest på underekstremiteter, nest vanligst i ansiktet. Diagnosen overlapper med cellulitt som klinisk har mindre skarpe grenser og en langsommere utvikling (Michael Y,2023).
Vanligste årsak er en huddefekt eller faryngitt som inngangsport for bakterier i form av streptokokker, hvorav gruppe A er vanligst ved ansikt-infeksjon (Rath E, 2017) og non-gruppe A på underekstremiteter. Risikofaktorer er lymfeødem, immunsuppresjon og nylig kirurgi.
Symptomer som utmattelse, feber og frysninger kan debutere 48 timer før hudlesjonen. Symptomene lokalt er brennende smerte og kløe og vesikler, og nekrose i alvorlige tilfeller.
Utredning omfatter laboratorieprøver der CRP og leukocytter (neutrofile) forventes å være forhøyet. Blodkulturer har vanligvis liten verdi, men er aktuelt hos klinisk dårlige pasienter, stoffmisbrukere, ved proteser, kunstige hjerteklaffer eller graft. Også septiske pasienter må utredes omfattende.
Differensialdiagnostisk vurderes andre årsaker til erythem, økt varme og smerte. Disse omfatter septisk bursitt, nekrotiserende fasciitt, orbital cellulitt, dyp venetrombose, abscess og urinsyregikt.
Behandlingen er med antibiotika, hvorav penicillin som monoterapi er førstevalg. Ved MRSA må en supplere med spesielle tiltak.
Prognosen under behandling er god. Ubehandlet kan livstruende systemiske komplikasjoner oppstå, slik som pneumoni og meningitt (Michael Y,2023).
ESBL (Methicillin-resistant Staphylococcus aureus) er beskrevet under avsnittet om Multiresistente mikrober i dette kapitlet.
Gastroenteritt
Læringsmål REV 175. Revmatologen skal ha god kunnskap om utredning, og selvstendig kunne behandle og iverksette smitteverntiltak ved akutt gastroenteritt.
Læringsmål REV 176. Revmatologen skal ha kunnskap om utredning, isolasjonsrutiner og behandling av Clostridium difficile enterokolitt. Ha kunnskap om symptomer og tegn på komplikasjoner.
Læringsmål REV 180. Revmatologen skal ha kunnskap om de hyppigste årsaker til feber, importdiaré og andre infeksjoner hos hjemvendte reisende, samt ha kunnskap om adekvate tiltak for videre utredning.
ICD-10: A08.4 (virus); A08.9 (bakterier)
Definisjon. Gastroenteritt er en infeksjon i ventrikkel og tarm. Økt motilitet i tarmen medfører hyppige tømninger og diare med eller uten oppkast, feber og abdominale smerter. Økt tømningsfrekvens foreligger ved tre eller flere vandige eller løse avføringer i døgnet eller minst 200 g avføring daglig. Basert på varigheten klassifiseres tilstanden som akutt ved varighet i 14 dager eller mindre, persistent over 14 dager, men mindre enn 30 dager, kronisk mer enn 30 dager og residiverende dersom diare begynner igjen etter 7 dagers symptomfrihet. Gastroenteritt kan forårsakes av ulike agens, vanligst er virus, deretter bakterier, sjeldnere parasitter eller sopp. Reaktiv artritt kan hos disponerte personer ofte relateres til forutgående gastroenteritt.
Symptomer er løs, vandig avføring, abdominale smerter, oppkast, hodepine, muskel– og leddsmerter og påvirket allmenntilstand med feber, frysninger, svette og nedsatt appetitt.
Undersøkelser omfatter anamnese for føde og væskeinntak, utenlandsreiser, varighet av symptomer, avføringsfrekvens og konsistens. Klinisk gjøres en generell status for å utelukke alarmerende funn. I blodprøver er CRP, Hb, hematokritt, leukocytter med differensialtelling trombocytter, lever-, nyre-, og thyreoidea funksjonsprøver, albumin, LD og elektrolytter aktuelt. Blodkulturer gjøres ved høy feber og alvorlig påvirket allmenntilstand. Avføringsprøver for bakterier kan være indisert ved dårlig eller langvarig tilstand, gravide, immunsupprimerte, alder over 70 år, komorbiditet og ved sykehusinnleggelse.
Smitte skjer fekal-oralt og via kontaminert føde, drikke og vann. God hygiene er forebyggende tiltak.
Behandlingen er først og fremst rehydrering gjennom drikke. Dersom dette ikke er tilstrekkelig kan intravenøst væske og elektrolyttinntak være nødvendig.
Viral gastroenteritt kjennetegnes ved brå debut kort tid etter smitte, men avhengig av det spesifikke viruset. Ved norovirus er inkubasjonstiden 12-48 timer, ved adenovirus opp til 3-10 dager. Norovirus er vanligst og svært smittsomt. Det er også mer resistent til mot desinfeksjon med klor og etanol enn andre virus. Sykdommen er imidlertid selvbegrensende, slik at de fleste friskner til i løpet av 72 timer uten senskader. Rotavirus er svært vanlig i befolkningen. Barn blir vaksinerte i henhold til vaksinasjonsprogrammet fordi småbarn (og nyfødte) er utsatte og lett utvikler komplikasjoner dehydrering. Blant voksne forløper rotavirus-infeksjon ofte asymptomatisk. Risiko for å smitte andre varer ca. 10 dager. Immunsupprimerte pasienter med rotavirus-infeksjon kan imidlertid ha lengre symptomvarighet og mer langvarig virusutskillelse (smitte) (Stuemfig ND , 2021).
Bakteriell gastroenteritt forårsakes av salmonella (vanligst), campylobakter, Clostridium difficile, shigella, shiga-toksinproduserende e.coli og sjeldnere vibro, yersinia eller listeria- bakterier. Bakteriell gastroenteritt forløper ofte mer alvorlig enn viral sykdom, slik at symptomer over mer enn tre dager er vanlig. Sykdomsforløpet kan da medføre alvorlige komplikasjoner. En bør spesielt være oppmerksom (“røde flagg) ved klinisk utvikling av tørre slimhinner, redusert turgor i huden, påvirket mental status, tachykardi, hypotensjon og ortostase, blodige avføringer, nylig sykehusopphold eller antibiotikabehandling, alder over 65 år og komorbiditet som diabetes, HIV eller sykdom behandlet med immunsuppressive medikamenter. Utredningen kan omfatte dyrkning av avføring for salmonella, campylobacter, shigella er aktuelt, listeria, clostridium, vibro og yersinia ved svangerskap, spesiell mistanke eller disposisjon. Ved blodig diare testes også for shiga-toksin og leukocytter i avføringen med tanke på EHEC (Enterohaemorrhagisk e. coli ). Vedvarende symptomer kan indikere behov for parasitt-undersøkelser. Behandling er vanligvis uten antibiotika, men i spesielle tilfeller gis azitromycin eller fluoroquinoloner empirisk som ved alvorlig sykdom med flere enn 6 avføringer daglig, feber eller behov for sykehusinnleggelse. Tetracycliner har størst effekt mot vibrio, mens ved clostridium stanses utløsende antibiotika. Gravide med listeria kan behandles med ampicillin (Sattar SBA, 2021).
Clostridium difficile enterokolitt
Læringsmål REV 176. Revmatologen skal ha kunnskap om utredning, isolasjonsrutiner og behandling av Clostridium difficile enterokolitt. Ha kunnskap om symptomer og tegn på komplikasjoner.
Clostridium difficile enterokolitt er en tarminfeksjon forårsaket av bakterien Clostridium difficile (C. diff) som er en spore-dannende bakterie som kan finnes i tarmen hos friske mennesker, men den kan forårsake infeksjon hos personer som har tatt antibiotika.
-Symptomer: Diaré, feber, abdominale smerter, blod og slim i avføringen, kvalme og oppkast, dehydrering. Utredning:
-Diagnose: Avføringsprøve for å påvise C. diff-toksin. Blodprøve for å utelukke andre årsaker til symptomene
-Behandling: Avbryte antibiotikabruk (hvis mulig), behandling med metronidazol eller vankomycin. Probiotika for å gjenopprette tarmfloraen.
Importdiaré
Læringsmål REV 180. Revmatologen skal ha kunnskap om de hyppigste årsaker til feber, importdiaré og andre infeksjoner hos hjemvendte reisende, samt ha kunnskap om adekvate tiltak for videre utredning.
Importdiaré er diaré som oppstår hos personer som har reist utenlands. Den er vanligvis forårsaket av inntak av forurenset mat eller drikke. Importdiaré kan være mild eller alvorlig, og kan i verste fall være livstruende.
Utredning: Reiseanamnese: Pasientens reisehistorie, inkludert hvor pasienten har reist, hva slags mat og drikke pasienten har spist og drukket, og om pasienten har hatt kontakt med andre syke personer er av interesse. Klinisk undersøkelse for å se etter tegn på dehydrering, feber og andre symptomer er aktuelt. Laboratorieundersøkelser: Avføringsprøve og blodprøve kan tas for å identifisere årsaken til diaréen.
Eksempler på importdiaré: Turistdiaré: Den vanligste typen importdiaré, ofte forårsaket av bakterier som Escherichia coli (E. coli) eller Salmonella. Giardiasis: Forårsakes av parasitten Giardia lamblia. Amebiasis: Forårsakes av parasitten Entamoeba histolytica. Tyfus er forårsakes av bakterien Salmonella typhi.
Andre importsykdommer omfatter malaria, Denguefeber, Zikavirus, hepatitt A og hepatitt E.
Behandling av importdiaré avhenger av årsaken. Mild diaré kan vanligvis behandles med rehydrering og hvile. Alvorlig diaré kan kreve sykehusinnleggelse. Antibiotika kan være nødvendig for å behandle bakteriell diaré. Parasittiske infeksjoner kan behandles med antiparasittiske legemidler.
Smittehåndtering ved gastroenteritt er viktig og nærmere omtalt under Smittevern ovenfor i dette kapitlet. For nærmere informasjon vises til Smitteveilederen, Folkehelseinstituttet og lokale metodebøker. For smittevern og håndtering etter utenlandsreiser vises til Folkehelseinstituttets veileder, 2019.
Hepatitt (viral)
Læringsmål REV 177. Revmatologen skal ha kunnskap om utredning, smitteverntiltak og behandling av virale hepatitter.
ICD-10: B15.9 (hepatitt A); B18.1 (hepatitt B, kronisk), B18.2 (hepatitt C, kronisk); B18.8 (kronisk virus hepatitt, annen)
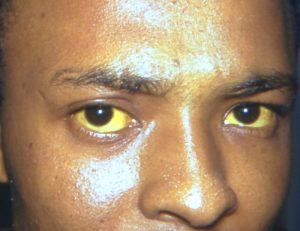
Definisjon: Virus hepatitt er inflammasjon i lever utløst av virus. Sykdommen kan forløpe akutt eller kronisk. Sykdommene har varierende symptomer og ulik prognose avhengig av det utløsende virus. Hepatitt B er et DNA, virus, alle andre virushepatitt forårsakes av RNA virus. Hepatitt A og E overføres fekal-oralt, mens Hepatitt B, C, og D smittes via blod. For nærmere informasjon om smitteverntiltak vises til Smitteveilederen, Folkehelseinstituttet og lokale metodebøker. Autoimmun hepatitt er omtalt i kapitlet om infeksjoner.
Hepatitt A
Hepatitt A-virus forårsaker akutt hepatitt, vanligvis via oral-fekal smittevei fra kontaminert mat, vann eller tett fysisk kontakt mellom mennesker. Forekomsten i den vestlige verden er lav. Utsatt er intravenøs stoffmisbrukere, menn som har sex med menn, personer som reiser i endemiske områder eller lever tett i kohorter. Hepatitt A virus forårsaker ikke kronisk sykdom i motsetning til hepatitt B og C og forløpet er vanligvis selvbegrensende og fulminant hepatitt er sjelden.
Symptomene på akutt infeksjon omfatter kvalme, oppkast, abdominal smerte, utmattelse, redusert appetitt og feber.
Inkubasjonstiden er vanligvis ca. 4 uker.
Klinisk kan ikterus observeres.
Diagnosen baseres på hepatitt spesifikke antistoff (HAV IgM) i blodet. I tillegg kan PCR test for viral RNA. IgG antistoff oppstår raskt etter infeksjon og vedvarer livet ut. Øvrige blodprøver viser forhøyede leverenzymer (ALAT), økt bilirubin og mild lymfocytose. Enzymene og bilirubin normaliseres innen 4-6 måneder. Protrombin er vanligvis normal. Forhøyet protrombin gir mistanke om alvorlig leversykdom og risiko for encefalopati.
Bildediagnostikk inklusiv ultralyd er ikke rutine.
Differensialdiagnoser omfatter alkohol-hepatitt, annen viral hepatitt (B, C, E), autoimmun hepatitt
Behandlingen er symptomatisk. vaksinasjon anbefales for barn over 12 måneder eller voksne med økt risiko for infeksjon eller kronisk leversykdom.
Smittevern innebærer at pasientene skal isoleres hjemme og i kontakt med et begrenset antall personer.
Litteratur: Ioro N, 2021; Folkehelseinstiuttet, 2019
Hepatitt B
Definisjon. Hepatitt B er en kronisk virusinfeksjon (hepatitt-B virus: HBV) i lever. Overføres via blod, spermier eller vaginal væske. Hepatitt B er viktig å vurdere før en begynner behandling med immundempende medikamenter mot revmatisk sykdom. Kronisk Hepatitt B infeksjon foreligger når virus (HBsAg) blir påvist i kroppen over 6 måneder eller lenger. Sykdommen forekommer hyppigst i Asia og Afrika. Ca. 1/3 av verdens befolkning er smittet med Hepatitt B. Etter sprøytestikk med infisert blod får 10-30% sykdommen overført. En latent (sovende) Hepatitt B infeksjon kan blusse opp dersom revmatisk sykdom blir behandlet med legemidler som medfører betydelig redusert immunsystem, for eksempel biologiske medikamenter (De Nard F, 2015).
Symptomer. Omtrent 30% er asymptomatiske. Akutt sykdom: Influensalignende symptomer med tretthet, leverbetennelse (forhøyede leverenzymer i blodprøver hos 30%), kvalme og oppkast. De fleste (90%) blir friske i løpet av 4 måneder. Kronisk sykdom: Blant 3 – 5% av de smittede blir sykdommen kronisk. Gradvis utvikler ca. 15% leverskade (leverfibrose, cirrhose). Etter mange år blir hepatocellulær cancer diagnostisert i noen tilfeller. Kronisk hepatitt B infeksjon er årsaken til ca. 50% av leverkreft tilfellene. Hepatitt B er i noen tilfeller relatert til vaskulitt-sykdommen polyarteritis nodosa. Kryoglobuliner forekommer og kan utløse kryoglobulinemi syndromet. Leddsmerter er vanlig.
Inkubasjonstiden er vanligvis 60 – 90 dager.
Laboratorieprøver. Celletellinger, leverenzymer, hepatitt B-antistoff (HBsAs, HBc), hepatitt Bs antigen (HBsAg). Ved positive funn sjekkes også hepatitt-C antistoff og HIV.
-Antistoff mot hepatitt B. HBsAs (antistoff mot hepatitt B) er en markør for gjennomgått sykdom eller vaksinasjon. Vaksinerte personer: HBsAg (antigen) og HBc er normale/negative. Anti HBc antistoff (mot “core”) forekommer i hele sykdomsforløpet. Anti HBc antistoff indikerer at personen har vært i kontakt med hepatitt B viruset en eller annen gang. Infeksjonen kan være overstått. Anti HBc antistoff bør ikke forveksles med HBc-antigen som befinner seg intracellulært (inne i cellene) og forekommer ikke i blodserum). HBsAg (antigen) kan påvises i blodet når infeksjonen er aktiv og krever behandling. Anti-HBe-antigen i blodet blir assosiert med sykdomsaktivitet og smittsomhet. Ved «negative (eller ingen) antistoffer» i blodet kan likevel latent virusinfeksjon persistere i leverceller. Ved immunsuppresjon (med legemidler) kan Hepatitt B bli reaktivert og sykdom oppstå. Hvis mistanke om tidligere infeksjon, kan HBV-DNA testes ved PCR teknikk før eventuell antirevmatisk behandling med rituksimab eller andre biologisk legemidler eller DMARDs.
Tolkning av antistofftester ved Hepatitt B
- Aldri smittet: HBsAg – / HBsAs – / HBc –
- Vaksinert: HBsAg – / HBsAs + / HBc –
- Tidligere gjennomgått infeksjon med liten sykdomsrisiko: HBsAg – / HBsAs + / HBc + (følg opp ALAT og HBV-DNA)
- Tidligere gjennomgått infeksjon med moderat sykdomsrisiko: HBsAg – /HBsAs – / HBc + (mål HBV-DNA)
- Kronisk infeksjon: HBsAg +/ HBsAs – / HBc + (Behandlingsindikasjon)
| HBsAg | anti-HBCore (HBc) | Anti-HBSurface (HBsAs) | HBV-DNA | ALAT | Betydning |
| + | + | – | + | ↑ | Akuttfase |
| + | + | – | ↑ | Kronisk infeksjon | |
| – | + | + | Restitusjonsfase | ||
| – | – | + | Vaksinert | ||
| – | – | – | – | Ikke infisert |
Nesten alle infeksjoner med Hepatitt B forblir latente (virus forblir i cellene). Ved biologisk behandling vil 20-50% få reaktivering, særlig etter rituksimab. Sjekk alle aktuelle blodprøver for hepatitt B før behandling begynner.
Behandling. PEGylert interferon og andre antivirale midler, men mange er non-respondere. Forebyggende er vaksine anbefalt dersom risiko for eksponering forventes.
Gode råd ved påvist hepatitt B smitte:
- Lag en behandlingsplan i samråd med infeksjonslege.
- Henvis alle anti-HBcore+ pasienter som skal starte med rituksimab til infeksjonsmedisiner for vurdering på antiviral behandling.
- Antiviral behandling bør ideelt sett begynne før eller i det minste samtidig med den immunsuppressive medikasjonen.
Litteratur: Easterbrook PJ, 2017 (diagnose av hepatitt); Tripathi N, 2021; Folkehelseinstituttet 2023.
Hepatitt C
Hepatitt C er forårsaket av hepatitt C-virus (HCV). Infeksjonen blir kronisk ( mer enn 6 måneders varighet) hos 70-80% av de infiserte (Folkehelseinstituttet, 2017). Diagnosen kan være viktig å vurdere dersom behandling med legemidler som medfører immunsuppresjon planlegges, selv om det er uvanlig at HCV reaktiveres ved immundempendeantirevmatisk behandling. Hepatitt C infeksjon kan også medføre revmatiske symptomer (vennligst se nedenfor).
Smitte via blodtransfusjoner, urene (kontaminerte) sprøyter (sprøyte-narkomane). I Norge er mellom 20.000 og 30.000 personer er smittet med Hepatitt C. Spesielt høy forekomst i Egypt, Alaska og Italia.
Symptomer. Blant nysmittede får 15-30% symptomer i form av utmattelse, kvalme, magesmerter, diare, feber og ikterus (gulsott) hos 10%. Kronisk infiserte kan plages med utmattelse og kognitive symptomer som redusert konsentrasjon og hukommelse. Etter år (20 år: 20%) utvikles levercirrhose og risk for hepatocellulær cancer. Revmatiske symptomer omfatter redusert funksjon i spytt- og tårekjertler kan medføre tørr munn og tørre øyne, noe som kan minne om Sjøgrens syndrom. Artritt er sjelden, men kan forekomme i to ulike former (Palazzi C, 2014): Små ledd angripes i begge hender og føtter, ligner på revmatoid artritt. Store ledd angripes, særlig knær og hofter. Kryoglobulinemi og symptomer på kryoglobulinemi syndrom.
Utredning. Anamnese for stoff- eller alkoholmisbruk og inntak av blodprodukter. Klinisk tegn til leversykdom. Hepatitt C antistoff i blodprøve, HCV RNA påvises ved PCR og genotyping. Hepatitt Bs antistoff, Hepatitt B Core antistoff og Hepatitt BsAg. HIV infeksjon. Alpha-phoetoprotein i blodprøve. Det er ikke uvanlig at Hepatitt C medfører produksjon av flere typer antistoff, uten at revmatisk sykdom foreligger. Andre: hepatitt B antistoff, INR, prothrombin tid, celletellinger, lever- nyre. og thyreoidea funksjonsprøver.
Bildediagnostikk. Ultralydundersøkelser av lever og milt.
Biopsi. Indikasjon ved mistanke om malignitet.
Behandling. Konferer med infeksjonsmedisiner. Ingen vaksine eller immunglobuliner. Tidligere var PEGylert Interferon i kombinasjon med Ribavirin (mer enn 50% blir varig virusfrie) førstevalg, men interferon gir ofte betydelige bivirkninger. Nyere kostnadseffektive (men dyre) behandlingsregimer uten interferon er aktuelle. Tolv ukers tablett-behandling er effektiv hos over 90%. Sjekk Hepatitt C-RNA 6 måneder etter avsluttet behandling (negativ = helbredet).
Litteratur: Easterbrook PJ, 2017 (diagnosis of hepatitis); Basit H, 2021; Det norske Folkehelseinstituttet
Hepatitt D
Hepatitt D-virus (HDV) er et inkomplett RNA-virus som ble første gang rapport 1977 hos en hepatitt B-smittet person med alvorlig leversykdom. Viruset ble identifisert i 1986 og fikk da navnet deltavirus. Membranen består hovedsakelig av HBsAg, og viruset forekommer derfor kun hos HBV-infiserte. Smitteoverføring skjer sammen med hepatitt B-viruset (koinfeksjon) eller til personer som allerede er kroniske bærere av hepatitt B-viruset (superinfeksjon) (Folkehelseinstituttet, 2019; Masood U, 2021).
Hepatitt E
Hepatitt E forårsakes av hepatitt E-viruset (HEV) og smitter hovedsakelig gjennom drikkevann og næringsmidler. Sykdommen er endemisk i Asia og Afrika, men sjelden i vår del av verden. Vanligvis er sykdomsbildet mildt, men tilfeller med alvorlig myositt er sett (Mengel AE, 2015). Også nevrogene smerter kan være en del av sykdomsbildet (Abravanel F, 2018). Inkubasjonstid er vanligvis 4-6 uker (Folkehelseinstituttet, 2019; Waquar S, 2021).
Infeksjoner ved immunsvikt
Læringsmål REV 183. Revmatologen skal ha kunnskap om og under supervisjon fra spesialist kunne iverksette adekvat antimikrobiell og støttebehandling hos pasienter med ervervet immunsvikt på grunn av: HIV, kreftsykdom, nyresvikt, bruk av immunmodulerende legemidler som cytostatika og biologiske legemidler.
Lungetuberkulose
Læringsmål REV 171. Revmatologen skal selvstendig kunne gjenkjenne kliniske symptomer og tegn som kan indikere lungetuberkulose. Ha god kunnskap om videre utredning og isolasjonsrutiner.
Meningokokk-infeksjon
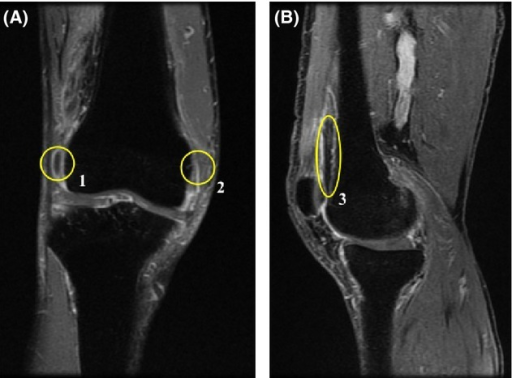
Forekomst: Artritt ses hos omkring 12 % av pasienter med meningokokk meningitt.
Symptomer og inndeling og behandling:
Type I: Artritt assosiert med meningitt eller annen lokalisert meningokokksykdom: Akutt mono- eller polyartritt (store effusjoner). 3-7 dager etter meningitt. Oftest negativ dyrkning fra leddvæske, men positiv fra cerebrospinalvæske. Heler som regel uten sekvele. Artritten behandles symptomatisk.
Type II: Septisk artritt. Leddsykdom assosiert med kronisk meningokokkemi. Som oftest artralgi, sjelden artritt. Positiv blodkultur. Responderer på antibiotika.
Type III: Primær meningokokk artritt: Akutt monartritt. Ingen andre symptomer eller funn av meningokokksykdom. Oppvekst i leddvæske (ofte purulent). Responderer på antibiotika og drenasje.0*****************************
MRSA (Methicillin-resistant Staphylococcus aureus): Vennligst se Multiresistente mikrober nedenfor
Multiresistente mikrober
Læringsmål REV 181. Revmatologen skal ha god kunnskap om de til enhver tid gjeldende anbefalinger når det gjelder importsmitte av resistente mikrober herunder MRSA, VRE og ESBL. Ha god kunnskap om adekvate videre undersøkelser, prøvetaking og isolasjonsrutiner.
Definisjonen på multiresistente bakterier varier. Meticillin-resistente gule stafylokokker (MRSA), vancomycin resistente enterokokker (VRE), multiresistente tuberkel-bakterier (MDRTB) og gramnegative stav-bakterier som danner bredspektred betalaktamaser (ESBL/MBL) er de vanligste. Infeksjoner med disse bakteriene kan ikke behandles med vanlig antibiotika. Problemet da er at infeksjonene kan bre seg hos den enkelte og dessuten utgjøre et betydelig smitteproblem. Personer med svekket immunsystem er spesielt utsatt. Det angår blant andre personer med immundempende revmatiske medikamenter mot revmatisk sykdom
Forekomst. ESBL («Extended Spectrum Beta-Lactamase») er funnet hos Klebsiella-arter, e.coli-bakterier, gramnegative tarmbakterier som kan produsere ESBL, ulike salmonellaarter, proteus mirabilis, andre Enterobacteriaceae og pseudomonas aeruginosa. Bakterier som produserer ESBL har en betydelig høyere forekomst i noen land, særlig i Sør-Europa (Italia, Hellas), Afrika og Asia.
Smitte. Bakteriene smittes fra person til person, vanligvis via hender (kontaktsmitte) eller gjennom dårlig rengjort utstyr og felles kontaktpunkter. For smittehåndtering av ESBL vises til Folkehelseinstituttets Smitteveileder, 2019.
Importsmitte og håndtering etter utenlandsreiser. Det vises til Folkehelseinstituttets veileder, 2019.
Symptomer. Friske personer (helsepersonell) er oftest uten sykdomstegn (asymptomatiske), mens ved nedsatt immunforsvar, som ved immunsupprimerende anti-revmatisk behandling eller alvorlig annen sykdom, kan infeksjoner utvikle seg.
Diagnose. En tar bakterieprøver fra sår eller overflater der bakterier mistenkes. Mikrobiologisk laboratorium gjennomfører resistensbestemmelse påviser bakteriene ved dyrkning eller gen-tekniske metoder (PCR).
Behandling. Forebygging er svært viktig. God håndhygiene og bruk av alkoholbaserte desinfeksjonsmidler er nødvendig. Rens sår med desinfiserende middel. Mat kokes, frukt skrelles. Infeksjoner må behandles ut fra resultatene av resistensundersøkelsene. Folkehelseinstituttet (i Norge) anbefaler følgende (pr 2016): Før eller ved innleggelse i sykehus anbefales det å ta prøve for ESBL-holdige bakterier av alle som har vært innlagt i helseinstitusjon utenfor Norden det siste året, det siste året har vært innlagt i helseinstitusjon i Norge eller annet nordisk land der det (under det aktuelle oppholdet) var et utbrudd med ESBL-holdige bakterier, har bodd sammen med person som har fått påvist ESBL-holdige bakterier det siste året, tidligere har fått påvist ESBL-holdige bakterier eller ved alle sykehusinnleggelser i avdelinger som etter lokal vurdering karakteriseres som avdelinger med særlig mottakelige pasienter og/eller stor risiko for spredning (brannskade-avdeling, intensivavdeling, hematologisk avdeling, nyfødtintensiv og lignende). Antibiotika: Det finnes i dag bare få grupper av betalaktam-antibiotika (gruppen karbapenemer og kombinasjonspreparat med betalaktam og betalaktamase inhibitor for eksempel piperacillin-tazobactam) som ESBL-produserende bakterier er følsom for.
Tiltak ved enkelttilfelle eller utbrudd. Infiserte bør isoleres mot kontaktsmitte på enkeltrom med eget toalett. Det anbefales ingen spesielle tiltak eller restriksjoner for helsepersonell som er bærere av ESBL-resistens. Ved utbrudd i en helseinstitusjon bør det settes ned en lokal arbeidsgruppe som etterforsker utbruddet og vurderer smitteverntiltak. Disse tiltakene kan omfatte: opplæring av personale, pasienter og pårørende, smitteoppsporing, isolering av kontakter og screening av utvalgte pasientgrupper (men ikke av personale).
Krav til å melde infeksjon. Smittebærere og infeksjoner med mikrober med spesielle resistensmønstre er meldingspliktig sykdom gruppe A til MSIS. Kriterier for melding er påvisning av enterobakterier med redusert følsomhet for meropenem og påvist ESBLKARBA gener, Pseudomonas aeruginosa med redusert følsomhet for meropenem og påvist ESBLKARBA gener. Acinetobacter spp. med redusert følsomhet for meropenem og påvist ESBLKARBA gener, Enterobacteriaceae, P. aeruginosa, Acinetobacter spp. isolater med nedsatt følsomhet for meropenem kombinert med andre fenotypiske funn forenlig med karbapenemase-produksjon, men som er negativ for kjente ESBLKARBA gener, skal undersøkes biokjemisk for karbapenemase-produksjon. Funnet skal meldes til MSIS (Norge) hvis karbapenemase-produksjon verifiseres i en validert biokjemisk assay. Varsling til kommuneoverlege, Folkehelseinstituttet og andre instanser ved utbrudd eller ved overføring av smittet pasient mellom helseinstitusjoner
Litteratur: Pana ZD, 2018; Folkehelseinstituttet i Norge
- Vedrørende importsmitte, isolasjonsrutiner og hygienetiltak vises til avsnittet om Smittevern i begynnelsen av dette kapitlet.
Nekrotiserende fasciitt
Læringsmål REV 179. Revmatologen skal selvstendig kunne gjenkjenne kliniske tegn ved nekrotiserende fasciitt, og selvstendig kunne iverksette nødvendige behandlingstiltak.
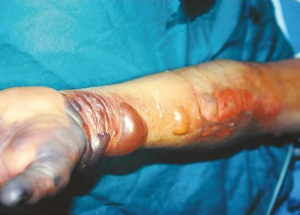
ICD-10: M72.6
Definisjon. Nekrotiserende fasciitt er en aggressiv, bakteriell infeksjon i hud og bløtvev og som forårsaker nekrose av muskelfascier og subkutant vev. Infeksjonen sprer seg typisk langs fasciene som har en lav blodforsyning. Den overliggende huden blir da relativt sent angrepet slik at diagnosen og kirurgisk behandling kan bli forsinket (Gundersen IM, 2024; Bonne S, 2017).
Sykdomsårsaken er gassproduserende bakterier som kommer inn via huddefekter etter kirurgiske inngrep, venefloner og lignende. Gram-positive kokker og da særlig Staphylococcus aureus og Streptococcus pyogenes (gruppe A streptokokker) er de vanligste mikrobene. Pasienter med redusert immun-status som ved diabetes, alkoholisme med levercirrhose eller immundempende medikasjon er mest utsatt.
Symptomene er intens smerte lokalt og tegn på systemisk infeksjon. Rask hevelse, erythem, blålig-sort misfarging under huden og blemmer, samt feber.
Klinisk ses ømhet og smerte ved palpasjon under en erythematøs rand. Forekomst av bullae, ekkymoser og parestesier ved nerveskade kan ses. Typisk er subkutant emfysem, krepitasjoner og raskt spredning av infeksjonen (i løpet av få timer).
Laboratorieprøver omfatter blodprøver med CRP der verdier over 150 mg/L indikerer mer alvorlig infeksjon, leukocytter med differensialtellinger, Hb, elektrolytter, kreatinin og glukose.
Bildediagnostikk kan være i form av ultralyd Doppler eller CT. Hastegrad gjør at MR er mindre anvendelig.
Behandling. Disse pasientene er svært syke og skal overføres til en intensivavdeling. Raske tiltak er avgjørende. En skal derfor ikke bruke for lang tid på utredningen dersom berettiget mistanke om nekrotiserende fasciitt foreligger, men det er nyttig å differensiere mellom nekrotiserende on non-nekrotiserende sykdom.
- Antibiotika. Tidlig empirisk, bredspektret intravenøs antibiotikabehandling initieres. Etter identifisering av utløsende mikrobe skiftes fra empirisk til målrettet antibiotisk behandling.
- Kirurgisk vurdering er essensielt fordi aggressivt kirurgisk inngrep for å drenere abscess og debridement av nekrotisk, infisert vev kan være essensielt.
- Væske. Tilførsel av væske og elektrolytter for å opprettholde blodsirkulasjon og organfunksjon.
- Oksygen: Tilførsel av oksygen for å forbedre vevsheling.
Prognosen er alvorlig med over 30% mortalitet. Dårlig prognostiske faktorer er enkelte streptokokk-varianter, høy alder, ukontrollert diabetes, i9mmunsuppresjon og forsinket kirurgisk behandling. En del pasienter får vedvarende betydelig nedsatt fysisk funksjon.
Litteratur: (Gundersen IM, 2024; Wallace HA, 2023).
Opportunistiske infeksjoner
Læringsmål REV 183. Revmatologen skal ha kunnskap om og under supervisjon fra spesialist kunne iverksette adekvat antimikrobiell og støttebehandling hos pasienter med ervervet immunsvikt på grunn av: HIV, kreftsykdom, nyresvikt, bruk av immunmodulerende legemidler som cytostatika og biologiske legemidler.
ICD-10: B48.5† Pneumocystose (J17.3*)
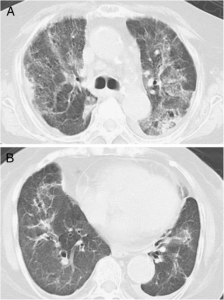
Disponerende faktorer: Anti-revmatisk behandling med immunsupprimerende legemidler som kortikosteroider (prednisolon >15-20mg/d eller tilsvarende), DMARDs, biologiske legemidler og JAK-hemmere. Diabetes mellitus (dårlig regulert) og alvorlig komorbiditet. Granulocytopeni ved aktiv systemisk lupus (SLE). Antall leukocytter i form av granulocytter er viktige i forsvaret mot infeksjoner (leukopeni). Spesielt vil antall CD4 T-celler under <200 /mikro-liter øker risikoen. HIV infeksjon når CD4 T-celle tall er lavt (<200). Immunsuppresjon ved andre autoimmune sykdommer, etter transplantasjoner eller ved kreftbehandling. Immunsvikt (CVID) eller andre årsaker til lave immunglobuliner (rituksimab-behandling, glomerulonefritt). Langvarig antibiotikabehandling som forstyrrer normalfloraen (mikrobiota)
Epidemiologi. Risikoen for opportunistisk infeksjon er ulik blant de bakenforliggende revmatiske sykdommene. Alder og komorbiditet er dessuten av betydning. Pneumocystis jiroveci, herpes zoster og tuberkulose medfører infeksjoner særlig ved myositt, inklusiv antisyntetase syndromet, samt ved SLE og ANCA-vaskulitt. Typisk relatert til remisjonsinduserende, immunosuppressive legemidler. Det likevel gjort lite forskning på forekomst og fordeling av opportunistiske infeksjoner blant pasienter med revmatiske sykdommer. En nasjonal kohorte-studie fra Taiwan viste imidlertid at risikoen var størst ved myositt, etterfulgt av SLE, systemisk sklerose, revmatoid artritt (RA) og primært Sjøgrens syndrom. De viste også at risikoen var størst det første året fra diagnose med gradvis avtakende deretter (Chung-Yuan Hsu, 2019).
Infeksjoner ved noen revmatiske sykdommer
SLE pasienter har klart økt risiko for opportunistiske infeksjoner. I har i utgangpunktet foreligger ofte redusert immunforsvar som omfatter immunologiske defekter i komplementsystemet, påvirket kjemotaksis og fagocytose. I tillegg øker infeksjonsrisikoen ved når bruk av kraftige immunosuppressive medikamenter og hospitalisering er nødvendig (Chung-Yuan Hsu , 2019).
Myositt. Det er flere årsaker til opportunistiske infeksjoner også ved myositt. Alvorlige sykdomsmanifestasjoner i lunger foreligger hos 40–65% med myositt, inklusiv antisyntetase syndromet (Fathi M, 2004), og pasienter med interstitiell lungesykdom er mer mottakelige for luftveisinfeksjoner med blant annet mykobakterier og aspergillus som er opportunistiske mikrober. I tillegg er behovet for immundempende medikasjon ofte stort, særlig det første året fra diagnose. Ytterligere infeksjonsrisiko foreligger ved myositt-relaterte svelgevansker og aspirasjon, eller når sykdommen er assosiert med malignitet, slik som dermatomyositt blant voksne.
Ved ANCA-vaskulitter og polyarteritis nodosa (PAN) foreligger en klart økt risiko for alvorlige infeksjoner, inklusiv opportunistiske. Nordamerikanske data viste klart økt dødelighet både ved MPA- og PR3 assosiert ANCA-vaskulitt med standard mortalitets ratio (SMR) på henholdsvis 16,4 og 6.5. (Wallace Zs, 2019). Hovedårsaker antas å være den immunosuppresiv induksjonsbehandling kombinert med at pasientene ofte er i høyre aldersgrupper med svekket immunsystem og komorbiditet.
Immundempende behandling
Eksempler på immundempende anti-revmatologisk behandling som øker risiko for opportunistiske og andre infeksjoner. Høye doser kortikosteroider (SoluMedrol, Prednisolon). Sammenlignet med lave prednisolon-doser (<7,5mg/d) steg risikoen 1,4 ganger ved doser 7,5-15mg og 2,24 ganger ved prednisolon >60mg/dag (korrigert Hazard ratio) (Yang S-C, 2018). Sendoxan (DMARD). Biologiske medikamenter. JAK-hemmere
Diagnostikk av opportunistiske infeksjoner
Anamnese omfatter tidligere infeksjoner, komorbiditet, medikasjon, reise-anamnese og andre risiko-situasjoner for smitte. Nattesvette, målt feber. Symptomer fra luftveier, mage-tarm, urinveier, hud, nervesystem, muskel-skjelett-system. Anamnesen skal dekke risikofaktorer for infeksjon.
Klinisk undersøkelse skal være generell indremedisinsk (lunger, hjerte, gastro-intestinalt, nervesystem, hud, øyne, ØNH) og revmatologisk. Den kliniske undersøkelsen omfatter puls, BT, pustefrekvens, oksygenmetning og perifer sirkulasjon (kapillærfylning normalt ≤2 sekunder).
Laboratorieprøver. Hb, hvite, nøytrofile, lymfocytter, trombocytter, CRP (prokalsitonin hvis tilgjengelig), kreatinin, leverenzymer, Na, K. Andre prøver (venøs syre-base status) på indikasjon. Antistoff kommer sent i forløpet (særlig hos immunsupprimerte). PCR, ELISA, direkte immunfluorescens gir raskt svar og rekvireres når mulig. Parasitter kan påvises ved biopsi fra sårkant (leishmaniasis), blod (Chagas sykdom), avføring (cryptosporoidose). Eosinofili i blodet kan forekomme. Ikke glem utredning ved mulig malaria og andre tropesykdommer. Urin-stiks, mikroskopi og dyrkning.
Blodkulturer Tas fra CVK. Bakteriologisk prøve av CVK innstikk hvis det ikke er helt tørt og fra alle andre mulige infeksjonsfoci.
Mikrobiologiske prøver: Prøvetakning til virusdiagnostikk er aktuelt ved luftveissymptomer og/eller sår. Bakteriologiske prøver fra nese, hals, urin og avføring bestilles på klinisk indikasjon. Sopp og mykobakterier ved dyrkning (spesialfarging), histologi, biopsi, eller PCR.
Bildediagnostikk: CT eller HRCT lunger
Munn og genitalier: Herpes (ulike typer) kan forårsake hyppige og uttalte sår i og rundt munnen, eller små, smertefulle blemmer. Soppinfeksjoner (candida)
Hud: Herpes zoster
Lunger: CT (HRCT) av lunger, Bronkoskopi med undersøkelse av BAL-væske (pneumocystis diagnostikk), atypiske mykobakterier kan angripe lungene, men også tarm, beinmarg, lever og milt, tuberkulose ved hoste og nattesvette må utelukkes. Soppinfeksjon.
CNS: MR med kontrast av hjernen: Encefalitt? Spinalvæskeundersøkelser. Herpes simpleks og zoster. Mykoser, systemiske. Toksoplasmose kan være årsak til feber, eksem, hoste, hodepine, kramper, forvirring, synsforstyrrelser og afasi.
Gastrointestinalt: CT abdomen (differensialdiagnose lymfom-feber). Rektalpensel (vancomycin resistente enterokokker, VRE). Avføring (clostridium). Cytomegalovirus (CMV) kan forårsake diaré og smerter i magen.
Urinveier: Dyrkning og PCR av urin.
Øyne: Cytomegalovirus kan angripe mange organer, men særlig øyne. Nedsatt syn, tap av sentralsynet eller i verste fall blindhet.
Noen opportunistisk infeksjoner
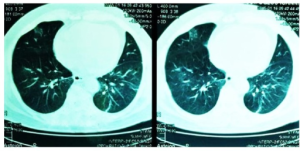
En studie fra USA (Baddley JW, 2014) bekreftet at pasienter behandlet med TNF-hemmere (biologiske legemidler) var mer utsatt for opportunistiske infeksjoner (% i listen nedenfor):
- Adenovirus. Adenovirus er vanligvis ufarlige, men forårsaker smerter i hals, røde øyne og feber spesielt hos barn. Revmatiske symptomer er ikke å forvente. Ved et svekket immunsystem, som ved immundempende behandling av revmatiske sykdommer, kan adenovirus imidlertid medføre komplikasjoner. Inkubasjonstid 5-10 dager (Lion T, 2014).
- Aspergillose (1,3%). Aspergillus-infeksjon (aspergillose) er en soppinfeksjon (mykose). Revmatiske symptomer er ikke å forvente. Ved et svekket immunsystem, som ved immundempende behandling, kan aspergillus imidlertid medføre komplikasjoner. Infeksjonen kan også forverre astma ved overfølsomhet. Luftveisinfeksjon med langvarig, antibiotika resistent feber og hoste. Nese, Bihuler, Øreganger (“Singapore ear”), Lunger. Aspergillom: kolonier i lunger og bihuler ( Borys M, 2017).
- BK-virus tilhører polyomavirus. Ligner JC-virus. Hele 80% friske personer har latent infeksjon i kroppen (eksisterende virus uten symptomer). Infeksjonen medfører ikke revmatiske symptomer, men ved et svekket immunsystem som under immundempende, anti-revmatisk behandling, etter organtransplantasjon eller ved HIV infeksjon, kan BK virus infeksjon bli alvorlig. Jo sterkere immunsuppresjon, desto mer alvorlig infeksjon (Saleh A, 2020; Gupta N, 2017).
- Blastomykose (1,3%): Lite aktuell i Europa. Ses i østlige deler av USA. Feber, artralgi, myalgi.
- Candidiasis. Systemisk soppinfeksjon (mykose). Candida albicans: utgjør ca. 2/3 av disse soppinfeksjonene i Norge. Revmatiske symptomer er ikke å forvente, og vanligvis er infeksjonen ufarlig. Ved et svekket immunsystem, som ved immundempende behandling av revmatiske sykdommer, kan candida imidlertid medføre komplikasjoner (Meena DS, 2022; Sigh S, 2015).
- Chikungunya er en myggoverført tropesykdom forårsaket av virus.
- Clostridium difficile medfører tarminfeksjon, paradoksalt nok som følge av antibiotika-behandling for andre infeksjoner. Samtidig er antibiotika også behandling av sykdommen. Langvarig behandling med bredspektrede antibiotika som klindamycin, cefalosporiner og ampicillin er mest disponerende. Ved et svekket immunsystem, som ved en de revmatiske sykdommer, kan clostridium-infeksjon forløpe alvorlig. Bruk av protonpumpehemmere (mot magesyre-refluks) kan også øke risikoen for clostridium infeksjon (Raknes G, 2020; Debast SB, 2014; van Beurde YH, 2017).
- Cryptococcus infeksjon (se kryptokokker nedenfor)
- Cryptosporidiosis parasitt («Krypto») er en ganske vanlig årsak til kraftig diare og magesmerter blant personer med et svekket immunsystem. Smitte via forurenset vann forekommer i hele verden, men vanligst i Afrika, India og Midt-Østen (Vanthy K, 2017).
- Cytomegalovirus (CMV). Humant cytomegalo-virus (HCMV/HHV-5) er en type herpes-virus. Dette viruset har 40-80% av friske personer i kroppen, men det gir vanligvis ingen symptomer. Smittemekanisme er ikke helt klarlagt, men kan være via spytt og andre kroppsvæsker. CMV infeksjon kan bli alvorlig hos personer med et svekket immunsystem, under immundempende antirevmatisk behandling, etter organtransplantasjon eller ved HIV infeksjon (Halenius A, 2014).
- Epstein Barr virus (EB): kan utløse MAS/HLH hos disponerte, mononukleose. I løpet av livet har 90% av off hatt EBV-infeksjon som forekommer over hele verden. De fleste smittes i ung alder. Det tar ofte 4-7 uker fra smitte til utbrudd. Mange merker ingen symptomer eller litt forkjølelse, mens andre blir veldig syke. Symptomene omfatter da feber, smerter og rødhet i svelget/halsen og kraftig forstørrede lymfeknuter på halsen og andre steder. Prognosen er vanligvis utmerket, og de fleste blir friske av seg. Fryktede komplikasjoner er at en forstørret milt sprekker, noe som medfører en alvorlig indre blødning. Også lever-betennelse kan ses med høye leverenzymer i blodet. Enkelte blir så hoven i svelget/halsen at pusteproblemer kan oppstå (Fugl A, 2019).
- Giardiasis parasitt. Dett er en parasitt-sykdom som spres blant annet via forurenset drikkevann. Symptomer begynner 1-3 uker etter smitte (inkubasjonstid). Diare, magesmerter og vekttap er typisk. Oppkast og blodig avføring er mindre vanlig. Et svekket immunsystem disponerer for sykdommen. Sykdomsvarighet er 2-6 uker eller lenger (Hooshyar H, 2019).
- Hepatitt B, hepatitt C (se egne avsnitt ovenfor i dette kapitlet)
- Herpes simpleks. Ved forkjølelse kan blemmer og sår skyldes herpes simpleks virus. Symptomene er røde, væskefylte små blemmer som svir og brenner omkring munnen og på leppene. Dersom symptomene vedvarer uvanlig lenge, bør andre årsaker som Crohns sykdom, cøliaki, vitamin mangel eller HIV utelukkes. Sårene er mindre enn ved Behcets sykdom og blemmer er heller ikke typiske for denne. Disse munnsårene avtar i hyppighet med alderen og er vanligst blant barn og ungdom. Apoteket har skyllevæsker og salver som kan være nyttige (Crimi S, 2019). Den mest alvorlige komplikasjon er herpes simpleks hjernebetennelse (encefalitt) som kan oppstå ved et svekket immunsystem og er livstruende.
- Herpes Zoster (“helvetesild). En av fire personer vil få herpes zoster i løpet av livet. Pasienter under immunsuppressiv behandling er spesielt utsatt. Shingrix er relativt ny vaksine på det norske markedet. Vennligst se også eget avsnitt nederst på denne siden.
- HIV (human immunodeficiency virus) er en type retrovirus som medfører en svekkelse av immunsystemet, slik at risiko for opportunistiske infeksjoner øker. HIV-viruset er også årsaken til acquired immunodeficiency syndrome (AIDS). Risikoen for opportunistiske infeksjoner er spesielt stor dersom immundempende medikamenter brukes.
- Histoplasmose (11,3%): Soppinfeksjon som er lite aktuell i Europa. Ses i USA, særlig i Ohio og Mississippi River Valleys og medfører pneumoni med noduli og artritt. Ved et svekket immunsystem som under immundempende, anti-revmatisk behandling, etter organtransplantasjon eller ved HIV infeksjon, er man mer mottakelig for histoplasmose infeksjon ( Olson TC, 2011).
- JC-virus (JCV) og PML infeksjon (progressiv multifokal leukoencefalopati). JC (John Cunningham) -virus (JC-virus, JCV) er et polyoma-virus, beslektet med BK virus som kan forårsake progressive multifokal leukoencefalopati (PML). PKL er en demyeliniserende sykdom som kan ligne multipel sklerose (MS). Den rammer hovedsakelig personer med et svakt immunsystem, for eksempel under anti-revmatisk behandling med rituksimab (Alstadhaug KB, 2017, Molloy ES, 2017, Maas RPPVM, 2016)..
- Kryptokokk infeksjon (3,8%): Mykose (Cryptococcus neoformans, Cryptococcus gattii). Den initiale infeksjonen i lungene gir vanligvis ingen symptomer. Hjernehinnebetennelse (meningitt). Diffuse symptomer gjør at det ofte går fra uker til måneder før diagnosen stilles (Fang W, 2019; Williamson PR, 2017; Brandshaw MJ, 2017; Sivertsen EA, 2004).
- Legionellose (5%); Legionella-bakterier som forårsaker legionær sykdom eller Pontiac feber. Feber, frost-anfall (feberfrysninger). Muskelsmerter, hodepine, utmattelse. Thoraks-smerter, hoste (tørrhoste eller med litt ekspektorat). Magesmerter og diare. Nyrebetennelse (glomerulonefritt), DIC (blødninger), Rabdomyolyse. Mental forvirring/nevropati. Inkubasjonstiden er 10-20 dager (Simonsen S, 2015).
- Listeriose (5%): Bakterie-infeksjon (listeria monocytogenes) som oppstår etter inntak av infiserte matvarer. Infeksjon under svangerskap kan medføre infeksjon hos den nyfødte eller dødfødsel. Feber. Diare og oppkast. Vertigo. Artralgi og myalgi. Meningitt, encefalitt.
- MRSA er infeksjon med Methicillin resistente staphylokokkus aureus som er en bakterie. Problemet er at behandling med antibiotika ikke virker. Pasienter med svekket immunsystem som har vært på sykehus i utlandet (der MRSA er et vanligere problem enn i Norge) er mest utsatt. En studie (fra Tyskland) viste imidlertid at personer med revmatiske sykdommer generelt ikke har oftere MRSA bakterier enn andre (Krämer J, 2018). Ved mistanke om smitte må spesielle prosedyrer bli fulgt (Hidron IA, 2010, Krämer J, 2018)
- Mykobakterier, ikke-tuberkuløse (11,3%): Mycobacterium avium complex (MAC) er vanligste organ. Lunger. Ledd. De er den vanligste ikke-tuberkuløse infeksjonen med mykobakterier som angriper lunger. MAC består av flere typer mykobakterier. Smitter ofte fra bakterier i urent vann eller vanndamp. Smitte fra akvarier (både ferskvann- og saltvann) forekommer (akvarie-granulom). Fra en smittes tar det 2-3 uker før eventuell infeksjon bryter ut (latenstid). Ikke smittsomt mellom mennesker (Tveiten H, 2018; Diel R, 2018 (MAC og lungebetennelse); Bi S, 2015 (Osteomyelitt); Henkle E, 2015; Tverer I, 2019 (akvariegranulom).
- Mykoplasma er en infeksjon med bakterien “Mycoplasma pneumonia”, oftest hos barn og unge voksne. Dette er ikke en klassisk ”opportunistisk infeksjon”, men ved et svekket immunsystem som under immundempende, anti-revmatisk behandling, etter organtransplantasjon eller ved HIV infeksjon, kan mykoplasma infeksjon bli alvorlig. Infeksjonen medfører hals- og lungebetennelse, men kan en sjelden gang spre seg til flere indre organer hos utsatte personer (Parrot GL, 2016, Tanaka H, 2016,, Miyashita N, 2009).
- Mykose, endemisk (1,3 %): Hud og slimhinner. Coccidioido-mykose (1,3%): Lite aktuell i Europa. Ses i Sørvestlige USA. Forårsaker “San Joaquin Valley fever” med feber, hoste, pleuritt, erythema nodosum, meningitt.
- Nocardiosise/actinomycose (12,15%): Gram-positive bakterier. Pneumoni; langsom progredierende. Encefalitt. Det finnes mange beslektede nocardia-bakterier. Infeksjonen angriper lunger, men også andre organer, deriblant hjernen. Kan ligne mange andre typer infeksjon, inklusiv tuberkulose og atypiske mykobakterier. Infeksjonen kan medføre svulst-lignede forandringer i muskler og skjelett, ellers ikke revmatiske symptomer. Tilstanden bør vurderes ved abscesser og subakutt infeksjon blant immunsupprimerte (Predersen HB, 2021; Li S, 2015; Yamagata M, 2013; Shariff M, 2016 (lunger)).
- Parvovirus B19 forårsaker ikke en klassisk ”opportunistisk infeksjon”, men er viktig å vurdere blant personer som får immunsuppresjon. Parvovirus B19 forårsaker utslett (erythema infektiosum), den såkalte 5. barnesykdommen blant små barn. Revmatologisk kan infeksjon medføre betydelig artralgi. Symptomer: ved debut (første uke) merkes influensalignende symptomer, feber, tetthet, hodepine, muskelsmerter (myalgi), forkjølelse, kløe. Blodprøver: anemi, leukopeni, trombocytopeni. Påfølgende uke: Utslett (rubella-lignende, mindre typisk hos voksne enn hos barn (erytehma infectiosum), artralgi. Blant barn med Erythema infectiosum får ca. 10% leddsmerter som også kan være enste symptom på infeksjonen. Voksne kan få en revmatoid artritt-lignende utbredelse med smerter og hevelser i mange ledd, inklusive fingerledd. Leddsmertene går tilbake av seg selv i løpet av tre uker, sjeldnere etter noen måneder (Soludo-Juresa D, 2015, Heegaard ED, 2002, Naides SJ, 1998.)
- Pneumocystis (PCP) (20%): Soppinfeksjon. Angriper særlig lungenes basale deler. Friske personer kan være bærere av pneumocystis uten å ha symptomer (eller trenge behandling). Debut etter behandling med Prednisolon mer enn 15-20mg/d, rituksimab (Rixathon, MabThera) eller Sendoxan. Symptomer omfatter nattesvette, vekttap, tørrhoste, dyspne. Forebygging/profylakse, hvorav: Bactrim / Trimetoprim Sulfa (cotromoxasol) (enten 2 tabletter tre dager i uken eller 1 tablett daglig) er mest brukt, OBS! Interaksjon med metotreksat. Ved sulfa-allergi er Dapson 50mg x 1 et alternativ (utenfor godkjent indikasjon) (McKinnel JA, 2012; Mecoli CA, 2017).
- Pseudomonas er en bakterie (P. aeruginosa) som kan forårsake opportunistisk infeksjon i bronkier/lunger, urinveier, sår, øyne eller medføre blodforgiftning (sepsis). Også oppløsninger for kontaktlinser kan være forurenset med pseudomonas. Enkelte pseudomonas er resistente (motstandsdyktige) mot de fleste antibiotika. Infeksjonen medfører ikke revmatiske symptomer, men ved et svekket immunsystem som under immundempende, anti-revmatisk behandling, etter organtransplantasjon eller ved HIV infeksjon, kan infeksjonen bli alvorlig (Wakabayashi A, 2018).
- Q-feber. Bakterie-infeksjon forårsaket av Coxiella burnetii som angriper både dyr og mennesker. Q-feber er svært sjelden i Norge. Tilfeller har forekommet etter smitte i utlandet. Sykdommen forekommer på alle kontinenter med utbrudd i flere europeisk land, inklusiv Frankrike og Nederland. Husdyr som storfe, sau, geit, hund og katt kan være bærere av bakterien og smitte mennesker. En sjelden gang kan smitte overføres via flåttbitt. Inkubasjonstiden er 9-40 dager. Infeksjonen kan en sjelden gang medføre aneurisme på aorta. Dette kan forveksles med revmatisk/inflammatorisk aorta aneurisme. Revmatiske symptomer kan være myalgi (Bråten LC, 2016, Leknesund SH, 2019).
- Salmonellose (10%): Salmonella-bakterier. Abdominale kramper. Feber. Diare.
- Toksoplasmose (1,3%) er en parasitt-sykdom forårsaket av Toxoplasma gondii. Influensa-lignende symptomer og hevelse i lymfeknuter. Infeksjon under svangerskap kan medføre fosterskade. Ved svekket immunsystem som kan forekomme under behandling med immundempende medikamenter mot revmatisk sykdom, kan toksoplasmose i sjeldne tilfeller forårsake alvorlige komplikasjoner. Smitte: Infeksjon via katter, rått kjøtt (særlig lam). Avføring (fekal) smitte via urene hender. Symptomer: Akutt stadium, influensa-lignende, hovne lymfeknuter, myalgi som varer over måneder. Encefalitt. Øyesykdom (nekrotiserende chorio-retinitt) (Halonen SK, 2014).
- Trikinose er en sjelden parasittsykdom (flere typer trikiner) som oppstår når infisert svinekjøtt spises uten å ha vært gjennomkokt eller gjennomstekt. Utbredelse: Tilfeller er rapportert i en rekke land, inklusiv USA, Kina, Argentina og Russland. Symptomene følger sykdommens to typiske faser. I første fase i en ukes tid fra infeksjonstidspunkt merkes kvalme, diare og magesyreoppstøt. I neste fase angripes muskler som er smertefulle og svake, hevelser særlig rundt øyne og feber er også typisk. Små blødninger i negler forårsakes av betennelse i små blodårer (vaskulitt). Diagnosen mistenkes når minst tre av følgende seks tegn foreligger: feber, muskelsmerte, mage-tarm-plager, hevelse i ansiktet, eosinofili i blodprøve, blødninger ved og i øyne (subkonjunktivalt, subungualt og retinalt). Blodprøve viser også utslag ved spesielle tester mot trikiner (ELSISA antigen-tester) (Kosmidou M, 2021)
- Tuberkulose (12,5%). Mycobacterium tuberculosis. Oftest lunger.
- Ureaplasma urealyticum. Bakterien forekommer i urinveier og genitalia og kan i sjeldne tilfeller forårsake artritt. Spesielt er personer med nedsatt immunsystem utsatt. Et norsk beskrivelse av et tilfelle (referanse: Kvalvik SA, 2020).
- Vancomycin resistente enterokokker (VRE) forårsaker normalt ikke sykdom. Etter bruk av antibiotika særlig cefalosporiner mot infeksjoner, kan enterokokker bli resistente, slik at behandlingen ikke virker lenger. Vancomycin er et effektivt antibiotikum mot mange livstruende infeksjoner, men enkelte enterokokker er blitt resistente. Vankomycin-resistente enterokokker kalles VRE. Personer med svekket immunsystem, slik som under immundempende antirevmatiske legemidler kan bli alvorlig syke av VRE. Mer informasjon ved Folkehelseinstituttet. Litteratur: Folkehelseinstituttet (2023).
Forebyggende tiltak mot opportunistiske infeksjoner. Før oppstart av immundempende behandling som MabThera / Rixathon (rituksimab), RoActemra (tocilizumab) og en del andre biologiske medikamenter er det vanlig å utelukke tegn til infeksjoner med blodprøver: Hepatitt B og Hepatitt C, HIV (AIDS-virus), tuberkulose (Tbc) (aktiv eller latent) i blodprøve (Interferon Gamma Release Assay, IGRA-test). Vaksinering mot pneumokokk-infeksjon (vaksine mot lungebetennelse) og influensa er ofte et godt forebyggende tiltak. Profylaktisk antibiotika mot pneumocystis med Bactrim eller Dapson (ved sulfa-allergi) dersom pasienten får tung immunsuppresjon (rituksimab, cyklofosfamid, prednisolon mer enn 30mg/dag over flere uker eller kombinasjonsbehandlinger)
Behandling. Antibiotika er essensielt. Valget er avhengig av mistenkt eller påvist mikrobe. Ved kjent kolonisering med en problemmikrober som MRSA, VRE, ESBL bør empirisk behandling dekke for disse mikrobene. Det anbefales å rådføre seg med infeksjonsmedisiner, samt følge lokale prosedyrer ved eget sykehus.
Blant antibiotika som brukes er ulike kombinasjoner av ampicillin og gentamicin, penicillin og gentamicin, piperacillin/tazobactam. Meropenem med vancomycin. Også linezolid, 3. generasjons cefalosporin (for eksempel cefotaksim), amoksicillin/klavulansyre og ciprofloksacin. Trimetoprim-sulfa iv, metronidazol po/iv. Soppbehandling. For spesifikke valg og dosering anbefales annen litteratur.
Litteratur: Winthrop KL, 2015
Pneumoni
Læringsmål REV 170. Revmatologen skal selvstendig kunne ta opp anamnese med hensyn til sannsynlige mikrober som årsak til pneumoni, særlig etter utenlandsopphold. Selvstendig kunne vurdere forventet følsomhet for antibiotika og iverksette behandling.
Læringsmål REV 172. Revmatologen skal ha kunnskap om smitteverntiltak ved særlig smittsomme lungeinfeksjoner.
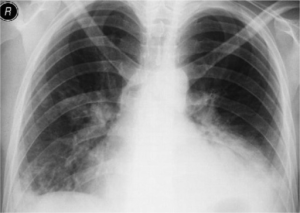
ICD-10: J18.9 (uspesifisert)
Definisjon. Pneumoni er inflammasjon i en eller begge lunger, vanligvis forårsaket av infeksjoner med bakterier, virus, sopp eller parasitter. Bakteriell pneumoni er vanligst. En kan klassifisere pneumonier i befolknings basert sykdom, sykehus-infeksjon, helsevesen-assosiert og ventilator assosiert sykdom, avhengig av infeksjonsveien. Bakteriell pneumoni deles inn etter etiologi i typisk og atypisk pneumoni. Begge typer har økt forekomst blant immunsupprimerte pasienter. Typisk pneumoni kan i motsetning til atypisk sykdom dyrkes på standard media eller ses ved Gram farging og er oftest forårsaket av Streptococcus pneumoniae, Haemophilus influenzae, Staphylococcus aureus, Gruppe A streptokokker, Moraxella catarrhalis, anaerobe og aerobic gram-negative bakterier. Atypisk pneumoni kan skyldes Legionella, Mycoplasma pneumoniae, Chlamydia pneumoniae og Chlamydia psittaci.
Anamnese. En bør ved atypisk pneumoni kartlegge om pasienten har vært eksponert for potensiell smitte som utenlandsopphold, kontaminert damp med legionella, menneskemengder (S.pneumonia, mycobacteria, mykoplasma, klamydia), husdyr eller fugler (coxiella burnetii, chlamydia psittaci). Risiko for aspirasjon vurderes (svelgevansker ved myositt, myopati, nevromuskulær sykdom, kramper, stoffmisbrukere, alkoholisme eller refluks).
Symptomer på pneumoni omfatter feber med tachykardi, frostrier og svettetokter. Hosten kan være tørr eller med ekspektorat, noen ganger blodtilblandet. Pleura kan være involvert i form av pleuritt med respirasjonsavhengige brystsmerter. Dyspne ved lav belastning, fatigue, hodepine, myalgi og artralgi ses også. Atypiske pneumonier har oftere ekstrapulmonale symptomer som påvirket mental funksjon og gastrointestinale symptomer ved legionella-pneumoni/legionellose.
Klinisk undersøkelse kan avdekke forhøyet kroppstemperatur over 38 grader eller i sjeldne tilfeller for lav temperatur. Økt respirasjonsfrekvens (mer enn 18 pr minutt), tachykardi (>100) sjeldnere bradykardi (<60/min) ved legionella. Perkusjon kan vise dempning over lungene. Auskultatorisk høres ofte krepitasjoner og bronkial respirasjon og i blant pleural gnidingslyd.
Laboratorieprøver omfatter Hgb, leukocytter med differensialtelling, trombocytter, kreatinin, elektrolytter, ALAT, CRP og blodkulturer. Arteriell blodgass gir informasjon om hypoksemi og respiratorisk acidose.
Urinen kan undersøkes for antigen eller PCR for spesielle agens.
Pulsoksymetri med pO2 <92% indikerer alvorlig hypoksemi.
Bildediagnostikk. Røntgen thoraks er standard. CT av lunger kan gi supplerende informasjon og er særlig aktuelt ved atypisk pneumoni.
Bronchioalveolær lavage (BAL) gjøres når analyse av bronkialsekret er viktig for behandlingen, for eksempel ved opportunistiske infeksjoner (pneumocystis).
Behandling med empirisk antibiotika skal begynne så raskt som mulig. Det er også viktig raskt å avklare om pasienten skal innlegges sykehus. Komorbiditet som kardiovaskulær sykdom, høy CRP, lav pO2 og utbredte radiologiske forandringer kan tilsi sykehusinnleggelse (Sattar SBA, 2023).
Protese-infeksjoner
Læringsmål REV 182. Revmatologen skal ha kjennskap til symptomer og tegn som indikerer infeksjon i protese, graft eller annet fremmedlegeme. Ha kjennskap til prinsipper for dannelse, forebygging og behandling av biofilm.
Sepsis
Læringsmål REV 169, Revmatologen skal selvstendig kunne bruke de rådende skåringskriteriene om faresignaler ved truende septisk sjokk. Selvstendig kunne finne sannsynlig fokus for sepsis og initiere adekvate videre undersøkelser. Selvstendig kunne iverksette initial antibiotikabehandling og støttebehandling ved sepsis.
ICD-10: A41.9 (uspesifisert)
Definisjon. Sepsis er en livstruende tilstand der infeksjon truer multiple organfunksjoner. Fortsatt er sepsis den vanligste dødsårsaken i en generell intensivavdeling.
Årsaker er septisk sjokk med hypovolemi, myokardskade og perfusjons-skader via vaso-regulerende mekanismer og mikrovaskulære tromboser som medfører iskemi i multiple organer. Disponerende faktorer er utbredelse av infeksjonen, virulens og pasientens miljø, genetikk, komorbiditet og medikasjon.
Symptomer og funn omfatter systemic inflammatory response syndrome (SIRS) som består av minst to av følgende: Temperatur >38 grader eller <36 grader. Hjertefrekvens >90/min. Tachype >20/min eller PaCO2<32 mmHg. Leukocytter >12.000 mm3 eller < 4000 mm3. Også NEWS kan anvendes i overvåkningen.
Klinisk kan sepsis medføre akutt respiratorisk distress syndrome (ARDS), kardiovaskulært septisk sjokk, akutt nyreskade, septisk encefalopati, critical illness anemi, myopati og nevropati. Septisk sjokk innebærer hypotensjon til tross for adekvat væskesubstitusjon.
Laboratorieprøver kan omfatte Hgb, leukocytter med differensialtelling, trombocytter, laktat, INR, kreatinin, ALAT, CRP, procalcitonin, lipase, TSH, f-T4, venøs blodgass, blodkulturer (minst to helst før antibiotika), fibrinogen, D-dimer. Viruspanel. Urin stiks og til mikrobiologisk diagnostikk.
Bildediagnostikk. Røntgen thoraks (ev. CT), vurder også CT caput, abdomen og bekken, MR cervikal- thoracal- og lumbalcolumna (epidural abscess).
Behandling skal ivaretagelse av organfunksjoner. Antibiotikabehandlingen bør følge nasjonale retningslinjer, med mindre det finnes lokale retningslinjer eller klare grunner til å avvike fra disse (bør journalføres). Empirisk antibiotikabehandling skal smales inn så snart mikrobiologiske funn eller pasienten tilstand tillater dette (Bullock B, 2023).
Sårinfeksjoner
ICD-10: L08.9
Definisjon. De vanligste bakterier er stafylokokker eller hemolytiske streptokokker. In noen tilfeller utvikles erysipelas (se nedenfor) eller systemisk infeksjon, inklusiv sepsis (se overfor). Pasienter med diabetes eller svekket immunsystem er mest utsatt for komplikasjoner.
Symptomer på infeksjon er smerter, erythem og sekresjon fra såret.
Undersøkelser omfatter anamnese på utløsende årsak og disponerende faktorer. Bakterie-undersøkelse (dyrkning) anbefales før ev. antibiotika.
Behandling omfatter rengjøring av sår, punksjon av abscesser. medikamentelt kan en sårsalve være effektiv. Ved kraftig infeksjon kan systemisk antibiotika være aktuelt. Ved ukomplisert infeksjon utenfor sykehus kan penicillin være et godt valg, et makrolid (erytromycin) ved penicillin-allergi. Mot stafylococcus aureus kan cloxacillin brukes (OBS! interaksjoner med metotreksat, warfarin med flere).
Urinveisinfeksjoner
ICD-10: N39.0 (uspesifisert lokalisasjon)
En ukomplisert urinveisinfeksjon skyldes bakterier i urinblæren (cystitt) og tilgrensende strukturer i nedre urinveier. Blant kvinner får ca. 40% urinveisinfeksjon minst en gang i livet, noe er en av de vanligste former for infeksjon. Bakteriuri uten symptomer regnes vanligvis ikke som en urinveisinfeksjon. Urinveisinfeksjon blant pasienter med svekket immunsystem, diabetes eller svangerskap og urinveisinfeksjon blant menn oppfattes som komplisert og krever spesiell oppmerksomhet fordi risiko for infeksjon også til øvre urinveier er økt. Reaktiv artritt kan utløses etter urinveisinfeksjon, særlig relatert til klamydiainfeksjon.
Sykdomsårsaker er bakterier, hvorav E. coli er vanligst. Andre bakterielle årsaker er proteus, klebsiella og enterokokker.
Symptomer på nedre urinveisinfeksjon er er vannlatingstrang, økt vannlatingsfrekvens, suprapubisk ubehag og dysuri. Ved spredning til øvre urinveier med pyelonefritt ses feber og smerter i nyrelosjer. Destruksjon av nyrevev /nefroner kan medføre hypertoni.
Blodprøver er aktuelle ved komplisert urinveisinfeksjon. Disse kan omfatte celletellinger (Hb, hvite med differensialtellinger, trombocytter), nyrefunksjonsprøver (kreatinin, eGFR) og inflammasjonsparametere (CRP). Blodkulturer.
Urin-undersøkelser med stiks (nitritt, ev også leukocytter og erytrocytter). Ved mistanke om komplisert urinveisinfeksjon er også bakteriekulturer å anbefale.
Bildediagnostikk i form av ultralyd og/eller CT av urinveier kan være aktuelt ved komplisert urinveisinfeksjon.
Behandling. Ukomplisert urinveisinfeksjon kan gå over uten behandling, men mange pasienter må behandles for å lindre symptomer og hindre at infeksjonen spres til nyrer / øvre urinveier). Antibiotika gis etter lokale anbefalinger. Mye brukt er trimetoprim sulfa, cefalosporin, nitrofurantoin over 1-6 dager er aktuelt. Asymptomatisk bakteriuri er aktuelt å behandle i svangerskap, blant immunsupprimerte og etter nylig urologisk-kirurgisk inngrep (Bono MJ, 2023). Ved komplisert urinveisinfeksjon kan være alvorlig og inkluderer livstruen de sepsis. Bredspektret antibiotika (før resistens-bestemmelse av initial urin-prøve) intravenøst på sykehus kan være nødvendig (Sabih A, 2023).
Urinveiskateter
Læringsmål REV 174. Revmatologen skal ha god kunnskap om indikasjoner og kontraindikasjoner ved bruk av blærekateter og pyelostomi-kateter.
Blærekateter er et tynt, rørformet instrument som føres inn i blæren gjennom urinrøret for å tømme blæren for urin. Pyelostomikateter er et kateter som settes inn i nyrebekkenet gjennom huden for å drenere urin fra nyren. Suprapubisk kateter kan legges via et kirurgisk snitt dersom det ikke er mulig å føre kateter til blæren via urinrøret, for eksempel ved tumor.
Indikasjoner for bruk av blærekateter: Urinretensjon, akutt nyresvikt, kirurgi (for å tømme blæren under operasjoner), urininkontinens.
Kontraindikasjoner for bruk av blærekateter: Urinveisinfeksjon (UVI), traume i urinrøret, prostatisme (en forstørret prostata kan gjøre det vanskelig eller umulig å føre inn et kateter).
Indikasjoner for bruk av pyelostomikateter: Obstruksjon av urinlederen, hydronefrose, nyrestein.
Kontraindikasjoner for bruk av pyelostomikateter: akutt nyresvikt (Pyelostomi kan forverre nyresvikten), urinveisinfeksjon (UVI), koagulasjonsforstyrrelser.
- Etter pyelostomi-kateter er lagt inn observeres pasienten for å utelukke blødning, infeksjon eller tett kateter. Forebygging av kateterrelatert urinveisinfeksjoner er beskrevet av Folkehelseinstituttets veileder, 2016.
VRE (vancomycin resistente enterokokker); Vennligst se avsnittet om Multiresistente mikrober ovenfor i dette kapitlet.
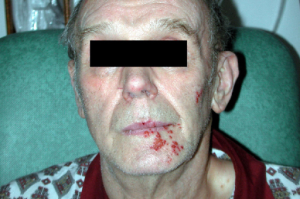
Zoster, herpes zoster
Definisjon. Herpes zoster er en virussykdom som forårsakes av varicella-zoster viruset, det samme viruset som forårsaker vannkopper. Etter å ha hatt vannkopper, forblir viruset latent i nervene. Hos noen personer kan viruset reaktivere senere i livet og forårsake helvetesild. Immundempende behandling mot revmatiske sykdommer øker risikoen for sykdommen.
Forekomst. En av fire personer vil utvikle herpes zoster (helvetesild) i løpet av livet. Risikoen stiger tydelig fra 50 års alder og ved svekket immunsystem, slik som ved bruk av immundempende medikamenter.
Symptomer. Utenom smertefullt eksem (ensidig) og lett feber kan infeksjonen medføre meningoencefalitt, sekundære stafylokokk- eller streptokokkinfeksjoner. Andre komplikasjoner omfatter zoster arteritt (vaskulitt) og slag, særlig relatert til zoster ophtalmicus (Bjark P, 2017). Postherpetisk nevralgi med intense, kroniske smerter forekommer hos 10-20% og kan vare i måneder-år.
Den nyere vaksinen Shingrix som erstatter den eldre (levende) Zovirax vaksinen og er anbefalt frfa 50-års alder. Immunsupprimerte pasienter er særlig utsatt for zoster og komplikasjoner og dermed også aktuelle for profylakse med vaksine (Winthrop KL, 2022).
Litteratur
- EULAR 2022 (Fraguolis GR, 2022; screening for opportunistiske infeksjoner)
- Norsk legemiddelhåndbok (behandling av infeksjoner)
- Winthrop KL, 2015 (behandling)
- Chung-Yuan Hsu, 2019 (risiko ved ulike revmatiske sykdommer)
- Di Franco M, 2017 (lungeinfeksjoner)
