BINDEVEVSSYKDOMMER (REV 021-033)
57 Interstitiell pneumoni med autoimmune kjennetegn/features (IPAF) (REV 022)
Øyvind Palm
Kjennetegn til IPAF (Interstitiell pneumoni med autoimmune kjennetegn/features)
Kroniske, inflammatoriske lungeforandringer kombinert med revmatiske symptomer og/eller antistoff.
Ikke klassifiserbar spesifikk bakenforliggende autoimmun, inflammatorisk revmatisk sykdom. Eksklusjon av antisyntetase syndrom, systemisk sklerose, Sjøgrens syndrom med flere.
Diagnosekoder ICD-10:: J84.1 (annen ILD med fibrose). M35.9 (uspesifisert bindevevssykdom)
Prosedyrekoder: EKG: FPFE15
ATC koder (for legemiddelstatistikk): L04A A Immunsuppressive legemidler
Definisjon
IPAF (Interstitiell pneumoni med autoimmune kjennetegn/features) er en sykdomsgruppe der det foreligger en kombinasjonen av inflammatorisk lungesykdom (ILD) i form av idiopatisk interstitiell pneumoni (IIP) og bakenforliggende symptomer og funn på en ikke nærmere klassifiserbar systemisk, autoimmun bindevevssykdom (Fisher A, 2015). Det er vist at 10-20% av tilfellene utvikler seg til definerte systemiske bindevevssykdommer (med lungemanifestasjon) i forløpet (Kono M, 2014; Sebastiani M, 2020). Således er det ikke klarlagt om IPAF er en distinkt sykdom eller en overlappende tilstand av andre sykdommer. Tilstanden er uansett et eksempel på at samarbeid mellom lungelege og revmatolog er nyttig i utredning og diagnostisering.
Historie
IPAF ble definert i 2015 av European Respiratory Society/American Thoracic Society (ERS/ATS). Hensikten var å definere en diagnose for pasientgruppen med idiopatisk interstitiell pneumoni som også har symptomer og funn som tyder på systemisk inflammatorisk bindevevssykdom, men ikke passer inn under en konkret diagnose. Definisjonen ble utarbeidet av en gruppe bestående av 13 lungeleger, fire revmatologer, en radiolog og en patolog (Fisher A, 2015). Før denne konsensus-rapporten viste flere studier at det forelå en undergruppe av interstitiell pneumoni med samtidige kliniske og serologiske tegn på ikke nærmere definert systemisk bindevevssykdom. Ulik terminologi og definisjon ble brukt, noe som var forvirrende og hindret sammenlignbare data (Shehata M, 2023).
Epidemiologi
Interstitiell lunge sykdom (ILD) er en stor gruppe sykdommer der lungevevet angripes. I ca. 30% av tilfellene foreligger en systemisk bindevevssykdom (Mitto S, 2009). Forekomsten av IPAF blant pasienter med ILD er usikker, men estimert til mellom 7 og 34%, avhengig av studiepopulasjoner og seleksjon. Til sammen utgjør ILD ved IPAF eller definert systemisk bindevevssykdom og idiopatisk lungefibrose de fleste tilfellene av ILD (Lee CT, 2017) (Raghu G, 2018). Alder ved debut varierer. De fleste med IPAF er omkring 60-65 år og forekomsten er lik mellom kvinner og menn. Dette er ulikt fra ILD ved definerte systemisk bindevevssykdommer der yngre kvinner vanligst angripes og fra idiopatisk lungefibrose som i større grad ses blant eldre menn (Shehata M, 2023).
Symptomer
- Symptomer på IPAF begynner typisk med økende tung pust ved belastning og vedvarende tørrhoste.
- Revmatiske, autoimmune symptomer er ofte leddsmerter (artralgi), artritt eller muskelsmerter (myalgi), Raynauds fenomen, utslett (Gottrons tegn, hovne/”puffy”fingre, palmar telangiektasi, udefinert eksem), feber eller symptomer fra ulike organer (Fischer A, 2015).
Undersøkelser
Sykehistorien kartlegger aktuelle symptomer med vekt på lunger og systemiske bindevevssykdommer med differensialdiagnoser.
Klinisk vurderes om tegn til spesifikk systemisk bindevevssykdom foreligger. Dette kan omfatte digitale symptomer som fissurer i form av “mekaniker hender” (antisyntetase syndrom), ulcerasjoner/nekroser (systemisk sklerose), artritt, Raynauds fenomen (systemisk sklerose, MCTD), teleangiektasier (systemisk sklerose, begrenset form), hovne/puffy fingre (MCTD, systemisk sklerose) og livide hudforandringer over MCP og PIP-ledd (Gottrons tegn ved dermatomyositt).
Laboratorieprøver kan omfatte celletellinger (Hb, leukocytter, trombocytter), lever- nyre- og thyreoidea-funksjonsprøver, CRP, SR og kreatin kinase (CK), samt urin stiks (proteiner eller blod). Antistoff-tester omfatter ANA som ved positiv test undersøkes for ENA og subgrupper. Myositt-spesifikke antistoff og/eller systemisk sklerose-blot bør også vurderes. Ved artritt undersøkes revmafaktorer (RF) og anti-CCP antistoff. For å utelukke tegn til vaskulitt i små eller mellomstor kar suppleres med ANCA (PR3 og MPO) (Jee AS, 2017).
Lungefunksjonstester vil tyde på nedsatt lungefunksjon som bør nærmere utredes radiologisk.
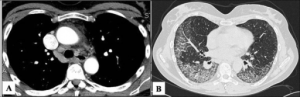
Bildediagnostikk er viktig. CT av lunger ofte i form av high-resolution chest tomography (HRCT) vil oftest vise tegn til non-spesifikk interstitiell pneumoni (NSIP), organisert pneumoni (OP) eller lymfocytisk interstitiell pneumoni (LIP) (Sambataro G, 2019). I tilfelle LIP eller usual interstitiell pneumoni (UIP) bør nærmere avklaring gjøres. LIP assosieres ofte med Sjøgrens syndrom. UIP er relativ uspesifikk, men ses ofte ved revmatoid artritt. Pleura– og perikardvæske kan også være en del av IPAF.
Klassifikasjonskriterier
Foreslåtte klassifikasjonskriterier for IPAF (Fisher A, 2015). For å oppfylle kriterier for IPAF kreves:
-
Radiologisk eller histopatologisk tegn på interstitiell pneumoni og
-
Komplett klinisk vurdering som utelukker andre årsaker til interstitiell pneumoni og
-
Inklomplette tegn til typisk systemisk bindevevssykdom (utelukke sikker SLE, Sjøgrens, (dermato-) myositt, systemisk sklerose, MCTD)
I tillegg til alle tre punkter ovenfor kreves minst ett punkt fra minst to av de tre domener i kolonne A, B og C i tabellen nedenfor:
| A. Kliniske kjennetegn | B. Serologi | C. Morfologiske manifestasjoner |
|---|---|---|
| 1. Distale digitale fissurer (mekaniker-hender)
2. Distale digitale ulcerasjoner på fingerpulpa 3. Inflammatorisk artritt eller polyartikulær leddstivhet om morgenen >60 minutter 4. Palmar telangiektasi 5. Raynauds fenomen 6. Uforklarte digitale ødemer / puffy hands 7. Uforklart vedvarende utslett over fingrenes DIP-ledd (Gottrons tegn) |
1. ANA ≥1: 320 titer, diffus, speckled, homogenent mønster or a) ANA nukleært mønster (uansett titer) eller b) ANA centromer mønster (uansett titer) 2. Revmatoid factor ≥2× øvre nivå av referanseområdet 3. Anti-CCP 4. Anti-dsDNA 5. Anti-Ro (SS-A) 6. Anti-La (SS-B) 7. Anti-ribonucleoprotein (RNP) 8. Anti-Smith (Sm) 9. Anti-topoisomerase (Scl-70) 10. Anti-tRNA syntetase ( Jo-1, PL-7, PL-12, EJ, OJ, KS, Zo, tRS) 11. Anti-PM-Scl 12. Anti-MDA-5 |
1. Typisk radiologisk mønster ved HRCT a) NSIP b) OP c) NSIP med OP overlapp d) LIP 2. Histopatologisk mønster eller funn ved kirurgisk lungebiopsi: a) NSIP b) OP c) NSIP med OP overlapp d) LIP e) Interstitielle lymfoide aggregater med germinale sentre f) Diffus lymfoplasmacytisk infiltrasjon (med- eller uten lymphoide follikler) 3. Multi-compartment manifestasjon (i tillegg til interstitiell pneumoni): a) Uforklart pleuravæske eller pleurafortykkelse b) Uforklart perikardvæske eller perikardfortykkelse c) Uforklart interstitiell lungesykdom d) Uforklart pulmonal vaskulopati |
LIP: lymfoid interstitiell pneumonia NSIP: non-spesifikk interstitiell pneumoni. OP, organiserende pneumoni.
Differensialdiagnoser
Symptomer og funn ved IPAF overlapper med andre tilstander. En bør spesielt skille IPAF fra følgende tilstander:
-
Idiopatisk pulmonal fibrose (IPF)
-
ILD relatert til spesifikke systemisk bindevevssykdommer (CTD-ILD) som antisyntetase syndrom, dermatomyositt og systemisk sklerose
-
Cryptogen organisert pneumoni (COP)
-
Idiopatisk non-spesifikk interstitiell pneumoni (NSIP)
-
Lymfocytisk interstitiell pneumoni (LIP)
- Sarkoidose
Behandling av IPAF
Kortikosteroider, csDMARDs, biologiske legemidler og antifibrotisk behandling. Lungeforandringene ved IPAF strekker seg fra inflammasjon til fibrose med økt bindevev. Mens inflammasjon lar seg behandle med kortikosteroider (prednisolon, SoluMedrol) og andre immundempende medikamenter (csDMARDs som cyclofosfamid, mykofenolat, azathioprin, ciclosporin A eller biologiske legemidler som rituksimab), kan fibrose behandles med anti-fibrotiske medikamenter som nintedanib/Ofev (Fischer A, 2013; Keir GJ, 2013; Kottin V, 2014; Shehata M, 2023). Mange anbefaler behandlingsstart med medikamenter dersom lungeforandringene øker og omfatter 20% eller mer av lungevevet (ved HRCT). Dersom en velger behandling med medikamenter, baseres vurderingen på den enkeltes sykdomsforløp og gjøres av erfarne leger, oftest spesialister i lungesykdommer i samråd med spesialister i revmatologi. Gode studier for behandling av IPAF foreligger ikke og behandlingen er således utprøvende (Torrisi SE, 2019).
Annet. Utenom legemidler er lungerehabilitering, oksygentilskudd over tid og behandling av eventuell gastroøsofageal refluks aktuelt.
Prognose
Det foreligger begrensede data, men foreløpige resultater tyder på at overlevelsen ved IPAF er sammenlignbar med systemisk bindevevssykdommer med tilsvarende lunge-manifestasjoner og bedre enn ved idiopatisk lungefibrose (Wells AU, 2020).
Oppfølging
Dersom lungeforandringene er de mest alvorlige manifestasjonen av sykdommen, er regelmessig oppfølging hos lungelege essensielt. HRCT undersøkelser og lungefunksjons-undersøkelser, eventuelt supplert med 6-minutters gangtest benyttes ofte. Revmatologer bidrar ofte med lang erfaring med de immundempende medikamentene og vurdering av ulike sykdomsmanifestasjoner utenom lungene. Utenom progressiv lungefibrose, bør en også følge opp med tanke på pulmonal hypertensjon, cor pulmonale, lungesvikt som krever oksygen og fordi risiko for depresjon og angst foreligger (Shehata M, 2023).
Litteratur
