ANDRE SYKDOMMER (REV 063-REV 077)
180 Malignitet/Kreft og revmatiske sykdommer. Cancermarkører. Sjekkpunkthemmere (REV 075, REV 201, REV 200)
Øyvind Palm and Jan Tore Gran
Læringsmål REV 075. Revmatologen skal selvstendig kunne oppdage primær-tumores i ledd og leddnære strukturer.
- Vennligst se også kapitlet om tumorer i ledd og leddnære strukturer og nedenfor i dette kapitlet.
Introduksjon.
Revmatiske sykdommer og kreft er to ulike sykdomsgrupper som kan ha overlappende symptomer og påvirke hverandre. Begge involverer immunsystemet, noe som kan skape kompliserte kliniske sykdomsbilder (Cappelli CL, 2020).
Revmatologer bør ha gode kunnskaper om kreft av flere årsaker:
- Differensialdiagnostikk: Revmatiske sykdommer og kreft kan forekomme samtidig. Det er avgjørende å kunne skille mellom symptomene for å sikre korrekt diagnose og behandling av begge tilstandene.
- Økt kreftrisiko: Enkelte revmatiske sykdommer øker risikoen for å få noen typer kreft. Revmatologer må derfor være årvåkne med denne risikoen for øye /Bernal-Bello D, 2025).
- Bivirkninger av kreftbehandling: Kreftbehandling kan utløse eller forverre revmatiske symptomer. Revmatologer kan bidra med behandling og lindring av disse bivirkningene.
- Kreft med revmatiske symptomer: Enkelte kreftformer kan gi symptomer fra ledd og muskler. Disse kan forveksles med primære revmatiske sykdommer.
En god forståelse av sammenhengen mellom revmatiske sykdommer og kreft kan være viktig for å gi optimal behandling og oppfølging til pasientene med disse tilstandene.

Kreft og autoimmun respons. Kreft kan forårsake en autoimmun respons med revmatiske symptomer. Lymfom er et eksempel. Denne typen kreft er vist å gi autoimmune manifestasjoner i 4,3% av tilfellene, herav immun-cytopenier (71,3%), nevrologiske utfall (10,2%), glomerulonefritt/kryoglobuliner (6,6%) og systemisk vaskulitt (5,6%) (Jachiet V, 2017). Andre funn inkluderer hovne lymfeknuter, feber, nattesvette og vekttap i tillegg til leddsmerter og inflammasjon som kan ligne revmatiske sykdommer.
Felles symptomer på malignitet og revmatisk sykdom kan være:
- Artralgi
- Artritt
- Fatigue/utmattelse
- Feber og vekttap
- Hovne lymfeknuter
- Muskel– eller skjelettsmerter
- Vaskulitt
Symptomer som gjør at revmatologen bør mistenke kreft
Læringsmål REV 201. Revmatologen skal ha kunnskap om revmatiske symptomer ved maligne sykdommer.
Revmatologen bør utrede med tanke på kreft dersom pasienter med revmatisk sykdom uten god annen forklaring (f. eks. infeksjon eller aktiv inflammatorisk revmatisk sykdom) (Naschitz JE ACS, 1995) får hovne lymfeknuter, feber/nattesvette eller vekttap.
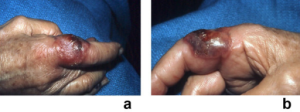
Paraneoplastiske revmatiske manifestasjoner
Paraneoplastiske manifestasjoner fra bevegelsesapparatet kan skyldes at cancerceller produserer abnorme mengder cytokiner og hormoner. Det kan da også dannes (“falsk positive”) antistoffer på grunn av tumorantigener eller ved at tumor stimulerer til hypersensitivitetsreaksjoner og lager immunkomplekser.
Kliniske kjennetegn:
- Tidsmessig relasjon til kreftsykdommen: Symptomene opptrer ofte i forbindelse med kreftdiagnose eller underveis i kreftsykdommen.
- Uvanlig sterkt påvirket allmenntilstand: Pasienten kan ha en betydelig dårligere allmenntilstand enn det som kan forklares av den revmatiske manifestasjonen alene.
- Atypisk debut og sykdomsforløp: Symptomene kan debutere atypisk revmatisk sykdom og ha et uvanlig forløp.
- Manglende virkning av antirevmatisk behandling: Revmatisk behandling har liten eller ingen effekt på paraneoplastiske manifestasjoner.
- Respons på vellykket kreftbehandling: Symptomene bedres ofte betydelig når kreftsykdommen blir effektivt behandlet.
Maligne sykdommer som lett feiltolkes som revmatisk sykdom
Ledd- og skjelettsmerter, metastaser. Når primærtumor eller metastaser er lokalisert i skjelett, Ieddnært eller tumor påvirker muskulatur, kan artropati eller myopati være dominerende symptomer. Eksempler er knesmerter ved cancer prostata med metastaser til distale femur ved kneleddet eller synovialcellekarsinom med artritt-lignende symptomer.
Kreft som relativt ofte metastaserer til skjelett inkluderer:
- Bryst/mamma: Den vanligste formen for kreft hos kvinner. Brystkreft kan spre seg til skjelettet, og det er ofte et av de første stedene det sprer seg til. Symptomer på skjelettmetastaser kan være smerter, frakturer og hyperkalsemi (Gerke O, 2025).
- Prostata: Den vanligste formen for kreft hos menn. Prostatakreft sprer seg ofte til skjelettet, spesielt ryggvirvler, bekken og ribbein. Symptomer på skjelettmetastaser fra prostatakreft kan være smerter, stivhet og nevrologiske problemer (Guo X, 2025).
- Lunge: Lungekreft kan spre seg til skjelettet, og det kan gi symptomer som smerter, brudd og nevrologiske problemer (Wang S, 2025).
- Nyre: Nyrekreft kan spre seg til skjelettet, og det kan gi symptomer som smerter, brudd og hyperkalsemi (Brown J, 2024).
- Myelomatose; En type kreft som oppstår i benmargen og påvirker plasmacellene. Myelomatose kan forårsake skader på skjelettet som kan føre til smerter, brudd og hyperkalsemi (Gay F, 2025).
- Thyreoidea: En relativt sjelden form for kreft som kan spre seg til skjelettet, spesielt ryggvirvler og ribbein. Symptomer på skjelettmetastaser fra thyreoideakreft kan være smerter og brudd (Nervo A, 2020).
- Urinblære: Urinblærekreft kan spre seg til skjelettet, men det er mindre vanlig enn for de andre kreftformene som er nevnt her (Stellato M, 2021).
- Sarkomer: En sjelden type kreft som oppstår i bindevevet. Sarkomer kan spre seg til skjelettet, og det kan gi symptomer som smerter, hevelse og brudd (Hosseini H, 2021).
Vennligst se kapitlet om tumorer i ledd og leddnære strukturer.
- Barn med nyoppstått smertefull artritt ledsaget av lave antall blodceller (ofte -penier i alle tre cellerekker) og redusert allmenntilstand bør vurderes av pediater, bl.a. pga. risiko for samtidig leukemi. Muskel og skjelettsymptomer, inklusiv halting er vanlig og kan være første sykdomstegn hos ca. en av tre barn. Symptomene kan da lett feilaktig tolkes som revmatologisk eller ortopedisk sykdom, noe som forsinker diagnosen (Mamman E, 2007).
I sykdomsforløpet ses imidlertid mer typiske leukemi-tegn som nattlige smerter, leukemiske infiltrater i hud eller skrotum, økt blødningstendens ved trombocytopeni, blekhet ved anemi, feber og infeksjoner ved leukopeni (Hunger SP, 2015).
- Artritt rapportert ved adult T-celle-leukemi, myeloid-leukemi, hårcelle-leukemi (kan også gi vaskulitt) og akutt lymoblastisk leukemi hos voksne (Slouma M, 2023). Ca. 15 % av leukemi-pasienter debuterer med artritt. Undersøkelse av leddvæske viser ikke alltid maligne celler. Artritten er oftest asymmetrisk, migrerende og ledsaget av skjelettsmerter, samt lokal ømhet. Opptil 20 % av cancerpasienter har serum-revmafaktor (RF), men sjelden anti-CCP. Vennligst les også om leukemier i kapitlet om blodsykdommer.
Lungekreft:
- Hypertrofisk (pulmonal) osteoartropati (se illustrasjon nedenfor) ved primær og metastaserende ca. pulm (clubbing, periostitt og artropati). Obs! Når artritt ledsages av ømhet av tilgrensende rørknokler (Kim J, 2024).
Myelodysplastisk syndrom:
- Ofte ledsaget av autoimmune fenomener (systemisk vaskulitt, kutan vaskulitt, autoimmun trombocytopeni, polyartritt, kolon ulcerasjoner, relapsing polykondritt og Sjøgrens syndrom). Feber, pleuritt og perikarditt sees ikke sjelden. Hyppigst med leukocytoklastisk vaskulitt og overlapp-syndromer.
- Kutane forandringer (purpura, noduli, papler, hudnekrose) sees hos 2/3. Ofte kan man påvise kromosomforandringer (Hasserjian RP, 2023).
Prognosen er i utgangspunktet dårlig, men den forverres ikke ved koeksisterende autoimmune manifestasjoner (Giannouli. Rheumatology 2004; de Hollanda et al. Arthritis Care Res 2011 ).
Non-Hodgkins lymfom: Kan forutgås av primært Sjøgrens Syndrom og debutere med lokalisert myalgi (quadriceps) eller polyartritt (Shi X, 2024).
Tabell. Paraneoplastisk artritt. 92 pasienter med kreft-diagnose maksimalt to år etter debut av artritt (Kisacik B, 2024)
| Paraneoplastisk (n=92) | Solide tumorer (n=53) | Hematologisk kreft (n=39) | |
| Alder | 50,9 år | 56,6 år | 43,3 år |
| Kvinner | 39% | 36% | 33% |
| Polyartritt | 39% | 38% | 41% |
| Oligoartritt | 41% | 49% | 31% |
| Monoartritt | 20% | 13% | 28% |
| SR (mm/t) | 60 | 60 | 62 |
| CRP (mg/L) | 72 | 59 | 90 |
| RF+/anti-CCP+ | 20%/8% | 24%/11% | 12%/3% |
| LD (U/L) | 566 | 316 | 857 |
Læringsmål REV 200. Revmatologen skal ha kunnskap om kreftutredning og under supervisjon kunne igangsette utredning av pasienter med mistanke om malign sykdom.
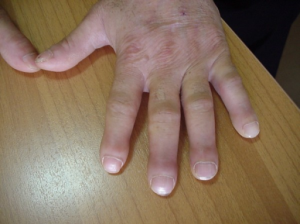
Utredning
Utredning ved mistanke om malign sykdom kan omfatte følgende:
-Anamnese. Risikofaktorer som genetisk disposisjon, miljøfaktorer (røking, tidligere cytostatika eller langvarig immunsuppresjon), tidligere kreft. Uforklarlig vekttap og/eller fatigue, feber av ukjent årsak, blod i avføringen, vedvarende hoste eller hemoptyse, blod i urinen, endret vannlating, kul i brystet, forstørrede lymfeknuter.
-Klinisk undersøkes hode og hals (harde, uømme lymfeknuter), hud (nevus, sår som ikke gror), brystene/mamma (knuter), abdomen (harde knuter) og rektalundersøkelse av endetarm med prostata.
-Laboratorieundersøkelser: Hb, leukocytter med differensialtellinger, trombocytter, kalsium, ALAT, ASAT, gamma.GT, LD, kreatinin, pankreas-amylase eller lipase, kreatin kinase (CK), blodsukker, TSH, f-T4, proteinelektroforese.
Tumor-markører: vennligst se avsnittet nedenfor. Urin stiks.
-Avføring ved kolorektal kreft. Tradisjonelt påvises spor av blod ved kvalitative, kjemiske tester, slik som Hemo-Fec. Imidlertid er sensitiviteten bare ca. 75% (Bjerregaard NC, 2009) og den påvirkes av inntak av grønnsaker, kjøtt og vitamin C. Nyere tester, for eksempel FIT (fecal immunological test), benytter antistoff rettet mot globindelen av hemoglobin og påvirkes ikke av kosthold og det tas kun en prøve. De er dermed mer sensitive og spesifikke for å påvise GI-blødning (Schwettmann L, 2022).
-Bildediagnostikk. CT thoraks/abdomen/bekken, mammografi av kvinner. Dersom utredningen styrker mistanken eller ikke avkrefter mistanken, er mer spesifikk utredning indisert. Denne kan omfatte MR, PET/CT og tumormarkører (se nedenfor). Det er viktig at ikke mye tid går til spille, slik at henvisning til spesialavdeling (pakkeforløp) kan være aktuelt.
-Andre: endoskopi, bronkoskopi, biopsi
Screeningprogrammer i Norge
Befolkningsbaserte screeningprogrammer for brystkreft og livmorhalskreft (kvinner) og tarmkreft gjøres via mammografi, celleprøve og avføringstest. I tillegg vurderes innføring av screening for lungekreft med lavdose-CT for røkere. Til sammen utgjør disse kreftformene va. 50% av alle krefttilfellene (Weinberg D, 2025).
Tumormarkører
Tumormarkører er oftest proteiner som produseres av svulster. De passerer basalmembranen og kan påvises i perifert blod (også i spinalvæske). De dannes også i friskt vev, men slipper i liten grad over i blodsirkulasjonen. Tumormarkører kan være nyttige i utredningen av flere typer kreft, men markørene er sjelden organspesifikke og aldri spesifikke for kreft. Blant annet kan lever og nyresykdommer kan medføre falskt forhøyede verdier/utslag. Også ved inflammasjon og benign hyperplasi av det aktuelle organet kan forhøyede verdier ses. Man anbefaler derfor forsiktig bruk og kritisk tolkning av tumormarkører (Filella X, 2022).
Supplerende utredning kan være PET/CT. Ved hovedsakelig nevrologiske manifestasjoner kan det dreie seg om paraneoplastisk nevrologisk sykdom (PNS) som i noen tilfeller kjennetegnes ved nevrogene antistoff som anti-PNMA2, anti-Ri, Anti-Yo, Anti-CV2, anti-Hu, anti-Recoverin, anti-Zic4, anti-TC, anti-SOX1 (Devine MF, 2021). Disse er også listet i tabellen nedenfor:
Noen tumormarkører i blodet:
- 5-HIAA. 5-hydroksyindolacetat. Karsinoide svulster
- Acetylkolin-reseptor antistoff. Thymom. Myasteni.
- alfa-1-føtoprotein (AFP): Hepatocellulær cancer (kronisk hepatitt, levercirrhose) < 14kU/I
- Ca125. Ovarialcancer (betennelser og graviditet). Produseres i peritoneum, pleura, perikard og normalt endometrium og øker (uspesifikt) ved irritasjon og sykdom i disse organene. < 35kU/I
- CA19-9. Svulster i pankreas eller galleveier (galle-stase). Andre tilstander med galle-stase og andre svulster. Lav sensitivitet og spesifisitet. Ikke anbefalt screening, men i oppfølging. < 60kU/I
- CEA Karsinoembryonalt antigen. Kolon-cancer, brystkreft.
- CV2-antistoff. Småcellet lungecancer, thymom. Sensorisk og sensomotorisk nevropati, ataksi, limbisk encefalopati, autonom nevropati.
- hCG og AFP. Testikkelkreft, hCG hos 50% med non-seminomer og 20% med seminomer. AFP øker ikke ved seminom.
- HE4, human epididymidis protein 4. Markør for ovarie-kreft. Bør tas sammen med CA125. <60pmol/L < 60 år, <80pmol/L >80 år.
- Hu-antistoff. Småcellet lungecancer. Vertigo, ataksi, parestesier, depresjon, kramper.
- Immunglobuliner. Paraprotenemi/uri ved myelomatose (IgG vanligst). IgM ved Waldenstöms makroglobulinemi
- Karsinoembryonalt antigen (CEA). ved kolorektal cancer (også ved ca. pankreas, lungecancer, metastaserende thyreoidea-karsinom og metastaserende mammacancer, samt ved kroniske leverlidelser og røykere) > 5mikrog/I. Økt verdi blant røkere, høy alder og kronisk leversykdom. Ikke anbefalt til screening.
- MUC-1. Systemisk residiv av cancer mamma. Økt også ved benign og malign sykdom i kolon, pankreas, lever, lunge, ovarier og prostata. <35kU/L.
- Neuronspesifikk enolase (NSE) og proGRP. Småcellet lungecancer (SCLC) (også ved nevroblastomer, hjernemetastaser, metastaserende maligne melanomer, seminom). NSE lett økt ved hemolyse. ProGRP nyttig supplement ved SCLC.
- PNMA2-antistoff. Testes tumorer. Paraneoplastisk limbisk encefalitt, diencefalittisk dysfunksjon, hjernestamme encefalitt.
- Prostata-spesifikt antigen (PSA). Ca. prostata (benign hypertrofi, prostatitt og urinretensjon). Stiger etter rektaleksplorasjon, kateter og sykling. Ved alder over 60 år er referanseverdien < 4μg/I, alder under 50 år <2,5 μg/I. 50-60års alder: referanse <3,5 μg/I
- Recoverin-antistoff. Cancerassosiert retinopati (CAR), melanomassosiert retinopati. Akutt eller subakutt synstap.
- Ri-antistoff. Brystkreft. Paraneoplastisk cerebral dysfunksjon.
- S100B ved malignt melanom (og ved hodeskader)
- SOX1-antistoff (Glianukleært). Småcellet lungecancer. Lambert-Eaton myastenisk syndrom.
- TG + TGAB. Oppfølging etter behandlet thyreoideacancer. Thyreoidektomerte skal ikke ha målbar TG
- TIF1Υ / P-155/140 antistoff. Cancer assosiert myopati / dermatomyositt
- NXP-2-antistoff (anti-nuclear matrix protein): Cancer assosiert myopati / dermatomyositt (Fierotino DF, 2013)
- Titin-antistoff. Thymom. Myasteni.
- Tr (DNER)-antistoff. Hodgkins lymfom. Paraneoplastisk cerebellær degenerasjon; hodepine, ataksi, fotofobi, feber.
- Zic4-antistoff. Småcellet lungecancer. Paraneoplastisk cerebellær degenerasjon (PCD). Koeksistens med Hu-antistoff.
- Yo-antistoff. Brystkreft. CNS: Ataksi, nystagmus, diplopi, vertigo, dysartri.
Multi-cancer early detection test (MCED)
MCED-tester påviser sirkulerende cellefritt DNA (cfDNA) fra kreftsvulster i perifert blod. Testene er imidlertid mindre følsomme for kreft i tidlig stadium enn mange av dagens screening-tester. En studie av 6 700 kvinner viste at en MCED-test hadde en høy spesifisitet på 99% for kreft i ulike organer, men sensitiviteten var skuffende lav på 18% for stadium I-svulster og 43% for stadium II-svulster. MCED-tester er møtt med stor entusiasme. Man anbefaler likevel å være forsiktige med bruken inntil randomiserte studier med forekomst og dødelighet av kreft som enderesultater foreligger (Weinberg D, 2025).
Kreftbehandling og revmatiske symptomer
Behandling av kreft og revmatiske sykdommer kan ha lignende bivirkninger, som tretthet, kvalme og håravfall. Det er derfor flere grunner til at revmatologen må kjenne til kreftsykdommer. I kreftbehandlingen har immunologiske sjekkpunkthemmere fått en sentral plass. Imidlertid medfører denne behandling immunrelaterte bivirkninger hos 10-20% og 3-7% får revmatiske tilstander (Calabrese L, 2020).
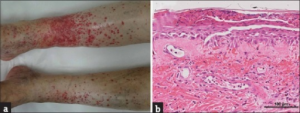
Sjekkpunkthemmere/signalhemmere
Mer enn 40% av all kreft kan behandles med sjekkpunkthemmere. Blant bivirkninger er imidlertid en rekke autoimmune fenomener. Disse kan oppstå der en ellers også ser autoimmune sykdommer, slik som i ledd, muskler, benmarg, nervesystem, hud, slimhinner og tarm. Revmatologiske bivirkninger fra ledd eller muskler ses hos 1-4%.
Type 1. Vanligst er oligoartikulær artritt (Type 1), symmetrisk RA-lignende, symmetrisk småledds-artritt som begge er selvbegrensende, polymyalgia revmatika-lignende symptomer, myositt og Sjøgrens syndrom-lignende (ofte SSA-negative sicca-fenomener (Kostine M, 2018)).
Symptomer behandles ved behov med kortikosteroider, men behandlingen kan interferere med kreft-behandlingen. Ved prednisolon-doser ≤ 10 mg/ dag kontinueres vanligvis sjekkpunkthemmer-behandlingen. Mindre enn 10% av tilfellene med artritt vil trenge supplerende anti-revmatisk behandling.
Type 2. Sjeldnere oppstår mer alvorlige autoimmune sykdommer, til dels med typiske antistoff som varer en begrenset periode (Type 2). Eksempler er CCP-positiv RA, Sjøgrens syndrom med SSA-antistoff, myasteni med anti-ACE antistoff og diabetes type-1 med pankreas-øycelle-antistoff. En relasjon til eosinofil fasciitt er også rapportert.
Type 3. Noen utvikler kronisk revmatisk sykdom (Type 3). En sjelden bivirkning er Vogt-Koyanagi-Harada syndrom-lignende toksisitet. Symptomvarighet er oftest noen måneder, til dels avhengig av hvor lenge sjekkpunkthemmere gis (Braaten TJ, 2020).
Granulocyttkolonistimulerende faktor (G-CSF)
En sjelden gang (mellom 1 per 1 000 og 1 per 10 000) er aortitt utløst av granulocyttkolonistimulerende faktor (G-CSF). En slik bivirkning av G-CSF etter for eksempel kreftbehandling bør mistenkes dersom feber og vedvarende forhøyede inflammasjonsparametere foreligger (Gaustad A, 2025).
Antirevmatisk behandling ved kreft
Selv om revmatologiske manifestasjoner foreligger, har optimal behandling av kreftsykdommen vanligvis første prioritet. Unntak kan være svær myositt, myokarditt, pneumonitt eller inflammatorisk tarmsykdom. Det er usikkert om immunmodulerende anti-revmatiske medikamenter som klassiske DMARDs, biologiske legemidler og høye doser kortikosteroider generelt kan være ugunstige for kreftsykdommen. Om nødvendig, er kortikosteroider førstelinje behandling. En tilstreber lavest mulige effektive dose f. eks. prednisolon 10 mg/dag eller lavere.
For biologiske legemidler har en over tid ikke observert sikre holdepunkter for økt kreftutvikling eller økt residivrate ved tidligere malign sykdom (Wong PKK, 2018). Når en ser på overlevelse etter kreft, kommer pasienter som kontinuerer TNF-hemmere ikke dårligere ut, heller motsatt, etter opp til tre års observasjonstid (Ruiz JI, 2025). Flere data er imidlertid ønskelig (Regierer AC, 2018; Vedamurthy A, 2022). For abatacept (Orencia) er sjekkpunkthemmeren iplimumab er en antagonist, slik at effekten kan påvirkes (Calabrese L, 2020).
I praksis vil en individuell vurdering der en tar hensyn til den revmatiske manifestasjonens alvorlighetsgrad og kreftsykdommens prognose være avgjørende for valg av medikasjon (Jeon CH, 2022).
Revmatiske sykdommer som kan være forbundet med malignitet
Enkelte revmatiske sykdommer for eksempel dermatomyositt hos voksne eller eosinofil fasciitt er assosiert med en økt forekomst av maligne lidelser.
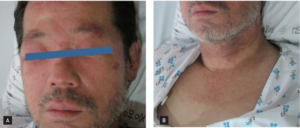
Amyloidose: Myelomatose kan gi amyloidavleiring og polyartritt med svær periartikulær hevelse (“The shoulder pad sign”). Også hender og knær. Hyppig med samtidig “karpal tunnel syndrom”.
Arthritis urica (urinsyregikt): Økt forekomst av urologiske, gastrointestinale og lungecancer (Wang W, 2015). Høye urinsyrenivåer og urinsyregikt ses sekundært ved myeloproliferative sykdommer, spes. polycytemia vera. Obs! For mulighet for cancer hos kvinner med a. urica som ikke har brukt diuretika.
Ankyloserende spondylitt/Bekhterevs: Lymfom kan medvirke til hurtig progredierende sakroiliitt. Mulig litt økt risiko for ca. coli, myelomatose og lymfom (Deng C, Scientific Reports, 2016
Cancer artritt: Dette er et uklart begrep som omfatter pasienter med akutt debut av RA-liknende sykdom hvor behandling av underliggende cancer fører til remisjon av polyartritt-sykdommen. Mistanke ved manglende affeksjon av hender, seronegativitet og asymmetrisk artritt, særlig med økt ALP i blodet. Ofte akutt debut av asymmetrisk artritt f eks. i underekstremiteter, og menn er overrepresentert. Relativt dårlig behandlingsrespons på steroider og DMARDs (Manger B, 2014). Perifer artritt ved PMR kan også være et symptom på malignitet (Michitsuji T, 2018). Artritt kan også ses ved T-celle lymfom med infiltrasjon i synovia, og leukemi kan debutere med artritt.
Dermatomyositt hos voksne: Cancer påvises hos 7-15 %. Økt risiko gjelder ikke polymyositt i særlig grad, sjelden personer under 49 år og ikke barn med (juvenil) dermatomyositt.
I de fleste cancer-tilfellene ved ny-diagnostisert dermatomyositt oppstår innen 1 år fra dermatomyositt-debut. Hyppigst med epitelial cancer: ovarier, ventrikkel, nasofaryngeale (asiater). Ca. coli er sjelden.
Hos 70 % oppstår cancer etter muskelsykdommen. I en norsk epidemiologisk studie var cancerrisikoen doblet ved dermatomyositt (standard insidens rate 2.0). Tilsvarende ved polymyositt var SIR = 1.3, mens inklusjonslegememyositt ikke hadde økt kreft-risiko (SIR = 0.9). Ovarialkreft var vanligere ved dermatomyositt enn blant kontrollene fra den generelle befolkningen (8.3% vs. 1.1%) (Dobloug GC, Semin Arthr Rheum, 2015).
De dermatomyositt-assosierte antistoffene TIF-1 gamma og NXP-2 disponerer for malign sammenheng. En internasjonal anbefaling til kreft-screening ved myositt foreligger (Oldroyd AGS, 2023).
Eosinofil fasciitt: Økt risiko for hematologisk malignitet og solide tumorer foreligger (Haddad H, Hematol Oncol Stem Cell Ter, 2014). Relasjon til sjekkpunkthemmere i kreftbehandling er også sett.
Erythromelalgi. Malignitet påvises hos ca. 10%. Disse er oftest astrocytomer, koloncancer eller brystkreft.
Hypertrofisk osteoartropati. Forekomsten ved lungekreft varierer mellom ca. 1-17% (Izumi M, 2010). Genetiske former som ikke er kreft- eller lungerelatert finnes også (Lui Q, 2023).
IgA vaskulitt / Henoch-Schönlein: Kan være debutsymptom ved solide tumorer hos voksne/eldre personer (ca. pulm, nyrecancer, prostata-ca.) (Podjasek J.O., Acta Derm Venerol, 2012)
Kryoglobulinemi: Type I (monoklonal IgM kappa) og tymom.
Leukocytoklastisk vaskulitt: Debut, spesielt etter 50-års alder, kan være malignitet-assosiert (ca. 3,5%). IgA nedslag (immunhistologi) utelukker ikke malignitet (Podjasek JO, 2012).
Migrerende artritt. Semi-migrerende, spesielt hos barn (Barre A, 2025).
Palmar fasciitt: Pasienter med rask utvikling av fleksjonskontrakturer og som har artritt i håndledd og store ledd har økt kreftrisiko (Alexandroff AB, 2003). Kan ha “Groove sign” – hvilket innebærer forsenkning av huden over overfladiske årer (venene fanges i fibrotisk vev) – særlig på håndbaken når armen holdes over hjertenivå. Noen får endret konisistens i hender (Wooden hands”), men finger- og tå-pulpa ikke angripes. Noen kaller dette “Palmar fasciitt og artritt syndrom”. God effekt av kortikosteroider forventes. Tilstanden er rapportert ved ca. ovari, endometrialt adenokarsinom, hepatocelluIært karsinom, ca. ventriculi, ca. renis, ca. mamma, ca. prostata, kronisk lymfatisk leukemi og småcellet lungekarsinom. Revmatiske manifestasjoner kan opptre måneder for symptomer på malign sykdom (Sheely. Clin Rheumatol 2007, Krishna K. Clin Rheumatol 2011 ; Yogarajoh M, J Royal Soc Med, 2008).
Pannikulitt: pankreaskreft, ofte med polyartritt/subkutane knuter/noduli (Wang P, 2021).
Polyartritt (akutt asymmetrisk) hos eldre personer som ofte sparer småleddene.
Raynauds fenomen: Metastaserende malignt melanom, ca. ovari og ca. testis. Malignitetassosiert Raynauds er ofte akutt innsettende og sees ved alder > 40 år. Raynauds fenomen og digitale ulcera rapportert som debutmanifestasjoner ved residiv av cancer mamma (Decross AJ, Am J Med 1992). Ved kreftbehandling kan kjemoterapi utløse Raynauds fenomen.
Refleks dystrofi (algodystrofi): Obs! ca. ovari.
Revmatoid artritt: Lungecancer og lymfom. Kan skyldes inflammasjon og cytostatika-behandling. Feltys syndrom øker risikoen for non-Hodgkins lymfom. RA og monoklonal gammopati: Paraproteinemi gir stor risiko for cancerutvikling – spesielt ved IgA lambda. (De Cock D, Vest Practice and Res Clin Rheum, 2018, Klein A, Hematol Onkol, 2018)
RS3PE (remitting seronegative symmetrical synovitis with pitting edema): Opp til 30% er kreft-assosiert. Forskjellig malignitet. Ødemene kan være betinget i vaskulær endothelial vekstfaktor. Symptomene kan respondere godt på prednisolon, men dårlig respons bør øke mistanken om bakenforliggende malignitet (Karmacharya P, Clin Exp Rheum, 2016).
Schnitzlers syndrom. Omtrent 15-20% vil utvikle en lymfoproliferativ sykdom, oftest Waldenstöms makroglobulinemi (Sokumbi O, 2012).
Sjøgrens syndrom: MALT-lymfom / non-Hodgkins lymfom. Klinisk eller laboratoriemessige suspekte endring i forløpet bør tilsi nærmere utredning (Reksten TR, 2014).
Skjelettsmerter. Spesielt nattlige skjelettsmerter.
Stiff person syndrome. Nevrologisk sykdom som i noen tilfeller er assosiert med ulike typer kreft (Peng Y, 2023).
Sweet’s syndrom: Ca. 20 % assosiert med cancer (Iymfoproliferative). Alle reagerer på kortikosteroider. Oftest akutt myelogen leukemi og andre hematologiske, men også solide tumorer forekommer. Obs! Det virker som om de responderer på behandling, men svært ofte gjenstår mikrometastaser (Heath MS, Front Immunol, 2019).
Systemisk Sklerose med fibroserende alveolitt: Gir antakelig litt økt risiko for cancer pulm, ca. mamma, cervix cancer og hudkreft (Szekanecz E, Autoimmunity Rev, 2012). Pasienter med antistoffet RNA-polymerase III er disponert for malignitet.
Vaskulitt: Uvanlig forløp kan tale for malignitet: Vanskelig klassifikasjon, negativ serologi, tidligere cancer, brennende følelse, evt. kløe. Lymfoproliferative og myeloproliferative sykdommer.
- Typer vaskulitt rapportert sammen med malign sykdom: systemisk nekrotiserende vaskulitt, granulomatøs vaskulitt, hypersensitivitets vaskulitt, erythema nodosum, IgA vaskulitt/Henoch-Schönleins purpura, leukocytoklastisk vaskulitt, urtikariell vaskulitt og PAN. Kan også sees ved solide tumorer (urinveier 40%, lunger 27%, GI-kanalen 27%).
- Også sjekkpunkthemmere som brukes i kreftbehandling kan utløse vaskulitt (Daxini A, Clin Rheum, 2018
Litteratur: Gran JT. Tidsskr Nor Lægefor, 1997; Agha A, Curr Rheum Rep 2012
Retningslinjer
Sebbag E, 2024 (EULAR: Artritt-behandling ved tidligere kreft)
Kostine M, 2020 (EULAR, Sjekkpunkthemmere)
Sepriano A, 2020 (EULAR, sikkerhet ved DMARDs og biologiske legemidler)
Litteratur
Bernal-Bello D, 2025 (Malignitet ved autoimmune sykdommer)
Shi X, 2024 (Autoimmune sykdommer og non-Hodgkins lymfom)
Russel MD, 2023 (JAK-inhibitorer og kreft)
Kostine M, 2021 (Sjekkpunkthemmere)
Szekanecz, Z, 2020 (Malignitet og revmatiske sykdommer)
Cappelli CL, 2020 (Malignitet og revmatiske sykdommer)
Wong PKK, 2018 (Behandling av pasienter med tidligere kreft)
Pekuska AB, 2016 (Barn med lymfom)
Manger B, 2014 (Paraneoplastiske revmatiske symptomer)
Teksten er skrevet og gjennomgått av forfatterne. I bearbeidelsen/redigeringen er kunstig intelligens brukt i noen avsnitt.
