ARTRITT (REV 006-REV 020)
12 Leddvæske: prøvetaking og mikroskopering, leddvæskediagnostikk, leddvæske ved krystallartritt (REV 012, REV 069)
Leddvæske -Prøvetaking og Mikroskopering
Jan Tore Gran and Øyvind Palm
Prosedyrekoder: Leddpunksjon/artrocentese (klikk for å spesifisere ledd:) TN_10. UL veiledet leddpunksjon: NXA10K. Mikroskopi av leddvæske: NXFT05. Leddvæskeundersøkelse i polarisert lys: NXFT05
I dette kapitlet:
- Leddpunksjon og leddvæskeaspirasjon
- Makroskopisk vurdering av leddvæske
- Leddvæskediagnostikk ved krystallartritt
- Polarisasjonsmikroskopi
- Ultralydundersøkelse
- Dual-energy-CT (DECT)
- Andre metoder
- Oppbevaring av leddvæske
- Oppsummerende tabeller
- Litteratur
Leddpunksjon og leddvæskeaspirasjon: Indikasjoner og diagnostisk verdi
Formålet med leddpunksjon og aspirasjon av leddvæske er både diagnostisk og terapeutisk. I tillegg er det gunstig å redusere trykket i et væskefylt ledd. Leddvæskeanalyse er obligatorisk ved mistanke om infeksiøs/septisk artritt (bakteriologisk dyrkning, polymerasekjedereaksjon/PCR og leukocytt-telling) og for diagnostisering av krystall-artritter ved bruk av polarisasjonsmikroskop (se REV 069 nedenfor) for påvisning av dobbeltbrytende krystaller.
Makroskopisk vurdering av leddvæske
Umiddelbar makroskopisk vurdering av aspirert leddvæske inkluderer analyse av viskositet og farge. Redusert viskositet (vannaktig) er typisk ved artritt, mens økt viskositet (seig) sees ved artrose.
- Hemartros (blodig leddvæske): Kan skyldes traumer, pigmentert villonodulær synovitt, blodsykdommer, antikoagulantia og malignitet
- Lett uklar (blakket) leddvæske: Vanligvis assosiert med inflammatorisk artritt.
- Klar, gul og viskøs leddvæske: Typisk for artrose.
- Uttalt uklar (strengt blakket), gul-hvit leddvæske::Karakteristisk for septisk / infeksiøs artritt og krystallartitt (urinsyregikt, kondrokalsinose/pyrofosfat-artritt) kjennetegnes ved strekt blakket, gul -hvit væske.
| Tabellen gir en oversikt over forventede funn ved ulike leddsykdommer (Horowitz DL et al, 2011) |
|||||||||
| Artritt-diagnose | Farge | Transparens | Viskositet | Leukocytter (x10^9/L) | Polymorfo-nukleære celler, antall (%) | Gram-farging | Dyrkning | PCR-test | Krystaller |
| Normal | Klar/strå-gul | Transparent | Høy | <0,20 | <25 | Negativ | Negativ | Negativ | Negativ |
| Non-inflammatorisk | Strå-gul | Transparent | Høy/seig | 0,2-2 | <25 | Negativ | Negativ | Negativ | Negativ |
| Inflammatorisk krystall-artritt | gul | Blakket | Lav/tynn | 2-100 | >50 | Negativ | Negativ | Negativ | Positiv |
| Inflammatorisk non-krystallisk | Gul | Blakket | Lav | 3-100 | >50 | Negativ | Negativ | Negativ | negativ |
| Infeksiøs: Borrelia | Gul | Blaket | Lav | 3-100 (gj.snitt 25.) | >50 | Negativ | Negativ | Positiv (85%) | Negativ |
| Infeksiøs: Gonokokker | Gul | Blakket/ugjennomsiktig | Lav | 34-68 | >75 | Variabel (<50%) | Positiv (25-70%) | Positiv (>75%) | Negativ |
| Infeksiøs: Non-gonokokk | Gul-grønn | Ugjennomsiktig | Veldig lav | >50 (>100 er mer spesifikk) | >75 | Positiv (60-80%) | Positiv (>90%) | – | Negativ (hvis ikke ko-eksistens) |
Leddvæskediagnostikk ved krystallartritt
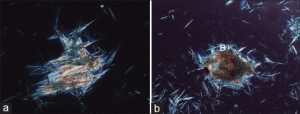
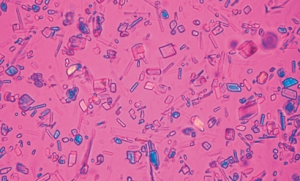
Mikroskopisk undersøkelse av leddvæske med polarisasjonsfilter er en sensitiv og spesifikk metode for diagnostisering av urinsyregikt (urinsyrekrystaller) og pyrofosfat-artritt / kondrokalsinose/pseudogikt (kalsiumpyrofosfat dihydrat-krystaller). Urinsyrekrystaller har en nåleformet morfologi og negativ dobbeltbrytning, mens pyrofosfatkrystaller er rombeformede og har positiv dobbeltbrytning.
Metoder for krystallidentifikasjon
Polarisasjonsmikroskopi
- “Gullstandard” for diagnostisering av urinsyregikt og kondrokalsinose.
- Resultatene kan være avhengig av undersøker.
Historie. McCarty og kolleger innførte leddvæskeundersøkelse med polarisert lys i 1969, og metoden har holdt seg som “gullstandard” for diagnostisering av urinsyregikt og kondrokalsinose. Imidlertid har mange rapporter vist at resultatene er avhengig av undersøker (variabel inter-rater reliabilitet) og ikke optimal i en klinisk setting (McGill NW, 1991).
Ultralydundersøkelse
- Kan påvise urat- og pyrofosfatkrystaller ved visualisering av en “dobbeltkontur” i leddet.
- Høy sensitivitet, men kan være lavere ved tidlig sykdomsforløp.
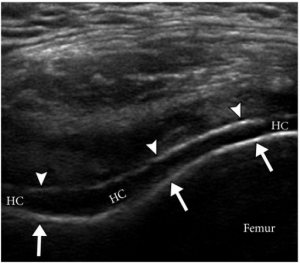
Kan påvise urat- og pyrofosfatkrystaller ved visualisering av en “dobbeltkontur” i leddet. Ultralyd-undersøkelse er dermed nyttig I diagnostisering av både urinsyre- og kondrokalsinose-krystaller og inngår i ACR/EULAR anbefalinger for diagnostikk (Neogi T, 2015). Krystallene reflekterer ultralydbølger, slik at det oppstår en karakteristisk dobbeltkontur i leddet. Metodens sensitivitet sammenlignet med mikroskopi i polarisert lys er over 90%, men sensitiviteten er lavere, spesielt ved kort sykdomsforløp. Blant pasienter med sykdom i mindre enn to år er sensitiviteten under 50% (Ogdie A, 2017).
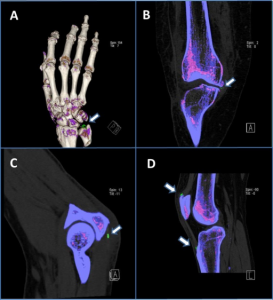
Dual-energy-CT (DECT)
- Kan differensiere mellom urat- og pyrofosfatkrystaller ved bruk av to ulike energispektre.
- Muliggjør tredimensjonal fremstilling og kvantifisering av krystaller.
- Begrenset tilgjengelighet og risiko for falske positive funn.
DECT benytter to ulike energier (80 eller 100 kV og 140 kV) med forskjellig vinkling, noe som fremstiller materialer med ulik tetthet. Både urinsyre- og pyrofosfatkrystaller kan påvises og fremstilles tredimensjonalt i ulike farger, på alle lokalisasjoner og med mulighet for kvantifisering av mengden krystaller. Metoden begrenses av redusert tilgjengelighet og mulige falsk positive funn, blant annet ved gonartrose (Bongartz T, 2015).
Andre metoder
Raman spektroskopi (RS): Gir 100 % nøyaktighet ved måling av kjemisk sammensetning, men klarer ikke og skille mellom intra og ekstra cellulære krystaller (Rosenthal AG, 2016).
Linse-løse mikroskop: Kan produsere hologrammer og visualisere krystaller med polarisasjonsfilter. (Zgang , 2016).
Oppbevaring av leddvæske.
- Ideelt sett bør leddvæsken undersøkes umiddelbart etter aspirasjon.
- Krystaller er relativt stabile (1-3 dager), men celler degenererer over tid.
- Antikoagulantia er ikke nødvendig.
- Sentrifugering kan konsentrere celler i væske med lavt celleinnhold.
(Zell M, John FitzGerald, 2019)
Oppsummerende om leddvæskeundersøkelse
Makroskopisk vurdering
| Parameter | Beskrivelse / Tolkning |
|---|---|
| Farge og klarhet | – Klar og strågul: Normal eller ikke-inflammatorisk (f. eks. artrose). – Grumsete / uklar: Inflammatorisk (f. eks. revmatoid artritt (RA)). – Purulent (tykk, gul-grønn): Infeksiøs artritt. |
| Viskositet | – Normal synovialvæske er seig og trådtrekkende. – Redusert viskositet ved inflammasjon (nedbrytning av hyaluronsyre). |
| Volum | Økt ved inflammasjon eller hydrops. |
Cytologisk analyse
| Parameter | Beskrivelse / Tolkning |
|---|---|
| Leukocytt-tall (WBC) | – < 2000/mm³: Ikke-inflammatorisk (artrose). – 2 000–50 000/mm³: Inflammatorisk (RA, urinsyregikt, SLE). – > 50 000/mm³: Tyder sterkt på infeksjon (infeksiøs/septisk artritt). |
| Differensialtelling | – Nøytrofildominans: Infeksiøs eller inflammatorisk artritt. – Mononukleære celler: Ikke-inflammatorisk eller kronisk sykdom. |
| Erytrocytter (RBC) | Kan forekomme ved traume, hemartrose eller etter punksjon. |
Mikroskopisk krystallundersøkelse
| Parameter | Beskrivelse / Tolkning |
|---|---|
| Polarisasjonsmikroskopi | Utføres for å påvise krystaller: |
| -Uratkrystaller (nåleformede, negativ dobbeltbrytning) | → Urinsyregikt |
| -Kalsiumpyrofosfat-krystaller (rombiske, positiv dobbeltbrytning) | → Kondrokalsinose/pseudogikt |
| -Andre krystaller (hydroksyapatitt, kolesterol, oksalat) | Sjeldnere årsaker til artropati. |
Mikrobiologiske analyser
| Test | Beskrivelse / Bruksområde |
|---|---|
| Gram-farging | Rask identifikasjon av bakterier. |
| Dyrkning (bakteriell, mykobakteriell, sopp) | Gullstandard for å bekrefte infeksiøs/septisk artritt. |
| PCR/DNA-analyse | Øker sensitiviteten, spesielt ved atypiske infeksjoner (f. eks. borreliose, TBc). |
Biokjemiske analyser
| Parameter | Beskrivelse / Bruksområde |
|---|---|
| Glukose | Redusert ved bakterielle infeksjoner og RA. |
| Protein | Økt ved inflammasjon. |
| LD (laktatdehydrogenase) | Økt ved inflammasjon og infeksjon. |
| Uratnivå | Kan være forhøyet ved urinsyregikt (sjeldent målt direkte i væsken). |
Supplerende analyser (ved spesifikke mistanker)
| Analyse | Bruksområde |
|---|---|
| Cytologi (tumorceller) | Mistanke om malignitet/metastase. |
| ANA, anti-CCP, RF i væsken | Ved usikker autoimmun årsak (sjeldent nødvendig – oftest serumprøver). |
| Crystal clearance-test | Ved uklare krystallsykdommer. |
