ARTRITT (REV 006-REV 020)
32 Psoriasisartritt (PsA) (REV 006)
Psoriasisartritt
Øyvind Palm and Jan Tore Gran
Diagnosekoder ICD-10: L40.5 (psoriasis med artropati M07.0- M07.3, M09.0), M07.1 (mutilans, L40.5), M07.2 (psoriasis-spondylitt, L40.5), M07.3 (psoriasisartritt, andre, L40.5), M09 (Juvenil psoriasisartritt), L40 psoriasis (hudsykdom)
Prosedyrekoder: Leddpunksjon/artrocentese (klikk for å spesifisere ledd:) TN_10. UL veiledet leddpunksjon: NXA10K. Mikroskopi av leddvæske: NXFT05.
ATC koder: Behandling med immunsuppressive legemidler: L04A. etanercept: L04AB01, adalimumab: L04AB04, triamcinolon (Lederspan): H02AB08, betametason (Celeston Chronodose): H02AB04, rituksimab: L01XC02, abatacept: L04AA24, tocilizumab: L04AC07, infliksimab: L04AB02, ustekinumab: L04AC05
Nøkkelord ved journalskriving ved psoriasisartritt
Diagnosen er basert på.
- Perifer artritt (lokalisering, DIP, store ledd, oligoartikulær, mutilans, asymmetrisk)
- Aksial artritt (inflammatorisk ryggsmerte, bildediagnostikk, HLA-B27)
- Daktylitt
- Entesitt
- Kjent psoriasis, ev psoriasis blant første eller andregrads slektninger
- Neglepsoriasis
- SR og CRP
- Fravær av RF og anti-CCP / ACPA
- Bildediagnostiske funn
Hensikten med konsultasjonen
Innhold
- Definisjon
- Psoriasisartritt
- Hudsykdommen psoriasis
- Epidemiologi
- Historikk
- Patogenese
- Symptomer (hud, ledd, aksial manifestasjon, subklasser, daktylitt, entesitt)
- Utredning
- Klassifikasjonskriterier
- Differensialdiagnoser
- Komorbiditet
- Sykdomsscore
- Svangerskap
- Behandling
- Prognose
- Retningslinjer
- Litteratur
Definisjon
Psoriasisartritt (PsA) er en kronisk inflammatorisk revmatisk sykdom hos ca. 20 % av pasienter med psoriasis (Alinaghi F, 2019. Typisk er ledd- og aksial inflammasjon (spondyloartritt), entesitt, daktylitt og hud- eller neglepsoriasis.
PsA regnes er en del av spondyloartritt-spekteret og kan ligne aksial spondyloartritt/ankyloserende spondylitt (Bekhterevs sykdom). Noen har like genetiske assosiasjoner (HLA-B27, IL-23R) og overlappende immunologiske mekanismer.
PsA varierer klinisk fra mild, oligoartikulær artritt til aggressiv erosiv polyartritt med betydelig funksjonstap. Ubehandlet ses ofte leddskader, redusert livskvalitet og økt kardiovaskulær risiko (Tiwari V, 2024).
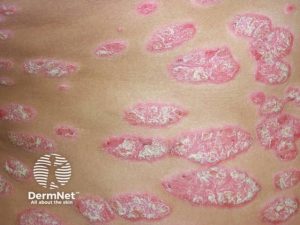
Hudsykdommen psoriasis
Psoriasis er er en autoimmun hudsykdom som rammer 2-4% av befolkningen. Genetisk disposisjon er vanlig. Noen medikamenter som betablokkere, kortikosteroider, hydroksyklorokin (Plaquenil),NSAIDs. klorokin og litium kan forverre symptomene, mens soleksponering kan være gunstig.
Tabell. Kliniske former, utløsende faktorer og behandling.
| Aspekt | Beskrivelse | Referanser |
|---|---|---|
| Definisjon | Psoriasis er en kronisk, inflammatorisk autoimmun hudsykdom som rammer 2–4 % av befolkningen. | — |
| Etiologi og risikofaktorer | Sykdommen har ofte arvelig disposisjon. Enkelte legemidler kan forverre psoriasis, inkludert betablokkere, kortikosteroider, hydroksyklorokin (Plaquenil), NSAIDs, klorokin og litium. Soleksponering virker ofte gunstig. | (Nair PA, 2021). |
| Vanlige kliniske former | ||
| – Plakkpsoriasis | Vanligst forekommende form. Velavgrensede erythematøse plakk med sølvgrå, skjellende overflate. | — |
| – Guttat psoriasis | Dråpeformede lesjoner, ofte etter streptokokkinfeksjon og hos yngre pasienter. | — |
| – Pustuløs psoriasis | Kan være lokalisert (palmoplantaris) eller generalisert. Kjennetegnes av sterile pustler. | — |
| – Erythroderm psoriasis | Alvorlig form med diffus erythem og avskalling over store hudområder, kan gi systemiske symptomer. | — |
| – Neglepsoriasis | Pitting, oljeflekker, subungual hyperkeratose og negledystrofi. Ofte assosiert med psoriasisartritt. | — |
| – Invers psoriasis | Glatt, rød og skarpt avgrenset hudaffeksjon i hudfolder (armhuler, under mammae, i lysker og interglutealt). | — |
| – Sebopsoriasis | Angriper seboreiske områder: hodebunn, panne, bak ører og nasolabialt. | — |
| – Oral psoriasis | Tungefissurer og erythematøse lesjoner i munnslimhinnen. | — |
| – Okulær psoriasis | Kan affisere øyelokk, konjunktiva og cornea. | (Nair PA, 2021). |
| Differensialdiagnoser | Eksem, seboréisk dermatitt, pityriasis rosea, mykosis fungoides, sekundær syfilis. | — |
| Diagnostisk vurdering | Psoriasis Area Severity Index (PASI) brukes for å vurdere alvorlighetsgrad og behandlingseffekt. | (Sbidian E, 2023) |
| Behandling – prinsipper | Behandling avhenger av alvorlighetsgrad og utbredelse. Fremskritt i moderne terapi har betydelig forbedret prognosen. | (Sbidian E, 2023) |
| Behandling – mild/moderat sykdom | Lokal behandling med fuktighetsgivende midler, keratolytika, vitamin D-analoger, kortikosteroider, ev. kulltjærepreparater. | — |
| Behandling – alvorlig sykdom | Systemisk behandling med metotreksat eller biologiske legemidler (f. eks. TNF-, IL-17-, IL-23-hemmere). | (Nair PA, 2021 ; Sbidian E, 2023) |
| Effekt på psoriasisartritt-risiko | Det er mulig at systemisk immunsuppressiv behandling kan redusere risikoen for utvikling av psoriasisartritt, men dokumentasjonen er foreløpig utilstrekkelig. | (Lopez-Medina C, 2024). |
Epidemiologi av psoriasisartritt
Psoriasisartritt (PsA) forekommer hos omtrent 0,1–1 % av befolkningen (prevalens) og hos ca. 20 % av pasienter med psoriasis (Alinaghi F, 2019). I Norge er prevalensen estimert til 0,1-0,2 % (1-2 pr 1 000 personer). Imidlertid kan kvinner ha høyere sykdomsaktivitet enn menn (Losinska K, 2024).
Sykdommen debuterer oftest i 30–50-årsalderen og diagnostiseres vanligst i aldersgruppen 40-59 år (Madland TM, 2005) med tilnærmet lik kjønnsfordeling.
Hos 70–80 % av pasientene begynner hudsymptomene først. Sjeldnere debuterer artritten samtidig eller forut for psoriasis.
Risikofaktorer for PsA inkluderer neglepsoriasis, alvorlig hudsykdom, familiær belastning, fedme og traumer (Koebner-fenomenet).
PsA kan starte i barnealder (juvenil psoriasisartritt), men er sjeldnere enn klassisk barneleddgikt (JIA).
Historikk
Sammenhengen mellom psoriasis og artritt ble beskrevet av den britiske hudlegen Thomas Batemant i 1813 og senere mer detaljert av den franske dermatologen Jean-Louis Alibert (1768–1837) i 1818. En annen fransk lege, Pierre Bazin, introduserte betegnelsen psoriasis arthritique i 1860 og regnes dermed som den første som systematisk skilte denne tilstanden fra andre artritter.
På midten av 1900-tallet beskrev Moll og Wright (Leeds, England) fem kliniske undergrupper av psoriasisartritt; distal interfalangeal artritt, asymmetrisk oligoartritt, symmetrisk polyartritt, spondylitt og artritt mutilans. Det var et arbeid som la grunnlaget for moderne forståelse av sykdommens kliniske mangfold (Moll JMH, 1973).
I 1964 ble PsA anerkjent som en egen diagnose, adskilt fra revmatoid artritt (RA) i American College of Rheumatology (ACR) sin klassifikasjon av revmatiske sykdommer. Senere ble psoriasisartritt innlemmet i gruppen spondyloartritter (SpA) på bakgrunn av fellestrekk som entesitt, aksial affeksjon, familiær opphopning og assosiasjon med HLA-B27.
I 2006 ble CASPAR-kriteriene (Classification Criteria for Psoriatic Arthritis) etablert som et internasjonalt anerkjent verktøy for klassifikasjon av psoriasisartritt (Taylor W, 2006). Disse kriteriene har siden vært mye brukt både i klinisk praksis og forskning og muliggjort en mer presis og standardisert diagnostikk av sykdommen.
Inndeling av spondyloartritt 1. Bekhterevs sykdom/ankyloserende spondylitt. 2. Psoriasisartritt (spondylitt, polyartritt, oligoartritt, monoartritt). 3. Artritt ved kronisk inflammatorisk tarmsykdom (Ulcerøs kolitt, Crohns sykdom). 4 Reaktiv artritt. 5. Udifferensiert spondyloartritt.
Psoriasisartritt utgjør mer enn 50% av alle spondyloartritter (Haglund E, 2010).
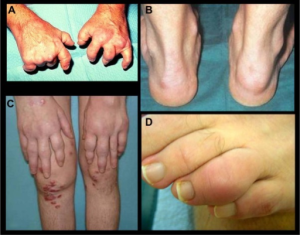
Patogenese
Ved PsA er både det medfødte og adaptive immunsystemet er involvert. Viktige patogene mekanismer omfatter aktivering av T-celler (særlig Th17 og Th1) (Azuaga AB, 2023) og produksjon av proinflammatoriske cytokiner som TNF-α, IL-17, IL-12/23 og IL-23.
Inflammasjonen rammer ledd, enteser, hud og negler. Entesitt antas å være en primær affeksjon som kan utløse sekundær synovitt og skjelettforandringer. Genetiske faktorer (HLA-B27, HLA-C*06:02), miljøfaktorer (infeksjoner, traumer, røyking) og dysbiose i tarmmikrobiota kan bidra til sykdomsutviklingen. En norsk tvilling-studie viste at 66% av eneggede tvillinger var konkordante for psoriasis og dermed hadde risiko for PsA. Samtidig indikerer studien at psoriasis skyldes 34% ikke-genetiske forhold (Grijbovski AM, 2007). HLA-B27 forekommer særlig ved aksiale manifestasjoner (ca. 50%), men sjeldnere enn ved ankyloserende spondylitt/Bekhterevs (>95%) og reaktiv artritt.
Mekanisk stress: En hypotese er at mekanisk stress eller mikroskade i enteser kan initiere en inflammatorisk tilstand og gi PsA (McGonagle D, 2019). Andre har også funnet tegn til at fysisk / mekanisk belastning eller traume kan indusere kan osteofytt-formasjon ved entesitt (dypt Köbner fenomen) (Simon D, 2016; Azuaga AB, 2023).
Infeksjoner: En kontrollert studie (case-control design) fant at infeksjoner som krevde antibiotikabehandling økte risikoen for utvikling av PsA (Eder L, 2011).
Røking: Det er funnet en invers assosiasjon med røking (Eder L, 2011).
Symptomer
Psoriasisartritt (PsA) har flere ulike manifestasjoner som kan opptre samtidig eller variere over tid hos samme pasient. De viktigste manifestasjonene inkluderer artritt, entesitt, daktylitt, aksial affeksjon, hud- og negleforandringer.
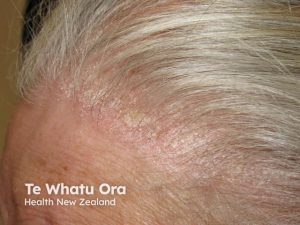
Hudsymptomer
Hudforandringer ved psoriasis omfatter erythematøse, skjellende plakk, typisk lokalisert til ekstensorsidene av albuer og knær, men også interglutealt, ved umbilicus, palmoplantart og på andre områder. Negleaffeksjon er vanlig.
Pasienter med utbredt psoriasis (≥3 lokalisasjoner) har høyere risiko for å utvikle PsA (relativ risiko 2,24) sammenlignet med mer moderate tilfeller (Wilson FC, 2009). Neglepitting og uveitt er også assosiert med økt risiko (Edel L, 2016).
I gjennomsnitt går det omtrent syv år mellom debut av psoriasis og utvikling av PsA, men variasjonen er stor (Scher JU, 2019).
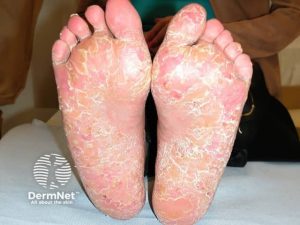
En spesiell form, pustuløs palmoplantar psoriasis (PPP-syndromet), kjennetegnes ved pustuløse utslett i håndflater og fotsåler. Enkelte forfattere skiller denne tilstanden fra vanlig psoriasis (Freitas E, 2020).
Negle-pitting. Forekomsten ved psoriasis er 40%, mens ved PsA påvises forandringene hos 80% (Haroon, 2013). En anatomisk likhet mellom negleapparatet og senefester i bensubstans kan være årsaken til en assosiasjon mellom neglepsoriasis og entesopatier ved psoriasis artritt.
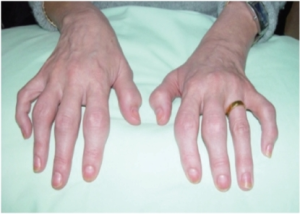
Leddsymptomer
Artritt ved PsA innebærer inflammasjon i synovialmembranen (synovitt) med påfølgende leddhevelse (hydrops), økt varme over ledd og ofte redusert bevegelighet. Tilstanden er mer enn bare leddsmerter (artralgi). Artrittforløpet kan være både akutt og snikende, og sykdommen kan lett overses uten målrettet anamnese og klinisk undersøkelse.
Pasienter med psoriasis bør derfor aktivt kartlegges for leddsmerter, hevelser, stivhet i ledd og rygg i mer enn 30 minutter om morgenen (se målrettet anamnese for inflammatorisk ryggsmerte) og tegn til daktylitt.
Artritt ved PsA viser stor variasjon i både utbredelse og mønster (Moll JM, 1973). Den kan affisere ett eller få ledd (mono- eller oligoartritt) eller utvikle seg til en mer utbredt polyartritt. Artrittmønsteret er ofte asymmetrisk, i motsetning til den typisk symmetriske affeksjonen som ses ved RA. Distale interfalangealledd (DIP-ledd) angripes ofte, spesielt hos pasienter med samtidig neglepsoriasis. Ved klinisk undersøkelse kan man finne varme, hevelse og smerte ved passiv og aktiv bevegelse, og etter hvert utvikling av ledd-deformiteter eller erosjoner ved utilstrekkelig kontrollert inflammasjon.
Aksial psoriasisartritt (spondylitt)
Aksial affeksjon kan forekomme isolert, men dette er relativt sjelden (2-5%). Hos pasienter med perifer artritt utvikler omkring 15 % aksial sykdom i løpet av ti år, og ved langvarig sykdom kan den kumulative insidensen stige til opptil 75 % (Chandran V, 2010).
Aksial PsA karakteriseres ved sakroiliitt og syndesmofytter i columna, ofte asymmetrisk og med preferanse for cervicalcolumna. I motsetning til ankyloserende spondylitt) er unilateral sakroiliitt hyppig. HLA-B27 påvises hos 14-44% (Poddubnyy D, 2021).
Forskjeller mellom aksial PsA og ankyloserende spondylitt er vist i tabellen nedenfor (modifisert ette (Poddubnyy D, 2021):
| Kjennetegn | AxSpA (f.eks. ankyloserende spondylitt) | Aksial psoriasisartritt (PsA) |
|---|---|---|
| Demografi | Vanligere hos menn, lav alder ved debut. | Omtrent lik forekomst hos menn og kvinner, noe høyere debutalder. |
| Bildediagnostikk | Symmetrisk sakroiliitt, klassiske syndesmofytter, hyppig fusjon av lumbale fascettledd. | Hyppigere affeksjon i cervicalcolumna, asymmetrisk sakroiliitt, mindre symmetriske syndesmofytter, paravertebrale ossifikasjoner. |
| Genetikk | HLA-B27 positiv hos >90 %. | 14–44 % HLA-B27 positive, oftere assosiert med HLA-B08 og HLA-B38 |
| Behandlingsrespons | NSAIDs, TNF-α- og IL-17-hemmere effektive; ikke sikker effekt av IL-23-hemmere. | Begrenset evidens; respons på TNF-α, IL-17 (secukinumab), IL-23 (guselkumab) og IL-12/23-hemmere (ustekinumab) rapportert. |
Subklasser av psoriasisartritt (Moll & Wright, 1973)
Moll og Wright beskrev fem kliniske undergrupper av PsA basert på leddmønster og sykdomsforløp (Moll JM, 1973). Disse brukes fremdeles i klinisk praksis og forskning.
| Subklasse | Kliniske kjennetegn og behandling | Referanser |
|---|---|---|
| DIP-leddsartritt | Affiserer hovedsakelig fingrenes DIP-ledd; vanskelig å skille fra artrose klinisk og radiologisk. Forekommer hos ca. 5 % av PsA-pasienter. Nesten alle har negleforandringer. Behandles med analgetika og NSAIDs. | (Moll JM, 1973). |
| Arthritis mutilans | Sjeldent, men alvorlig destruktiv form med benresorpsjon og deformiteter («pencil-in-cup», teleskopfingre/tær). Behandles med NSAIDs, csDMARD og biologiske legemidler; kirurgi kan bedre funksjon. | (Laasonen L, 2020). |
| Oligoartritt | Nest vanligst etter symmetrisk polyartritt. Færre enn fem affiserte ledd (22,9–40 %), monoartritt hos 5,8–15 %. Behandles med NSAIDs, eventuelt intraartikulære kortikosteroider, csDMARDs (ofte metotreksat) eller bDMARDs ved høy sykdomsaktivitet. | (Madland TM, 2005; Kasiem FR, 2021). |
| Symmetrisk polyartritt | Hyppigste form (23–68,6 %). Ligner revmatoid artritt, men uten RF og anti-CCP. Behandles som RA. | (Madland TM, 2005; Kasiem FR, 2021). |
| Spondylitt / aksial artritt | Affiserer iliosakralledd og sjeldnere columna. Radiologisk distinkt fra ankyloserende spondylitt/Bekhterevs. Behandles med fysioterapi, NSAIDs og biologiske legemidler. | (Madland TM, 2005) |
Over tid kan pasienter skifte subklasse f. eks. fra oligo- til polyartritt eller utvikle pustuløs palmoplantar psoriasis (Freitas E, 2020). En rekke ekstraartikulære manifestasjoner bør også vurderes i henhold til klassifikasjonskriteriene (vennligst se eget avsnitt nedenfor).
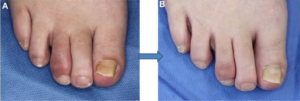
Daktylitt forekomsten ved PsA er ca. 10% ved PsA-diagnose Kasiem FR, 2021) og 40-50% senere i forløpet. typisk er fortykkelse i hele finger eller tås lengde og tegn til fleksorsensesynovitt eller tendovaginitt ved ultralyd- eller MR-undersøkelse. Oftest angripes 3. og 4. tå, men ses også i fingre (Gladman DD, 2013).
Entesitt kan lett overses, men kan påvises (klinisk, ultralyd eller MR) hos ca. 10% ved diagnose (Kasiem FR, 2021) og 30-50% i forløpet. Affeksjon av plantarfascien, Akilles-sener, peripatellært, i bekken, epikondylært og ved supraspinatus-senen er vanlig.
Utredning
Hudforandringer ved PsA trenger ikke å være omfattende. Ved utredning av alle typer seronegativ artritt er det viktig å avklare om pasienten har udiagnostisert psoriasis. Sjekk typiske steder som øregang, hodebunn, navle og negler. Unntaksvis kan diagnosen PsA stilles hos pasienter uten psoriasis, forutsatt at artrittmønsteret er typisk for PsA og det foreligger psoriasis i nær familie (se CASPAR-kriteriene nedenfor).
Psoriasisartritt starter oftest gradvis og være vanskelig å diagnostisere i et tidlig stadium. En ganske plutselig og akutt start er mer uvanlig. Forsinket diagnose med seks måneder mellom symptomer og første besøk hos revmatolog kan imidlertid gi dårligere behandlingseffekt og prognose (Snoeck Henkemans SVJ, 2024; Haroon M, 2015).
Anamnese og klinisk undersøkelse
Pasienter med psoriasis bør alltid kartlegges for tegn på inflammasjon i ledd og enteser. Viktige spørsmål i en målrettet anamnese inkluderer forekomst av ledd- og ryggsmerter, hovne ledd, daktylitt, entesitt, stivhet i mer enn 30 minutter om morgenen og smerter i rygg eller ledd.
Laboratorieprøver.
Rutineprøver kan omfatte CRP, SR, Hb, leukocytter med differensialtellinger, trombocytter, lever-, nyre- og thyreoidea-funksjonsprøver. Urin stiks.
CRP og senkningsreaksjon (SR) er forhøyet hos ca. 40%.
PsA er ikke assosiert med autoantistoffer (“seronegativ sykdom”) i motsetning til revmatoid artritt (RA). Anti-CCP og ANA kan imidlertid være aktuelle differensialdiagnostisk.
I forskning er biomarkørene OPG, MMP-3, CPII:C2C ratio (Chandran V, 2010) og CXCL10 (Abji F, 2016) brukt for å skille PsA fra utelukkende hudmanifestasjon. Foreløpig er ingen spesifikke antistoffer eller biomarkører tilgjengelige for rutinemessig bruk.
| Blodprøver ved psoriasisartritt | Hensikt | Typisk funn ved PsA |
|---|---|---|
| Revmatoid faktor (RF) | Utelukke revmatoid artritt (RA) | Negativ |
| Anti-CCP | Utelukke revmatoid artritt (RA) | Negativ |
| CRP / SR | Vurdere generell inflammatorisk aktivitet | Ofte normal (kan være forhøyet) |
| HLA-B27 | Vurdere aksial affeksjon | Positiv hos ca. 50% |
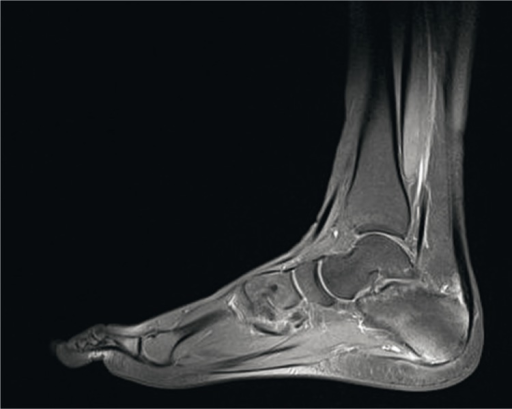
Genetikk.
HLA-B27 forekommer hos ca. 50% av pasienter med aksial affeksjon, men er sjeldnere enn ved ankyloserende spondylitt/Bekhterevs (ca. 95%) og ved IBD-relatert spondyloartritt (ca. 75%). HLA-allelene B*08, B*27 og B*38 er funnet å være risikofaktorer for PsA, mens HLA-C*06 er beskyttende (Eder L, 2012). Disse testene er foreløpig ikke tilgjengelig for rutinemessig bruk. Se også sykdomsårsaker ovenfor.
Bildediagnostikk
Bildediagnostikk supplerer klinisk undersøkelse ved mistanke om PsA. Perifer artritt gjenkjennes oftest klinisk, men ultralyd og MR kan brukes for å påvise synovitt, hydrops og tidlige strukturelle forandringer som ikke alltid fremgår av røntgen.
Radiologiske funn ved PsA omfatter kombinasjonen av skjelett- og bruskdestruksjon (smal leddspalte, erosjoner) og ny benformasjon, inkludert periostitt, osteofytter/entesofytter ved senefester/enteser og i enkelte tilfeller benet ankylose. Dette mønsteret med både destruktive og proliferative forandringer er karakteristisk for PsA.
Ved aksial affeksjon brukes røntgen, CT og MR på samme måte som ved ankyloserende spondylitt. Unilateral sakroiliitt forekommer langt hyppigere ved PsA enn ved typisk bilateral sakroiliitt hos pasienter med ankyloserende spondylitt/Bekhterevs. MR er mest sensitiv for tidlige inflammatoriske forandringer i sakroiliakalledd og columna.
Ultralyd med Doppler er særlig nyttig for å påvise tendinitt og tenosynovitt ved daktylitt samt tegn til inflammasjon ved entesopati, og kan dermed bidra til å skille PsA fra andre artritter i tidlig fase.
Klassifikasjonskriterier
Klassifikasjonskriterier for PsA er ikke validert, men brukes som retningslinjer i klinisk praksis og i forskning. Selv om CASPAR kriteriene ble basert på pasienter med langvarig sykdom, er det vist at de også kan fungere godt i tidlig sykdomsfase (Chandran V, 2007).
| Klassifikasjonskriterier for psoriasisartritt (CASPAR) krever perifer eller aksial artritt eller entesitt og 3 eller flere poeng/Score fra følgende 5 punkter: |
||
| Kriterium | Forklaring | Score |
| 1. Forekomst av psoriasis | ||
| -Nåværende Psoriasis | Psoriasis i huden eller hodebunnen påvist av dermatolog eller revmatolog | 2 |
| -Sykehistorie på psoriasis | Anamnese i henhold til pasient, fastlege, hudlege eller revmatolog | 1 |
| -Familie-anamnese på psoriasis | Psoriasis hos første- eller andregrads slektninger i henhold til pasientens opplysninger | 1 |
| 2. Psoriasis i negler (negle-dystrofi) | Typisk negle-dystrofi (onycholyse, pitting, hyperkeratose) observert av lege ved aktuell konsultasjon | 1 |
| 3. Negativ test for revmafaktorer | Gjelder ikke latex-test, ellers alle revmafaktor tester, fortrinnsvis ELISA eller nefelometri. Utslag over referanseområdene | 1 |
| 4. Daktylitt | ||
| -Pågående daktylitt | Hevelse i hele finger/tås lengde som observeres ved legeundersøkelsen | 1 |
| -Sykehistorie på daktylitt | I henhold til revmatolog | 1 |
| 5. Radiografisk påvist juksta-artikulær ny benformasjon | Patologisk ossifikasjon nær leddspaltene (ikke osteofytter) ved røntgen av hender eller føtter | |
| 98,7% spesifisitet og 91,4% sensitivitet, Taylor W, 2006 | ||
Differensialdiagnoser
Disse tilstandene kan alle gi symptomer som overlapper med psoriasisartritt og dermed kreve grundig differensialdiagnostikk i revmatologisk praksis:
- Andre former for spondyloartritt: Kan alle gi inflammatorisk ryggsmerte, perifer artritt og entesitt som kan ligne på psoriasisartritt:
- Artrose: Kan gi smerter, stivhet og bevegelsesinnskrenkning og kan affisere DIP-ledd i fingre, slik som også psoriasisartritt.
- Pustulosis palmoplantaris: Karakteriseres av sterile pustler i håndflater og fotsåler. Kan forekomme hos pasienter med psoriasisartritt, men er ikke spesifikk for denne tilstanden.
- Revmatoid artritt (RA): Selv om RA oftest rammer små ledd i hender og føtter symmetrisk, kan den også gi asymmetrisk artritt og affisere større ledd som kan ligne på psoriasisartritt.
- SAPHO syndromet: Karakteriseres av synovitt, akne, pustulose, hyperostose og osteitt og kan gi hud- og skjelettmanifestasjoner som ligner på psoriasisartritt.
- Systemisk lupus (SLE): Kan ha artritt, hudutslett og fatigue og ligne på psoriasisartritt, men har også andre karakteristiske manifestasjoner som affeksjon av indre organer.
- Urinsyregikt: Kan medføre akutt inflammatorisk artritt i stortåen (podagra) eller andre ledd. Den kan noen ganger presentere seg med polyartikulær affeksjon og ligne på psoriasisartritt.
| Psoriasis-artritt til forskjell fra revmatoid artritt (RA): Tabell tilpasset etter Coates LC, Clinical Medicine 2017: |
||
| Symptomer | PsA | RA |
| Antall affiserte ledd | 30-50% har oligoartritt | Polyartritt vanligst |
| Ledd-affeksjon | Hvilket som helst, inkludert DIP | Ikke DIP ledd |
| Entesitt | Klinisk hos 60-80% | Uvanlig |
| Daktylitt | Klinisk hos 30% | Uvanlig |
| Aksial affeksjon | Aksial fenotype | Erosiv cervikal affeksjon |
| Kutan/negle affeksjon | Psoriasis: 80% hud, 60% negler | Ikke økt forekomst |
| Serologiske antistoff | RF og CCP vanligvis negative | RF og CCP oftest positive |
| Bildediagnostikk | Periostal ny benformasjon | Erosjoner og osteopeni |
| Forskjeller på ulike spondyloartritter (Richlin CT, 2018) | ||||
| Kjennetegn | Psoriasisartritt | Bekhterevs /ankyloserende spondylitt | Reaktiv artritt | IBD-assosiert artritt |
| Alder ved debut (år) | 36 | 20 | 30 | 30 |
| Mann/kvinne ratio | 1:1 | 3:1 | 3:1 | 2:1 |
| Perifer artritt | 96% | 30% | 90% | 30% |
| Aksial artritt | 50% | 100% | – | 30% |
| Daktylitt | Vanlig | Fraværende | Uvanlig | Fraværende |
| Entesitt | Vanlig | vanlig | Uvanlig | Uvanlig |
| Psoriasis | 100% | 10% | 10% | 10% |
| Negle-lesjoner | 87% | Uvanlig | Uvanlig | Uvanlig |
| HLA-B27 | 40-50% | 90% | 70% | 30% |
Komorbiditet
Psoriasisartritt (PsA) er assosiert med komorbiditeter som kan påvirke både sykdomsforløp, behandling og prognose. Mange av disse er relatert til den kroniske systemiske inflammasjonen, mens andre skyldes livsstilsfaktorer eller effekter av behandling. Pasienter med PsA har en betydelig økt forekomst av kardiovaskulære risikofaktorer, inkludert:
- Adipositas
- Hyper/dyslipidemi eller dyslipidemi
- Diabetes mellitus type 2,
- Hypertensjon
- Metabolsk syndrom
- Fysisk inaktivitet
Den kumulative risikoen for hjerte- og karsykdom (inkludert hjerteinfarkt og cerebrovaskulær sykdom) er høyere sammenlignet med befolkningen for øvrig. Dette skyldes både tradisjonelle risikofaktorer og den vedvarende systemiske inflammasjonen. Regelmessig screening, livsstilsintervensjoner og aktiv behandling av risikofaktorer er derfor anbefalt, ofte i nært samarbeid med pasientens fastlege.
Uveitt forekommer hos omtrent ca. 5 % av pasientene med PsA (Delmås ADC, 2023). Uveitt kan være ensidig eller residiverende, og den kan være assosiert både med aksial sykdom og HLA-B27-positivitet. Tidlig diagnose og øyefaglig vurdering er viktig for å unngå komplikasjoner som synstap.
Andre mulige komorbiditeter:
- Inflammatorisk tarmsykdom (IBD): Forekommer hyppigere hos personer med psoriasis og PsA enn i normalbefolkningen (Alinagi F, 2020).
- Non-alkoholisk fettleversykdom: Vanlig ved kronisk inflammasjon og overvekt; kan påvirke valg av systemisk behandling.
- Depresjon og angst: Økt forekomst, delvis betinget av smerte, funksjonstap og synlige hudmanifestasjoner (Zafiriou E, 2021).
- Osteoporose og økt frakturrisiko: Kan forekomme, særlig ved inaktivitet og langvarig bruk av glukokortikoider (Wang Y, 2023).
Komorbiditet har betydning for valg av behandlingsstrategi. For eksempel kan fedme og metabolsk syndrom redusere effekten av enkelte biologiske legemidler, mens leversykdom kan begrense bruk av metotreksat.
Sykdoms-score
- Senkningsreaksjon (SR) og CRP korrelerer med inflammatorisk aktivitet, men i mindre grad enn ved RA.
- Perifer artritt: 28-Ieddstatus brukes ofte, men pga. hyppig affeksjon av DIP- ledd, føtter og ankler bør disse også undersøkes.
- BASDAI (Bath ankylosing spondylitis activity index) anvendes i klinisk praksis også ved monitorering av aksial PsA.
- Et sammensatt sykdoms-score er foreslått: CPDAI (composite psoriatic disease activity index).
- Ultralyd er nyttig til å diagnostisere og monitorere entesitt, daktylitt og perifer artritt.
- Utbredelse av psoriasis i huden estimeres ved PASI score
- Ved polyartritt kan røntgen av hender/håndledd og føtter benyttes til artritt-klassifikasjon (jfr. CASPAR) og monitorering.
Vennligst se også kapittel om kliniske verktøy og skåringssystemer
Svangerskap
Sykdomsforløp under svangerskap: Litt over halvparten (53%) av kvinner med psoriasisartritt opplever redusert sykdomsaktivitet under svangerskap, men hos ca. 40% blusser sykdommen opp igjen i ukene etter fødsel (Østensen M, 1988; Polachek A., Li S 2017). Norske studier bekrefter lavere sykdomsaktivitet under svangerskap og en viss økning ca. seks måneder post partum (Ursin K, 2019).
Behandling under svangerskap: For pasienter med høy sykdomsaktivitet kan det være aktuelt å fortsette behandlingen f. eks med biologiske legemidler gjennom hele svangerskapet. Dette gjelder imidlertid ikke alle medisiner. Metotreksat må for eksempel seponeres før unnfangelse.
Risiko for komplikasjoner: Sammenlignet med gravide uten PsA er det litt økt risiko for tidlig fødsel (OR 1,63) og fødsel ved sectio (OR1,47-1,43). Risikoen for spontanaborter, dødfødsler eller misdannelser er ikke sikkert økt (Remaeus K, 2019).
Hudsymptomer under svangerskap: Psoriasis i huden blir bedre eller uendret hos over 80% av kvinner i løpet av svangerskapet (Berman M, 2018).
Mer informasjon: For mer detaljert informasjon om svangerskap og psoriasisartritt, se avsnittet om svangerskap og informasjonen fra NKSR.
Behandling av psoriasisartritt
Individualisert tilnærming:
Psoriasisartritt (PsA) krever en individualisert tilnærming til behandlingen. Før oppstart er det aktuelt å kartlegge alle manifestasjoner av sykdommen, inkludert perifer artritt, aksial sykdom, daktylitt, entesitt, psoriasis og neglesykdom og identifisere hvilke av disse som er mest plagsomme for den enkelte pasienten.
Behandlingsmål:
Evidens for “treat-to-target”-strategier ved PsA er begrenset, men det er likevel viktig for prognosen og behandlingsresultatet å sette klare mål for behandlingen. Sentrale behandlingsmål ved PsA kan inkludere:
- Minimal eller ingen sykdomsaktivitet/inflammasjon.
- Optimal fysisk funksjon.
- Bedre livskvalitet og sosial deltakelse.
- Forebygging av strukturell skade. og komorbiditet.
- Minimering av komplikasjoner fra behandlingen (Coates LC, 2016).
Livsstilsendringer
Livsstilsendringer som røykeslutt, vektreduksjon ved overvekt og regelmessig mosjon er viktige tiltak som bør vurderes i kombinasjon med annen behandling.
Medikamentell behandling
Målet med medikamentell behandling er å dempe inflammasjonen for å oppnå de fastsatte behandlingsmålene. Ved oligoartikulær leddaffeksjon har tidlig behandling vist å kunne hindre utvikling til polyartikulær sykdom i mange tilfeller (Gossec L, 2024). Vurdering av sykdomsaktivitet initialt og fortløpende er nyttig for å styre behandlingen. I motsetning til kutan behandling av psoriasis, krever PsA oftere systemisk behandling.
NSAIDs Ikke-steroide antiinflammatoriske legemidler (NSAIDs) som ibuprofen, naproxen og diklofenak er en symptomatisk basisbehandling og kan være tilstrekkelig ved mild artritt. Forsiktighet må utvises ved økt risiko for gastrointestinal blødning, kardiovaskulær sykdom og NSAIDs skal ikke brukes i svangerskapet siste trimester.
Steroidinjeksjoner Steroidinjeksjoner i ledd kan være nyttig ved mono- og oligoartritt. Systemiske kortikosteroider (f.eks. prednisolon) har begrenset plass i behandlingen (Grossec L, 2024).
Sykdomsdempende medikamenter inkluderer csDMARDs (hovedsakelig metotreksat), biologiske legemidler og JAK-hemmere:
csDMARDs. Konvensjonelle syntetiske DMARDs (csDMARDs) som metotreksat, sulfasalazin og leflunomid er førstevalg ved perifer artritt.
Metotreksat foretrekkes dersom det også er hudmanifestasjoner. Ciklosporin A er et mindre brukt alternativ.
Kombinasjonsbehandling. Kombinasjon av metotreksat og en TNF-hemmer (biologisk) brukes ofte dersom metotreksat alene ikke er tilstrekkelig (Fagerli MK, 2012). Studier tyder imidlertid på at kombinasjon med csDMARDs ikke nødvendigvis gir bedre effekt enn biologiske legemidler alene (Regierer AC, 2024). Aksiale manifestasjoner og entesitt responderer ofte dårligere på csDMARDs.
Biologiske legemidler (bDMARDs). Ved utilstrekkelig effekt av minst ett csDMARD eller ved aksial manifestasjon er biologisk behandling indisert. TNF-hemmere (adalimumab, etanercept, infliximab, golimumab, certolizumab) er ofte førstevalget, med secukinumab, ixekizumab (IL-17A-hemmer), bimekizumab (IL-17AF-hemmer) eller ustekinumab (en IL-12/23-hemmer) som alternativer.
Med TNF-hemmere har man lengst erfaring (Fagerli KM, 2018). De kan være effektive mot alle typer PsA også for hud-psoriasis, og entesitt responderer ofte bra (Mathew AJ, 2024). Enkelte tilfeller av psoriasisutbrudd relatert til TNF-behandling for andre sykdommer er rapportert (paradoksal psoriasis) (Abdelghaffar M, 2024).
IL-17- hemmere (sekukinumab/Cosentyx eller ixekizumab/Taltz, bimekizumab/Bimzelx) virker på aller typer PsA og på hud-psoriasis.
Ustekinumab (IL-12/23-hemmer) er effektiv mot psoriasis i huden, mot PsA og har lange behandlingsintervaller. Imidlertid er effekten usikker ved aksiale manifestasjoner.
Guselkumab og Risankizumab (IL-23-hemmere) mot PsA og hud-psoriasis. Ikke forventet effekt på aksiale manifestasjoner.
Apremilast (Otezla) (PDE-4-inhibitor) brukes lite i Norge på grunn av kostnad, men har vist effekt ved PsA og kan være et alternativ ved milde forløp med oligoartritt der biologiske legemidler ikke har effekt eller ikke kan brukes. Medikamentet har en gunstig bivirkningsprofil (Reed M, 2017),
Prednisolon unngås så langt som mulig ved PsA fordi nedtrapping/seponering kan medføre eksaserbasjon av psoriasis (rebound fenomen).
Eksaserbasjon av psoriasis i huden ses også ved bruk av hydroksyklorokin (Plaquenil) som vanligvis ikke er anbefalt.
Bruk av medikamenter utenfor godkjent indikasjon skal dokumenteres grundig (vennligst se eget kapittel om utprøvende behandling).
Tabell: Konvensjonelle DMARDs, Biologiske legemidler (bDMARDs) og JAK-hemmere (tsDMARDs) mot PsA
🟢 = Førstelinje. 🟡 = Alternativ / andre linje. 🔵 = Biologisk legemiddel. 🟣 = JAK-hemmer
| Manifestasjon | Førstelinje | Alternativ / andre linje | Biologiske legemidler | JAK-hemmere | Kommentarer / bivirkninger | Referanser |
|---|---|---|---|---|---|---|
| Polyartritt | 🟢 csDMARD (metotreksat ved psoriasis) | 🟡 bDMARD ved svikt | 🔵 TNF-hemmere (adalimumab, etanercept, infliximab, golimumab, certolizumab), IL-17-hemmere (secukinumab, ixekizumab, bimekizumab), IL-12/23-hemmer (ustekinumab), IL-23-hemmere (guselkumab, risankizumab) | 🟣 JAK-hemmere | TNF-hemmere har lengst erfaring; effekt på hud og entesitt. IL-12/23 og IL-23 mindre effekt på aksiale manifestasjoner. Paradoksal psoriasis kan forekomme med TNF-hemmere | Fagerli KM, 2018; Mathew AJ, 2024; Abdelghaffar M, 2024; Baraliakos X, 2021; van der Heijde D, 2019 |
| Oligoartritt | 🟢 Ingen csDMARD nødvendig med mindre prognostisk ugunst | 🟡 bDMARD ved svikt | 🔵 Samme som polyartritt | 🟣 JAK-hemmere | bDMARD brukes hvis minst én csDMARD har vært mislykket. TNF-hemmere ofte førstevalg | Gossec L, 2024; Coates LC, 2017 |
| Entesitt | ❌ csDMARD ikke effektivt | 🟢 bDMARD som førstevalg | 🔵 TNF-hemmere, IL-17-hemmere | 🟣 JAK-hemmere | Effektive som førstelinje; csDMARD ikke effektivt | Gossec L, 2024; Coates LC, 2017 |
| Daktylitt | 🟢 csDMARD (metotreksat) | 🟡 bDMARD | 🔵 TNF-hemmere, IL-17-hemmere, IL-12/23-hemmere, abatacept (CTLA4-Ig) | 🟣 JAK-hemmere | Flere valgmuligheter, individuell vurdering | Gossec L, 2024; Coates LC, 2017 |
| Aksial PsA | ❌ csDMARD ikke effektivt | 🟢 bDMARD | 🔵 TNF-hemmere, IL-17-hemmere | 🟣 JAK-hemmere | IL-17-hemmer og TNF-hemmere anbefales; IL-12/23 og IL-23 forventes ikke effektive | van der Heijde D, 2006; Baraliakos X, 2021; van der Heijde D, 2019 |
| Hud-psoriasis | 🟢 csDMARD | 🟡 bDMARD | 🔵 TNF-hemmere, IL-17-hemmere, IL-12/23-hemmere, IL-23-hemmere | 🟣 JAK-hemme |
Prognose
Psoriasisartritt (PsA) kan være en alvorlig form for artritt, selv om prognosen har blitt betydelig bedre de senere årene (Losinska K, 2024). Ubehandlet kan PsA føre til betydelig smerte, stivhet og funksjonsnedsettelse. Studier fra før introduksjonen av biologisk behandling viste at 47 % av pasientene utviklet erosjoner i leddene i løpet av de to første årene, til tross for behandling med konvensjonelle syntetiske DMARDs (Kane D, 2003).
Bedret sykdomsforløp med biologisk behandling: Biologiske legemidler endret sykdomsforløpet for mange pasienter med PsA. Med adekvat behandling opplever de fleste en betydelig reduksjon i sykdomsaktivitet og en forbedring i funksjon. Imidlertid må det forventes residiv ved seponering av biologisk behandling, og spontan remisjon er svært uvanlig.
Prediktorer for destruktivt forløp: Forløpet av perifer artritt ved PsA er variabelt, fra selvbegrensende og ikke-destruktivt til langsomt progredierende og uttalt destruktivt. Flere faktorer er identifisert som prediktorer for et destruktivt forløp: Polyartritt, høy SR/CRP, daktylitt og/eller negle-manifestasjoner, terapirefraktær sykdom og allerede påvist leddskade. Tidlig identifisering av disse faktorene er viktig for å intensivere behandlingen og forebygge ytterligere leddskade.
Hjerte-karsykdom: Personer med PsA har en økt risiko for kardiovaskulær sykdom, inkludert koronararterie-manifestasjoner. Denne økte risikoen bidrar til økt mortalitet sammenlignet med den generelle befolkningen (Fagerli KM, 2018).
Retningslinjer, anbefalinger og prosedyrer
EULAR: Gossec L, 2024 (medikamenter)
GRAPPA/EULAR 2017, Coates LC, 2017
Norsk Revmatologisk Forening/Legeforeningen
- Vennligst les mer om behandlingsretningslinjer i eget kapittel
Litteratur
- Yi RC, 2025 (nyere behandling)
- Azuaga AB, 2023
- Sbidian E, 2023 (behandling av plakkpsoriasis, Cochrane)
- Ruyssen-Witrand A, 2020 (behandling)
- EULAR: Gossec L, 2020 (medikamenter)
- Ocampo V, 2019
- Richlin CT, 2018
- Coates LC, Clinical Medicine 2017
- Eder L, 2015
- Mease PJ. Ann Rheum Dis. 2011
- Madland TM. Norsk epidemiologi 2008;18:16-20.
Teksten er basert på aktuell faglitteratur. Den er skrevet og gjennomgått av forfatterne. I bearbeidelsen er kunstig intelligens brukt i noen avsnitt.
