ARTRITT (REV 006-REV 020)
25 IBD-relatert spondyloartritt. Enteropatisk artritt. Crohns, ulcerøs kolitt (REV 007)
Øyvind Palm
Diagnosekoder ICD-10: M07.5 + K51.9 Artritt, SpA, ved Ulcerøs kolitt, M07.4 + K50.9 Artritt ved Crohns, M45 (Ankyloserende SpA/Bekhterevs sykdom), M46.1 Isolert radiologisk artritt i IS-ledd uten annen SpA affeksjon
Prosedyrekoder: Leddpunksjon/artrocentese (klikk for å spesifisere ledd:) TN_10. UL veiledet leddpunksjon: NXA10K. Mikroskopi av leddvæske: NXFT05.
ATC koder: Behandling med immunsuppressive legemidler: L04A. adalimumab: L04AB04, triamcinolon (Lederspan): H02AB08, betametason (Celeston Chronodose): H02AB04, infliksimab: L04AB02, ustekinumab: L04AC05, vedolizumab: L04AA33.
Nøkkelord som kan vurderes ved anamnese og klinisk undersøkelse hos pasienter med IBD og revmatiske manifestasjoner
- Leddsmerter og stivhet – varighet, lokalisasjon, morgenstivhet, påvirkning av aktivitet
- Leddhevelse / varme / rødhet – mono-, oligo- eller polyartikulær fordeling
- Aksiale symptomer – ryggsmerter, nattsmerter, bedring ved bevegelse, debutalder <45 år
- Perifere leddaffeksjoner – knær, ankler, små ledd i hender/føtter
- Daktylitt – «pølsefinger/pølsetå», hevelse i hele finger/tå
- Entesopati / senefeste-inflammasjon – spesielt Akillessene, plantar fascia
- Ekstraintestinale manifestasjoner – erythema nodosum, pyoderma gangrenosum, uveitt, episkleritt, primær skleroserende kolangitt
- Tidspunkt i forhold til tarmsykdom – debut før, samtidig med, eller etter IBD-diagnose
- Familiehistorie – IBD, spondyloartritt, ankyloserende spondylitt
- Respons på tidligere behandling – NSAIDs, DMARDs, biologiske legemidler, kortikosteroider
- Hensikten med konsultasjonen
Innhold
- Definisjon
- Ulcerøs kolitt (UC)
- Crohns sykdom (CD)
- Historie
- Epidemiologi
- Genetikk
- Patogenese
- Symptomer og sykdomsmanifestasjoner
- Laboratorieundersøkelser
- Bildediagnostikk
- Differensialdiagnose
- Svangerskap
- Behandling
- Prognose
- Retningslinjer
- Litteratur
Definisjon
Ulcerøs kolitt (UC) og Crohns sykdom (CD) er kroniske inflammatoriske tarmsykdommer (inflammatory bowel disease; IBD). Sykdomsårsakene er ikke helt klarlagt, men man antar at det foreligger en skade på tarmslimhinnens mukosa-barriere som fører til en dysregulert immunrespons hos genetisk disponerte personer. Nyere behandlingsstrategier går ut på å hemme eller blokkere deler av den overaktive immunresponsen (Higashiama M, 2023).
IBD er ofte forbundet med ekstraintestinale manifestasjoner. De vanligste er revmatiske, som perifer artritt (IBD-artritt/enteropatisk artritt), artralgi, entesopati og daktylitt. Disse klassifiseres innen spondyloartritter (SpA). Klassisk ankyloserende spondylitt/Bekhterevs sykdom kan også være en del av sykdomsbildet.
Ulcerøs kolitt (UC)
Ulcerøs kolitt angriper colon, men ikke andre deler av gastrointestinaltraktus. Sykdommen kan debutere i alle aldre, men ses oftest hos unge voksne. Inflammasjonen affiserer mucosa og submucosa. Vanlige symptomer ved UC er:
- Abdominale smerter
- Blodig diaré
Ekstraintestinale manifestasjoner er hyppige Spondyloartritt er den vanligste revmatiske manifestasjonen. Andre vanlige ekstraintestinale manifestasjoner inkluderer erythema nodosum, pyoderma gangrenosum, uveitt, episkleritt og primær skleroserende kolangitt.
Undersøkelser
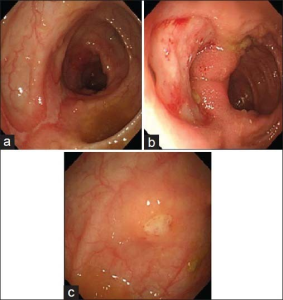
- Koloskopi: Viser inflammasjon i hele eller deler av colon.
- Blodprøver: Økt CRP og tegn til anemi er vanlig.
- Fekal calprotectin: Kan indikere subklinisk (mikroskopisk) inflammasjon.
- Endoskopi med biopsier: Nødvendig for å bekrefte diagnosen.
Behandling er primært 5-ASA-preparater som basisbehandling, supplert med kortikosteroider i akutte faser og immunhemmende eller biologiske legemidler ved alvorlig eller behandlingsresistent sykdom.
Crohns sykdom (CD)
Crohns sykdom kan ramme hele gastrointestinaltraktus – fra munnhule til anus. Inflammasjonen er typisk transmural (går gjennom hele tarmveggen) og granulomatøs. Sykdommen debuterer oftest i barne- eller ung voksen alder, men kan forekomme i alle aldersgrupper.
Symptombildet varierer avhengig av hvilke deler av tarmen som er affisert. Vanlige symptomer inkluderer:
- Abdominale smerter fra tynn- og/eller tykktarm
- Diaré
- Rektal blødning (vanligere ved UC)
- Feber, vekttap, utmattelse
- Fistler (til andre organer eller gjennom huden)
Som ved ulcerøs kolitt er Spondyloartritt den vanligste ekstraintestinale manifestasjonen. Andre vanlige manifestasjoner er erythema nodosum, uveitt og episkleritt
Undersøkelser:
- Fekal calprotectin: Kan indikere subklinisk intestinal inflammasjon.
- Kapselendoskopi: Påviser inflammatoriske forandringer i tynntarmen.
- Endoskopi med biopsi: Nødvendig for å bekrefte diagnosen og vurdere utbredelse.
Behandlingen er med kortikosteroider i akutte faser. Som vedlikeholdsbehandling eller alvorlig sykdom brukes ofte immunhemmende midler og biologiske legemidler (f eks. TNF-hemmere) for å forhindre tilbakefall og alvorlige komplikasjoner.
Historie
Ulcerøs kolitt ble først beskrevet som egen sykdom av Samuel Wilks i 1859. Crohns sykdom ble senere definert som en separat diagnose av Burrill Bernard Crohn i 1932.
En mulig sammenheng mellom IBD og artritt ble først omtalt av White i 1895 (White MH, Lancet, 1895), men det tok mange år før IBD-assosiert artritt ble skilt fra revmatoid artritt (RA).
I 1930 rapporterte Bargen at 4,3% av pasientene med ulcerøs kolitt utviklet artritt (Bargen J, Medicine, 1930). Fem år senere viste Hench at denne artritten var forskjellig fra RA (Hench PS, 1935). En sammenheng mellom ankyloserende spondylitt/Bekhterevs og IBD ble første gang dokumentert av Romanus i 1953 (Romanus B, 1953).
Epidemiologi
Ekstraintestinale manifestasjoner forekommer hos en betydelig andel av pasienter med inflammatorisk tarmsykdom. Risikoen er samlet sett 15–20 % ved ulcerøs kolitt (UC) og 20–40 % ved Crohns sykdom (CD). De revmatiske manifestasjonene er de vanligste og forekommer omtrent like hyppig hos kvinner og menn.
- Perifer artritt: Utvikles hos 15–20 % av pasientene (Ossum, AM, 2018).
- Ankyloserende spondylitt/Bekhterevs påvises hos 4-5%.
- Aksial SpA hos 5-10% (Ossum AM, 2018).
Omvendt viser studier at 6–14 % av pasienter med ankyloserende spondylitt har samtidig IBD ved undersøkelse av tarmen (Fragous GE, 2019).
Genetikk
Det er funnet flere genetiske faktorer med felles disposisjon for ankyloserende spondylitt, CD og UC (Cortes A, 2013). En islandsk studie viste at første- og andregrads slektninger av pasienter med ankyloserende spondylitt har 2-3 ganger økt risiko for IBD (Thjodleifsson B, 2007). Vevstypen HLA-B 27 er sterkt assosiert med ankyloserende spondylitt ved IBD (75%), men ikke for perifer artritt (Palm Ø, 2002).
Utenfor HLA-systemet ses viktige variasjoner (polymorfismer), særlig i CARD 15 (NOD2-genet), som koder for proteinet NOD2. Denne genetiske varianten øker risikoen for både CD og sakroiliitt.
NOD2 er en intracellulær reseptor for bakterielle molekyler og forekommer på overflaten av makrofager, lymfocytter, Paneth-celler og annet intestinalt epitel. NOD2 kan aktivere innate immunrespons via nukleær faktor kappa-BetaB (NFκB) som regulerer gener for proinflammatoriske mediatorer. Dermed er NOD2 sentral i tarmens immunforsvar og utviklingen av inflammasjon (Fragous GE, 2019).
Patogenese
Utviklingen av inflammatorisk tarmsykdom (IBD) og tilhørende revmatiske manifestasjoner er multifaktoriell. Miljøfaktorer, genetisk disposisjon og mikrobiell ubalanse virker sammen i sykdomsprosessen.
Ved IBD-relatert spondyloartritter står samspillet mellom tarm, immunsystem og ledd sentralt, tilsvarende som ved andre spondyloartritter. Endringer i tarmens mikrobiom (samlet bakterieflora) og migrsajon av lymfocytter mellom tarm og ledd antas å være av betydning for utvikling av spondyloartritt ved IBD (Gilis E, 2018). Omtrent 50 % av pasienter med ankyloserende spondylitt har subklinisk (mikroskopisk) tarminflammasjon, uten symptomer (Cypers H, 2014). Hos de fleste forblir denne tarminflammasjonen under kontroll, men hos 6-14% utvikles klinisk IBD (Fragoulis GE, 2019).
Symptomer og sykdomsmanifestasjoner
Bevegelsesapparatet kan affiseres på to hovedmåter:
- Perifere ledd (artralgi og artritt )
- Aksiale ledd (rygg og bekken)
Bevegelsesapparatet angripes på to måter: En som affiserer perifere ledd med artralgi og artritt og en type som angriper de aksiale leddene (rygg og bekken).
Perifer artritt ved IBD
Symptomer:
- Alle ledd kan angripes, men vanligst er knær og ankler (Type 1 – oligoartritt).
- Et mindretall utvikler affeksjon i små ledd, oftest MCP-ledd (Type 2 – polyartikulær) som kan vedvare over måneder/år og ligne revmatoid artritt (RA) (Orchard TR, 2000).
- Leddsymptomene inkluderer smerte (artralgi), stivhet, varme og hevelse.
- Artrittaktivitet følger ofte tarmens inflammatoriske aktivitet, men kan debutere før, samtidig med eller etter tarmsykdom.
- Erythema nodosum kan opptre samtidig med perifer artritt (Palm Ø, 2001).
Undersøkelser
- Klinisk undersøkelse bekrefter mono- eller oligoartikulær som vanligvis er asymmetrisk og non-erosiv med varighet under 4 uker (Palm Ø, 2001).
- Vanligst affiserte ledd: knær → ankler → fingerledd/albuer.
- Pasientene er vanligvis seronegative for revmatoide faktorer og anti-CCP.
Aksial manifestasjon ved IBD
Symptomer:
- Ankyloserende spondylitt/Bekhterevs utvikles hos 4–5 % av pasienter med UC eller CD. Det er cirka fire ganger hyppigere enn i normalbefolkningen.
- Aksial spondyloartritt (basert på ASAS-kriteriene) forekommer hos ca. 7,7 % av IBD-pasienter.
- Typisk inflammatorisk ryggsmerte: gradvis debut før 40–45 års alder, morgenstivhet >30 minutter, nattsmerter, bedring ved fysisk aktivitet, varighet >3 måneder påvises hos ca. 11,5 % av pasientene (Ossum AM, 2018; Palm Ø, 2002).
Undersøkelser:
- MR eller radiografi av sakroiliakalledd kan påvise inflammasjon og sakroiliitt.
- Aksiale manifestasjoner bør kartlegges tidlig, men radiografiske forandringer (røntgen eller CT) utvikles først etter 2–6 år.
- CT abdomen, tatt for å evaluere tarmen, kan sekundært påvise sakroiliitt.
Kliniske, revmatiske manifestasjoner ved IBD
| Klassifikasjon av IBD-relatert (ECCO consensus; Harbord M, 2015) | ||
| Lokalisering | Sykdomskarakteristika | Subtyper |
| Perifer artritt | Tegn til inflammasjon; eksklusjon av andre artrittformer. | Type 1: ≤5 ledd, underekstremiteter, akutt og selvbegrensende, følger IBD-aktivitet
Type 2: >5 ledd, overekstremiteter, vedvarende, uavhengig av IBD-aktivitet |
| Aksial SpA | Inflammatorisk ryggsmerte + MR/røntgen sakroiliitt | Sakroiliitt med eller uten spondylitt |
Daktylitt («pølsefinger/pølsetå») er hevelse i hele fingres eller tærenes lengde. Dette skyldes fleksorsenesynovitt og er et karakteristiskfor IBD-relatert sykdom og ved noen andre spondyloartritter. Forekomsten ved IBD relatert spondyloartritt er 2-4% (Brakenhoff LK, 2010). Daktylitt påvises ved klinisk undersøkelse, ultralyd av fleksorseneskjeder eller MR-undersøkelse.
Entesopati/entesitt er inflammasjon i senefester, mest typisk der Akillessenen fester seg til calcaneus. Symptomene er smerte og hevelse. Forekomsten er 5-10% ved IBD relatert SpA (Brakenhoff LK, 2010).
Artralgi. Leddsmerter uten artritt er hyppige, særlig ved CD (22%). Symptomene kan redusere livskvaliteten (Palm Ø, 2005), men årsaken er uklar. En klar sammenheng med tarmsykdommens aktivitet er ikke påvist, og fibromyalgi forekommer ikke oftere enn i befolkningen generelt (Palm O, 2001).
Andre ekstra-intestinale manifestasjoner
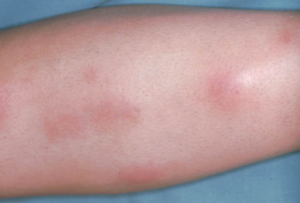
- Erythema nodosum (10-20%)
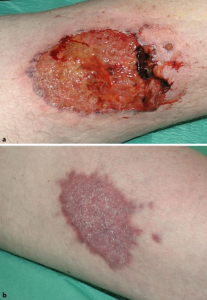
- Pyoderma gangrenosum (0,4-21%)
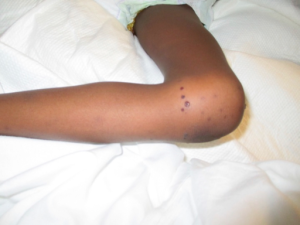
- Artritt-dermatitt syndrom, Bowel-associated dermatosis-arthritis syndrome BADAS
- Uveitt (2-5%)
- Primær skleroserende kolangitt (<1%)
Laboratorieundersøkelser
- Blodprøver: CRP, SR, Hb, leukocytter med differensialtelling, trombocytter, elektrolytter, lever-, nyre-, pankreas- og thyreoidea-funksjon, albumin.
- Immunologiske markører: Anti-CCP. ANA. Ingen spesifikke markører for IBD-relatert artritt; p-ANCA kan være positivt uspesifikt. PR3- eller MPO-ANCA forventes å være normale.
- Urin: Stiks.
Typiske funn:
- Forhøyet CRP og SR på grunn av tarminflammasjon.
- Anemi særlig ved CD og tidlig i sykdomsforløpet og ved høy CRP (Høivik M, 2014).
- Forhøyede leverenzymer med cholestase-mønster kan indikere skleroserende kolangitt (hyppigere ved UC).
- HLA-B27 positivitet styrker mistanken om aksial manifestasjon; 50–75 % av pasienter med ankyloserende spondylitt + IBD er HLA-B27 positive.
Bildediagnostikk
De fleste perifere manifestasjoner (artritt, daktylitt og entesopati/entesitt) påvises klinisk uten behov for bildediagnostikk.
- Røntgen og CT: Vanligvis normale ved non-erosiv perifer artritt, som er den vanligste formen.
- Ultralyd- og MR: Kan dokumentere artritt, daktylitt og entesopati.
- Aksiale manifestasjoner: MR av columna og sakroiliakalledd viser tidlig inflammasjon. Radiografiske forandringer utvikles vanligvis etter 2–6 år. CT-abdomen, tatt for tarmvurdering, kan også vise sakroiliitt som bi-funn (Kim DK, 2024).
Differensialdiagnoser
- Andre former for spondyloartritt:
- Ankyloserende spondylitt (Bekhterevs sykdom): Kan involvere ryggraden og gi lignende symptomer som enteropatisk/IBD-artritt.
- Psoriasisartritt: Assosiert med psoriasis.
- Reaktiv artritt: Utløses av forutgående infeksjon.
- Andre former for artritt:
- Revmatoid artritt: ikke assosiert med IBD.
- Infeksiøs artritt: Artritt forårsaket av en infeksjon.
- Andre tilstander:
- Fibromyalgi: Utbredt smerte og utmattelse, men ikke artritt.
- Artrose: Bruskskade med smerter og stivhet.
Svangerskap
Svangerskap kan forverre både ulcerøs kolitt og Crohns sykdom. God gastroenterologisk oppfølging er viktig for å tilpasse behandling og oppnå optimal sykdomskontroll. Høy sykdomsaktivitet under svangerskapet øker risikoen for komplikasjoner (Shannahan SE, 2019).
Behandling
Behandlingen av revmatiske og andre ekstraintestinale manifestasjoner ved IBD krever ofte tverrfaglig samarbeid mellom revmatolog og gastroenterolog. I mange tilfeller vil en god kontroll på tarmsykdommen være gunstig også for den revmatiske tilstanden. Unntak er aksial artritt, pyoderma gangrenosum, uveitt og skleroserende cholangitt som ofte forløper uavhengig.
Behandlingsmålet er å eliminere inflammatoriske revmatiske manifestasjoner uten å forverre tarmsykdommen. Helst bør behandlingen virke mot begge tilstandene.
| Kategori | Tiltak / Medikament | Kommentar / Effekt |
|---|---|---|
| Generelle prinsipper | Kontroll av tarmsykdom | Reduserer ofte perifere revmatiske symptomer. |
| Spesielle manifestasjoner | Aksial artritt, pyoderma gangrenosum, uveitt, skleroserende cholangitt følger ofte ikke tarmens aktivitet; krever særskilt behandling. | |
| Behandlingsmål | Eliminere inflammasjon uten å forverre tarmsykdom | |
| Medikamentell behandling | NSAIDs | Lindrer perifer og aksial artritt; kan forverre tarmen hos ~20 % (Kvasnovsky CL, 2015); forsiktig bruk, også for COX-2-hemmere (Hijos-Maldala G, 2021). |
| csDMARDs (sulfasalazin, metotreksat) | Effekt på perifer artritt; ikke på aksiale manifestasjoner. | |
| Kortikosteroider (intraartikulært triamcinolon (Lederspan) eller kortvarig systemisk prednisolon) | Effekt ved perifer artritt. | |
| Biologiske legemidler/bDMARDs (TNF-hemmere: infliksimab, adalimumab; alternativer: ustekinumab, vedolizumab) | Ved manglende effekt av NSAIDs; etanercept og IL-17-hemmere bør unngås. Ustekinumab og vedolizumab er andre alternativer. | |
| JAK-hemmere (tsDMARDs) | Brukes ved moderat til alvorlig UC; kan også redusere perifer artritt (Moran GW, 2025). | |
| Supplerende tiltak | Aksial manifestasjon | Fysioterapi, egentrening og medikamenter som ved ankyloserende spondylitt. |
| Osteoporose | Vurder DEXA-måling og profylaktisk behandling. | |
| Øyemanifestasjon | Uveitt/skleritt: vurder øyelege; episkleritt trenger ikke alltid spesialistbehandling (Harbord M, 2015). |
Prognose
Forløpet av IBD-relatert artritt varierer mellom pasientene. Perifer artritt: Type 1 (≤5 ledd) er oftest selvbegrensende, mens Type 2 (polyartikulær) kan være langvarig.
Aksiale manifestasjoner kan ha et alvorlig forløp, men generelt mer benign enn idiopatisk ankyloserende spondylitt. Forløpet av aksial artritt er uavhengig av tarmsykdommens aktivitet. Selv ved helbredende kolektomi ved UC vil ryggsykdommen ofte fortsette å progrediere.
Retningslinjer, anbefalinger og prosedyrer
- Britiske guidelines for IBD, 2025
- AGA Practical guiedlines for UC, 2024
- AGA Guideleines for Crohns, 2018
- ECCO (The First European Evidence-based Consensus on Extra-intestinal Manifestations in Inflammatory Bowel Disease), Harbord M, 2015.
- Vennligst les mer generelt om behandlingsretningslinjer i eget kapittel
Gastrointestinale manifestasjoner ved andre revmatiske sykdommer er beskrevet i eget kapittel
Litteratur
- Moran GW, 2025
- Higashiama M, 2023 (behandling)
- Ordas I, 2012 (Ulcerøs kolitt)
- Whitney D, 2023 (Ulcerøs kolitt)
- Indika R, 2024 sp (Crohns sykdom)
- Malik TF 2023 sp (Ekstraintestinale manifestasjoner)
- Ossum AM, 2018
- Harbord M, 2015 (definisjoner av ekstraintestinale manifestasjoner)
Teksten er basert på aktuell faglitteratur. Den er skrevet og gjennomgått av forfatterne. I bearbeidelsen er kunstig intelligens brukt i noen avsnitt.
