BASISKOMPETANSE (REV 001-005)
2 Anatomi, fysiologi, patologiske prosesser (REV 001-002)
Jan Tore Gran and Øyvind Palm
Læringsmål REV 001. Revmatologen skal ha god kunnskap om anatomi og fysiologi ved normale og patologiske prosesser relevant for revmatiske sykdommer, herunder beinmetabolisme, fatigue, inflammasjon, smertefysiologi og smertemekanismer.
Læringsmål REV 002. Revmatologen skal ha god kunnskap om normal, samt mikroskopisk og makroskopisk pato-anatomi og histologi av organsystemer og vev relevant for revmatologiske sykdommer.
Dette kapitlet beskriver normal anatomi og histologi (makro + mikro) av strukturer i ledd, synovium, brusk, leddkapsel, bindevev og blodkar. Det omtaler også patologiske endringene (makro + mikroskopisk) ved revmatiske sykdommer og peker på viktige kliniske og terapeutiske konsekvenser.
- Benmetabolisme er beskrevet i kapitlet om osteoporose.
- Fatigue er omtalt i eget kapittel
- Inflammasjon beskrives i kapitelet om immunsystemet
- Smertefysiologi og smertemekanismer er beskrevet i kapitlene om smertetilstander, fibromyalgi, algodystrofi og analgetika.
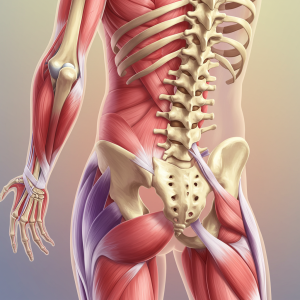
Innledning
Leddene muliggjør all bevegelse. Forståelse av leddenes anato mi og fysiologi er viktig for å kunne diagnostisere og behandle leddsykdommer. Innholdet er delt inn i fire hoveddeler:
- Normal anatomi og histologi (makroskopisk og mikroskopisk)
- Leddstruktur makroskopisk
- Columna
- Leddets histologi og mikroskopisk struktur, brusk og subkondralt vev
- Bindevev
- Blodårer
- Patologiske prosesser (makro- og mikroskopiske) ved revmatiske sykdommer
- Synovitt og artritt
- Bruskskade
- Erosjoner
- Fibrose
- Systemiske bindevevssykdommer
- Vaskulitt
- Klinisk betydning og relasjon for behandling
- Diagnostisering
- Behandling
- Oppsummering: normal versus patologisk
- Normalt og patologisk synovium, brusk, subkondralt beinvev, kapsel, ligamenter, bindevev og blodkar.
- Klinisk og terapeutisk betydning.
1. Normal anatomi og histologi (makroskopisk og mikroskopisk) -relevante strukturer
Leddstruktur — makroskopisk oversikt
Et typisk synovialledd består av:
- Leddkapsel (ytterste fibrøs kapsel + indre synovialhinne)
- Synovialvæske (intraartikulær væske)
- Brusk (hyalin brusk) på benflater
- Underliggende ben (subkondralt ben)
- Tilgrensende strukturer: leddbånd, sener, bursae, menisker eller skiver (f. eks. i columna)
Et ledd er en forbindelse mellom to eller flere ben- eller bruskstrukturer. De kan klassifiseres strukturelt (etter type bindevev) eller funksjonelt (etter grad av bevegelighet). Tradisjonelt deles ledd inn i tre hovedtyper basert på struktur og bevegelighet:
Ekte ledd (diartroser/synovialledd) kjennetegnes av en leddhule (cavum articulare) fylt med synovialvæske. Synovialvæsken smører og ernærer leddbrusken (cartilago articularis) og andre intraartikulære strukturer. Ekte ledd er de mest bevegelige leddene.
- Eksempler: Skulderleddet (articulatio humeri), albueleddet (articulatio cubiti), hofteleddet (articulatio coxae), kneleddet (articulatio genus) og fingerledd (articulationes interphalangeales manus).
- Sammensatte ledd: Noen ledd er sammensatte, der flere anatomiske ledd inngår i en funksjonell enhet, som for eksempel skulderleddet (articulatio humeri) som funksjonelt involverer glenohumeralleddet, det akromioklavikulære leddet, sternoklavikulærleddet og det skapulotorakale “leddet” (en glideflate mellom skulderbladet og brystkassen).
Halvekte ledd (amfiartroser) mangler leddspalte og leddvæske. Disse leddene har begrenset bevegelighet. Benflatene er forbundet med en leddskive (discus articularis) av fibrobrusk eller en sammenvoksning av fibrobrusk (f. eks. symfyser).
- Eksempler: Symphysis pubica (symfysen mellom kjønnsbeina) og mellomvirvelskivene (disci intervertebrales).
- Kjeveleddet (Articulatio temporomandibularis): Selv om det inneholder en intraartikulær diskus, klassifiseres det nå som et ekte ledd (synovialledd) på grunn av sin struktur og bevegelighet.
Uekte ledd (synartroser): Disse leddene mangler leddhule og synovialvæske. Bevegeligheten er svært begrenset eller fraværende. Det finnes flere undergrupper:
- Fibroseforbindelser (syndesmoser): Benflatene er forbundet med fibrøst bindevev, f.eks. membrana interossea mellom tibia og fibula.
- Bruskforbindelser (synkondroser): Benflatene er forbundet med hyalin brusk, f.eks. epifyseskivene (disci epiphysiales) hos barn og costochondralleddene (mellom ribben og ribbensbrusk).
- Benforbindelser (synostoser): Benflatene er direkte forbundet med benvev som følge av ossifikasjon av tidligere fibrøst eller bruskholdig vev. Eksempler er forbenede suturer i kraniet hos voksne og sammenvoksingen av hoftebeinet (os coxae) fra de tre separate bena (ilium, ischium og pubis).
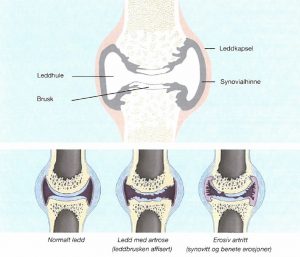
De ulike strukturene i et ledd jobber sammen for å sikre bevegelse, stabilitet og støtte:
- Leddflater og brusk (facies articulares og cartilago articularis): Leddflatene er dekket av hyalin leddbrusk.
- Leddhulen (cavum articulare): Et lukket rom mellom leddflatene, fylt med synovialvæske.
- Leddkapsel (capsula articularis): En bindevevskapsel som omgir leddet og omslutter leddhulen og synovialvæsken. Den består av et ytre fibrøst lag (stratum fibrosum) og et indre synovialt lag (stratum synoviale/synovialhinnen).
- Leddbånd (ligamenter): Sterke bånd av bindevev som forbinder ben og stabiliserer leddet.
- Sener (tendiner): Bånd av bindevev som fester muskler til ben og bidrar til leddbevegelse.
- Intraartikulære disker og menisker (leddskiver, disci et menisci articulares): Fibrobruskstrukturer som deler leddhulen helt eller delvis og bidrar til stabilitet, kongruens og belastningsfordeling. Meniskene i kneleddet er C-formede skiver av fibrobrusk.
- Synovialvæske (synovia): En viskøs væske produsert av synovialhinnen som smører og ernærer leddbrusken og andre intraartikulære strukturer.
I tillegg kan ledd inneholde fettvev (fettlegemer/corpora adiposa) og blodkar (f.eks. i synovialhinnen).
Embryologi: Utviklingen av ledd følger visse prinsipper:
- Proksimale strukturer utvikles før distale (proximodistal gradient).
- Kraniale strukturer dannes før kaudale (kranial til caudal gradient).
Dette innebærer at overekstremiteten utvikles før underekstremiteten, og at proksimale deler av ekstremitetene utvikles før distale. Dette har betydning for forståelsen av medfødte misdannelser (Langman’s Medical Embryology).
Betegnelser på ledd
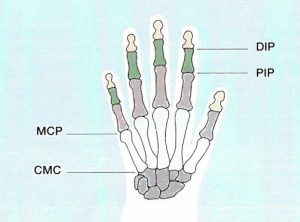
Hender
- Distale Inter-Phalangealledd (DIP)
- Angripes ofte ved artrose og ved psoriasisartritt, men ikke ved revmatoid artritt (RA)
- Proksimale Inter-Phalangealledd (PIP)
- Angripes ved artrose, RA og psoriasisartritt
- Meta Carpo Phalangealledd (MCP, grunnledd)
- Angripes ved RA og psoriasisartritt, ikke ved artrose
- Carpo Metacarpo Phalangealledd (CMC)
- CMC-1 (ved tommel) angripes ved artrose
Føtter
- MetaTarso Phalangealledd) (MTP) tilsvarer MCP (grunnledd) i hender
- Hele MTP-rekken angripes ved RA, MTP-1 (store tå) ved artrose (hallux valgus)
Ryggsøylen/columna
Ryggsøylen (columna vertebralis) (ryggraden) er kroppens sentrale akse. Den gir støtte, stabilitet og bevegelighet og beskytter ryggmargen (medulla spinalis). Ryggsøylen består av vanligvis 24 virvler (vertebrae) som er forbundet med ledd, muskler og ligamenter. Hos voksne mennesker består ryggsøylen også av korsbenet (os sacrum) og halebenet (os coccygis) (til sammen 26 virvler). Os sacrum og os coccygis er dannet ved sammensmeltning av flere virvler. Hos barn ses 33-34 separate virvler.
Ryggsøylen kan deles inn i fem seksjoner (halsvirvelregionen, brystvirvelregionen, lendevirvelregionen, korsbenet og halebenet):
- 7 halsvirvler: Gir bevegelighet til hodet.
- 12 brystvirvler: Festet til ribbeina og danner brystkassen.
- 5 lendevirvler: Bærer mye av kroppens vekt.
Hver virvel har en kropp (corpus) og en bue (arcus). Buen danner en ring som omslutter ryggmargen. Mellom virvlene er det bruskskiver (discus) som fungerer som støtdempere og gir bevegelighet.
Fasettleddene er synovialledd mellom de fleste virvlene. De er små, parvise ledd dorsalt for corpus som gir bevegelighet i ryggraden, men begrenser bevegelser for å beskytte ryggmargen. Hver voirvel har fire fascettledd, to som peker oppover og to som peker nedover. Fasettleddene er dekket av brusk og omgitt av en synovialhinne som produserer leddvæske. En relativt vanlig tilstand med alderen er artrose i fascettleddene som medfører stivhet og smerte i nakke eller rygg.
Skiveleddene er mellomvirvelskivene som ligger mellom virvlene (discus intervertebralis). De fungerer som støtdempere og gir bevegelighet i ryggraden. Skiveleddene er bygd opp av en geleaktig kjerne omgitt av en fibrøs ring. Ved skiveprolaps er kjernen kommet ut gjennom kapselen og kan trykke nerverøtter og medføre utstrålende smerte (isjas).
Iliosakralledd er et synovialledd med kapsel som forbinder korsbenet (sacrum) med hoftebeinet (ilium). Det er et kraftig ledd som gir stabilitet til bekkenet og ryggraden og absorberer støt. Iliosakralleddet er dekket av brusk og omgitt av en synovialhinne som produserer leddvæske. Inflammasjon i iliosakralledd (sakroiliitt) er essensielt ved spondyloartritt.
En rekke sykdommer kan ramme ryggsøylen. Noen av de vanligste er muskelspenninger, artrose/spondylose, skiveprolaps og isjias og spondyloartritt.
Leddets histologi og mikroskopisk struktur
Synovialhinnen (stratum synoviale, synovia) er det indre laget av leddkapselen og dekker innsiden av leddhulen i ekte ledd. Den bidrar til leddets stabilitet, beskyttelse, ernæring av leddbrusken og smøring via synovialvæsken. En balanse mellom anabole og katabole prosesser er regulert av matrixmetalloproteinaser (MMP). MMP finnes normalt i synovialvæsken, men forekommer i økte konsentrasjoner ved patologiske tilstander som artritt og artrose (Tchetverikov I, 2005).
Synovialhinnen er unik ved at den mangler basalmembran, noe som muliggjør en direkte utveksling av substanser mellom synovialvæsken og de synoviale kapillærene. Dette bidrar til rask transport av næringsstoffer til brusken og fjerning av avfallsstoffer. Synoviocyttene utgjør cellelaget i synovialhinnen og finnes i to hovedtyper:
- Type A synoviocytter (makrofaglignende): Har fagocyterende egenskaper og fjerner partikler og avfallsstoffer fra leddhulen.
- Type B synoviocytter (fibroblastlignende): Produserer synovialvæskens komponenter som hyaluronsyre, glykoproteiner og andre proteiner.
Synovialvæsken (leddvæsken) er en klar, viskøs væske som dannes ved filtrasjon av plasma fra de synoviale kapillærene med tillegg av hyaluronsyre og glykoproteiner som produseres av type B synoviocytter. Synovialvæsken er til stede i små mengder i leddhulen og har flere viktige funksjoner:
- Smøring: Reduserer friksjonen mellom leddflatene under bevegelse. Smøreeffekten skyldes særlig hyaluronsyre og lubricin (et glykoprotein).
- Ernæring: Transporterer næringsstoffer til den avaskulære leddbrusken.
- Støtdemping: Bidrar til å absorbere støt og fordele belastning i leddet.
- Fjerning av avfallsstoffer: Fjerner metabolske avfallsprodukter fra brusk og andre leddstrukturer.
- Beskyttelse mot infeksjon: Inneholder immunceller og proteiner som bidrar til å beskytte leddet mot infeksjoner.
- Under normale forhold er synovialhinnen relativt tynn og uten vesentlig celleinfiltrasjon.
Det intraartikulære trykket er normalt lett negativt i hvileposisjon, noe som bidrar til leddstabilitet. Ved økt væskeansamling i leddet (hydrops, leddutgytelse, effusjon) blir trykket positivt. Trykket varierer også med leddets stilling; det laveste trykket oppnås ved en fleksjon på 30–40 grader.
Brusk (leddsbrusk)
Leddbrusk (cartilago articularis) er en spesialisert type bindevev som dekker leddflatene (facies articulares) i ekte ledd (diartroser). Bruskens hovedfunksjon er å dempe og fordele belastning over det underliggende benvevet og å redusere friksjon mellom leddflatene under bevegelse. Brusken tåler kompresjon, skjærkrefter og gjenvinner sin opprinnelige form etter å ha blitt trykket sammen (viskoelastisitet).
Brusken er avaskulær (mangler blodkar), alymfatisk (mangler lymfekar) og aneuronal (mangler nerver). Det begrenser bruskens evne til reparasjon og regenerasjon (Holck P, snl, 2020). Ernæring av kondrocytter skjer via diffusjon av næringsstoffer fra synovialvæsken.
Bruskens manglende regenerasjon ble observert allerede av John Hunter som slo fast “once destroyed is not repaired”. I praksis vil mindre bruskskader sjelden repareres fullstendig og kan disponere for utvikling av artrose over tid.
Oppbyggingen av brusk. Leddbrusk består av kondrocytter som er spredt i en ekstracellulær matriks (ECM). ECM består hovedsakelig av:
- Kollagen: Mest type II kollagen som danner et nettverk som gir brusken strekkfasthet. Mindre mengder av andre kollagentyper (f. eks. type IX, XI) finnes også.
- Proteoglykaner er store molekyler med en proteinkjerne bundet til glykosaminoglykaner (GAGs) som kondroitinsulfat og keratansulfat. Aggrekan er det dominerende proteoglykanet i brusk og bidrar til at brusken binder vann og motstår kompresjon.
- Vann utgjør en betydelig del av bruskens vekt og viktig for dens mekaniske egenskaper.
Brusk er en sentral struktur i de fleste ledd og spiller en viktig rolle i patogenesen ved revmatiske sykdommer som revmatoid artritt (RA) og artrose.
Subkondralt ben og tilgrensende områder
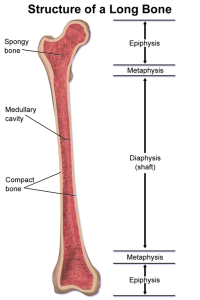
Ossøse deler
Rørknokler (ossa longa) består av tre hoveddeler:
- Epifyse (epiphysis): Den proksimale og distale enden av knokkelen. Består hovedsakelig av spongiøst benvev (substantia spongiosa) dekket av et tynt lag kompakt benvev (substantia compacta). Leddflatene (facies articulares) på epifysene er dekket av hyalin brusk (cartilago articularis).
- Metafyse (metaphysis): Overgangsområdet mellom epifysen og diafysen. Inneholder epifyseskiven (discus epiphysialis) hos barn og ungdom. Denne er ansvarlig for lengdeveksten av knokkelen. Etter vekststopp forbenes epifyseskiven og blir til en metafysær linje (linea epiphysealis). Metafysen er rik på blodkar og er et vanlig sete for infeksjoner (osteomyelitt) hos barn.
- Diafyse (diaphysis): Skaftet av knokkelen. Består hovedsakelig av kompakt benvev som omgir en marghule (cavitas medullaris) som inneholder benmarg (medulla ossium).
Metafysearteriene (arteriae metaphysiales) forsyner metafysen og epifyseskiven. Epifysearteriene (arteriae epiphysiales) forsyner epifysen. Diafysen forsynes av næringsarterien (arteria nutricia) og periostale arterier (arteriae periostales).
- Mikrostrukturen i subkondralt ben: kompakt bencortex + trabekulært (svampaktig) ben med trabekler.
- Mikroskopisk finnes osteoblaster, osteocytter (inne i benmatrix) og osteoklaster (på benoverflater).
- Kontakt med brusk og interaksjon mellom brusk og ben skjer mellom subkondralt ben og kalsifisert brusk.
Sener, ligamenter og enteser (senefester)
- Sener og ligamenter består av kompakt kollagenfibre (type I dominans), med fibroblaster (tenocyter) spredt mellom fibrene.
- Ved festet (entese) kan man se gradvis overgang: sene → fibrobrusk → mineralisert sone → ben.
- Mikroskopisk vil man finne kollagenfibriller, noe elastiske fibre, og i nærhet av entesefestet også blodkar.
Bindevev og interstitielt vev
- Bindevev generelt: fibroblaster, retikulære celler, ekstracellulær matriks bestående av kollagen (type I, III), elastiske fibre og intercellulær substans (proteoglykaner, glykosaminoglykaner).
- I leddkapselkapsel og omkringliggende strukturer finnes bindevevsforbindelser, fettvev og små blodkar.
Bindevev finnes i alle organer og bidrar til kroppens strukturelle støtte og stabilitet. Det er flere typer bindevev, hver med en spesifikk sammensetning og funksjon.
- Løst bindevev finnes mellom organer og vev (stroma). Det gir strukturell støtte og fungerer som et medium for transport av næringsstoffer og avfallsstoffer.
- Fast bindevev dominerer i sener, ligamenter, kapsler og skjelett. Det gir strekkfasthet og bidrar til kroppens mekaniske stabilitet.
- Spesielt bindevev omfatter vev med unike funksjoner f. eks. fettvev (energilagring og isolasjon). Bindevev består hovedsakelig av den ekstracellulære matriks (ECM) som er en blanding av proteinfibre (mest kollagen) og grunnsubstans som er en gel-lignende substans av glykosaminer, proteoglykaner og glykoproteiner.
Kollagener er en familie av ekstracellulære polypeptider karakterisert ved en trippelheliks struktur og et høyt innhold av aminosyrene prolin og hydroksyprolin. Det finnes minst 28 ulike kollagentyper med varierende distribusjon og funksjon.
- Type I kollagen utgjør 90 % av alt kollagen i organismen og finnes i hud, skjelett, sener og ligamenter.
- Type III kollagen forekommer i hud, blodkarvegger og synovialmembranen. Kollagenbiosyntesen er en kompleks prosess som starter med dannelsen av pre-prokollagen. Ved økt kollagenomsetning, som ved vevsskader eller reparasjon, øker serumnivåene av aminoterminale propeptider (PINP og PIIINP) og av karboksyterminale peptider (PICP). PINP er en sensitiv markør for osteoblastaktivitet og brukes i monitorering av osteoporose.
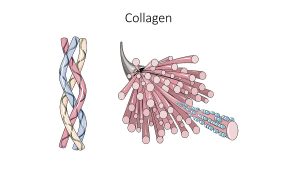
Kollagenfibrenes organisering: De lange kollagenfibrene er dannet av kollagentypene I, II, Ill, IV og XI. Korte fibre (kollagen IX, XII og XIV) forbinder de lange fibrene. Kollagen VII forankrer kollagenfibrene til basalmembranen som skiller ECM fra cellene.
Grunnsubstans i ECM:
Glykosaminoglykaner, proteoglykaner og glyko-proteiner er grunnsubstanser i bindevevet. Disse forsterker ECM og bindes til bl.a. reseptorproteiner på overflaten av celler (integriner).
- -Glykosaminoglykaner (GAGs) er lange, uforgrenede polysakkarider sammensatt av disakkaridenheter. Viktige GAGs består av hyaluronsyre, kondrontinsulfat og dermatansulfat.
- -Proteoglykaner er proteiner med kovalent bundne GAGs. Aggrecan er det dominerende proteglykanet i brusk.
- -Glykoproteiner består av oligosakkaridkjeder. Eksempler på viktige glykoproteiner i ECM er fibronektin og laminin.
Fibroblaster er de viktigste cellene i bindevevet. De syntetiserer og vedlikeholder ECM-komponentene som kollagen, elastin, proteoglykaner og vekstfaktorer. Fibroblaster kan differensieres til myofibroblaster, som har kontraktile egenskaper og bidrar til sårtilheling.
Blodårer
Blodårer danner et nettverk av rørstrukturer som transporterer blod, oksygen og næringsstoffer til alle deler av kroppen. De er avgjørende for fysiologisk likevekt og overlevelse. Blodårene deles inn i arterier, vener og kapillærer (mikroskopiske kar som forbinder arterier og vener og muliggjør utveksling av gasser, næringsstoffer og avfallsstoffer mellom blod og vev). Blodårenes vegg er alle bygd opp av tre lag, hver med spesifikk funksjon:
- Tunica intima: Det innerste laget er laget og er sammensatt av endotelceller som er glatte celler som sørger for en jevn blodstrøm.
- Tunica media: Det midterste laget er laget av muskelceller og elastiske fibre som gir blodårene styrke, fleksibilitet og motstand mot trykkendringer.
- Tunica adventitia: Det ytterste laget består av bindevev som gir strukturell støtte, beskytter blodårene og forankrer dem til omliggende vev.
Blodårene transporterer arterielt, oksygenrikt blod fra hjertet til alle deler av kroppen, næringsstoffer fra fordøyelsessystemet til vevene og avfallsstoffer fra vevene til lungene og nyrene, hvor de skilles ut fra kroppen. I tillegg transporteres hormoner fra kjertlene til målorganene. Blodårene hjelper også til med å regulere kroppstemperaturen ved å utvide eller trekke seg sammen og dermed regulere blodstrømmen til huden.
2. Patologiske prosesser (makro- og mikroskopiske) ved revmatiske sykdommer
Når revmatiske sykdommer rammer vevene, skjer en rekke patologiske endringer. Noen av disse er felles (f. eks. synovitt), mens andre er mer sykdomsspesifikke.
Synovitt og artritt
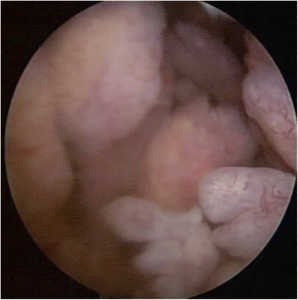
Artritt er en generell betegnelse for en inflammatorisk tilstand i et ledd. Synovitt er inflammasjon i synovialhinnen som er det indre laget av leddkapselen i ekte ledd. I klinisk praksis brukes ofte begrepene artritt og synovitt om hverandre, spesielt når det refereres til inflammatoriske leddsykdommer.
Makroskopisk blir synovium tykt, rødlig og villøst. Overflaten kan vise villøse folder eller polypplignende strukturer. Leddhulen kan inneholde mer væske (eksudat) og fibrin.
Patologiske forandringer i synovialhinnen gjenspeiles også i synovialvæskens sammensetning. Ved inflammasjon i synovialhinnen (synovitt) ses:
- Økt permeabilitet: Økt lekkasje av væske og proteiner fra kapillærene til leddvæsken.
- Endret sammensetning: Økte nivåer av proinflammatoriske cytokiner (som TNF-α, IL-1, IL-6), enzymer (som MMP) og andre inflammatoriske mediatorer.
- Hydrops: Økt produksjon av synovialvæske.
Patologisk synovialvæske ved artritt kjennetegnes av forhøyede nivåer av proinflammatoriske cytokiner som både initierer og vedlikeholder synovial inflammasjon. Forskning på synovialvæske har bidratt til utviklingen av en rekke effektive legemidler som spesifikt hemmer proinflammatoriske cytokiner (McInnes IB, 2007; Orr C, 2017).
Det er viktig å skille artritt fra artrose (osteoartritt, engelsk: “arthritis/osteoarthritis”) som er en degenerativ leddsykdom med en mindre uttalt inflammatorisk komponent.
Synovialhinnen med de fibroblastlignende synoviocyttene (type B synoviocytter) er et målorgan for immunologiske angrep ved mange inflammatoriske revmatiske sykdommer som revmatoid artritt og psoriasisartritt. Selv ved artrose spiller synovitt en rolle i sykdomsprogresjonen (Orr C, 2017).
Mikroskopisk/histologisk kjennetegnes synovitt av:
- Hyperplasi av synoviocytter og økt proliferasjon av synoviocyttene i synovialhinnen.
- Inflammatoriske celleinfiltrasjon: Infiltrasjon av immunceller i synovialvevet, inkludert T- og B-lymfocytter, plasmaceller, makrofager, nøytrofile granulocytter, mastceller, NK-celler (natural killer cells) og dendrittiske celler.
- Angiogenese: Nye blodkar dannes i synovialhinnen. Dette bidrar til økt tilførsel av inflammatoriske celler og mediatorer (Mullan RH, 2007).
- Ødem: Opphopning av væske i synovialvevet.
På cellenivå bidrar proinflammatoriske cytokiner som tumornekrosefaktor-alfa (TNF-α), interleukin-1 (IL-1) og interleukin-6 (IL-6) til nedbrytning av ekstracellulær matriks (ECM) i brusk og benvev. Dette kan føre til dannelse av pannus som er et prolifererende inflammatorisk vev som vokser inn over leddbrusken og kan forårsake erosjoner i det underliggende benvevet (Mullan RH, 2007). Heterogenitet i synovialvevet med ulike subpopulasjoner av immunceller og synoviocytter med varierende funksjoner kan bidra til de ulike kliniske fenotypene som observeres ved revmatoid artritt (Bhamidipati K, 2022).
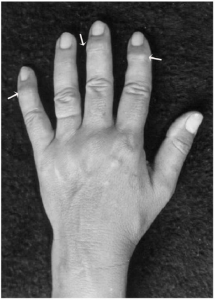
Pannus referer til proliferasjon av inflammatorisk vev som sprer seg fra synovialhinnen til leddbrusken. Pannus består av en blanding av inflammatoriske celler (makrofager, fibroblastlignende synoviocytter, dendrittiske celler, plasmaceller, mastceller) og granulasjonsvev. Pannus kan forårsake betydelig skade på brusk og benvev og bidrar til utvikling av erosjoner og ledddestruksjon (Jang S, 2022). Pannus kan visualiseres ved artroskopi, MR og ultralydundersøkelser.
Artritt-sykdommer
Det finnes mange artrittsykdommer. Noen viktige kategorier er:
- Autoimmune artrittsykdommer: Revmatoid artritt (RA),juvenil artritt (barneleddgikt, JIA), spondyloartritter (ankyloserende spondylitt/Bekhterevs sykdom, psoriasisartritt, reaktiv artritt, enteropatisk/IBD-relatert artritt).
- Krystallartritter: Urinsyregikt (podagra), kalsiumpyrofosfatartritt (kondrokalsinose/pseudogikt).
- Infeksiøs artritt (septisk artritt): Forårsaket av mikroorganismer (bakterier, virus, sopp).
- Artrose (osteoartritt): Selv om artrose primært er en degenerativ leddsykdom, spiller inflammasjon (synovitt) en rolle, spesielt i senere stadier.
Symptomer på artritt og andre kliniske forhold er beskrevet i en egen del i boken som omhandler artrittsykdommer.
Bruskskade (lesjoner i Cartilago articularis) og degenerasjon
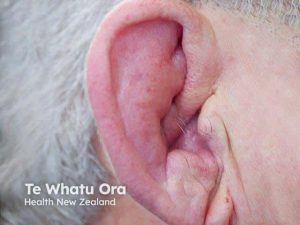
Bruskskade kan ha flere årsaker:
- Mekanisk overbelastning: Akutte traumer som slag eller vridninger eller kroniske, repeterte belastninger.
- Inflammatoriske prosesser: Ved inflammatoriske leddsykdommer (f. eks. revmatoid artritt) frigjøres proinflammatoriske cytokiner (som tumornekrosefaktor-alfa (TNF-α), interleukin-1 (IL-1), interleukin-6 (IL-6) som bidrar til nedbrytning av ECM og kondrocytter.
- Genetisk predisposisjon øker risikoen for bruskskade og utvikling av artrose.
- Andre faktorer: Alder, fedme og metabolske faktorer (diabetes, hemokromatose) kan også spille en rolle.
Makroskopisk kan brusken kan bli tynnere, fliset eller erodert. Overflaten kan bli ujevn med sprekker eller fullstendige defekter. Dersom brusklaget er delvis eller helt tapt, vil underliggende ben bli utsatt for mekanisk stress og skade.
På cellenivå induserer cytokiner nedbrytning av ECM ved å stimulere produksjonen av matrixmetalloproteinaser (MMP) som er enzymer som bryter ned kollagen og proteoglykaner. Histologisk ses:
- Redusert antall og funksjon av chondrocytter
- Nedregulert produksjon av kollagen II og proteoglykaner
- Økt aktivitet av degradative enzymer (metalloproteinaser, kollagenaser etc.)
- Apoptose av chondrocytter
- Fragmenter av matriks og kollagen i leddhule
- Endringer i gradienten fra ikke-mineralisert til mineralisert brusk
Det pågår omfattende forskning for å forstå mekanismene bak bruskskade bedre med mål om å utvikle effektive legemidler (Tateiwa D, 2019).
Andre brusksykdommer: I tillegg til bruskskader relatert til traume og inflammasjon, artrose, relapsing polykondritt og kondromalasi av andre årsaker finnes det andre brusksykdommer:
- Kondrodysplasier: En gruppe genetiske sykdommer som påvirker utviklingen av brusk og ben.
- Kondromer: Benigne (godartede) svulster som oppstår fra bruskvev.
- Kondrosarkomer: Maligne (ondartede) svulster som oppstår fra bruskvev.
Behandlingen av bruskskade avhenger av alvorlighetsgraden og årsaken til skaden. Regenerering av hyalin brusk er fortsatt en stor utfordring i klinisk praksis. Mye forskning fokuserer på å utvikle nye metoder for å stimulere bruskreparasjon og forebygge utvikling av artrose.
Konservativ behandling
- Tilpasset trening: For å styrke muskulaturen rundt leddet og forbedre stabiliteten.
- Vektreduksjon: Ved overvekt for å redusere belastningen på leddene.
- Smertelindring: Med analgetika (f. eks. paracetamol, NSAIDs) og eventuelt intraartikulære kortikosteroidinjeksjoner.
- Fysioterapi: For å forbedre bevegelighet, styrke og stabilitet.
Kirurgisk behandling: Vurderes i utvalgte tilfeller (Katz JN, 2022), f. eks. ved større bruskskader, løse bruskfragmenter eller ved manglende effekt av konservativ behandling. Kirurgiske metoder inkluderer:
- Artroskopisk debridement: Fjerning av løst bruskvev og utjevning av ujevnheter.
- Mikrofrakturering: Stimulering av benmargen for å danne fibrobrusk.
- Mosaikkplastikk (osteokondral transplantasjon): Overføring av bruskplugger fra et lite belastet område til det skadede området.
- Autolog kondrocyttransplantasjon (ACT): Dyrking av pasientens egne kondrocytter og reimplantering i det skadede området.
Eksperimentelle metoder
- Stamcelleterapi: Bruk av stamceller (f.eks. mesenkymale stamceller fra benmarg eller fettvev) for å forsøke å regenerere brusk (Gorgan S, 2022; Jeng L, 2011).
- Injeksjoner med plateberiket plasma (PRP): Injeksjon av konsentrert blodplater som inneholder vekstfaktorer. Effekten av PRP er fortsatt omdiskutert og evidensgrunnlaget er begrenset (Benell KL, 2021; Ekås GR, 2015).
- Vekstfaktorer og hormoner: Forskning pågår for å undersøke potensialet for bruk av vekstfaktorer og hormoner for å fremme bruskvekst, men dette er foreløpig ikke etablert som standardbehandling (Weng C, 2021).
Erosjoner i subkondralt ben/benresorpsjon
Makroskopisk: arr-like defekter i ben (“erosjoner”) på røntgen eller MR, tap av benmasse nær leddflater.
Mikroskopisk:
- Osteoklaster (aktive) sitter i resorpsjonslakuner
- Osteoklast‐mediert resorpsjon av benmatrix
- Lokal benavspaltning, osteolyse
- I områder med pannus‐kontakt: direkte beninvasjon av den synoviale proliferasjonen
- Mikrofrakturer i benstruktur
- Reaksjoner i kantsoner (periartikulær sklerose, remodellering)
Eksempler på revmatiske sykdommer som kan angrepet benvevet og føre til ulike typer skader:
- Osteoporose: Redusert benmasse og skadet mikroarkitektonisk svekker benvevet, noe som øker risikoen for frakturer. Osteoporose kan være primær (f. eks. postmenopausal osteoporose) eller sekundær til andre sykdommer eller medikamentbruk (f. eks. kortikosteroider, revmatoid artritt).
- Revmatoid artritt (RA): Inflammasjon i synovialhinnen (synovitt) kan spre seg til det underliggende benvevet og forårsake usurerende skader (erosjoner) i leddnære områder. Disse erosjonene er karakteristiske radiologiske funn ved RA.
- Juvenil artritt (JIA): Kan føre til overvekst i epifysene (hypertrofi) i affiserte ledd på grunn av økt blodtilførsel og stimulering av vekstsonene. Dette kan resultere i lengdeforskjell mellom ekstremiteter.
- Infeksiøs osteomyelitt: En infeksjon i benvevet er oftest forårsaket av bakterier (f. eks. staphylococcus aureus). Barn rammes oftest i metafysen på grunn av den rike blodtilførselen der. Infeksjonen kan føre til rask destruksjon av benvev og utvikling av abscesser.
- Systemiske bindevevssykdommer: Ved systemiske bindevevssykdommer som systemisk lupus erythematosus (SLE) er artritten oftest ikke-destruktiv (uten radiologiske erosjoner). Dette skiller SLE fra RA, hvor erosjoner er et typisk funn. Imidlertid kan SLE predisponere for osteonekrose (bennekrose), spesielt ved bruk av kortikosteroider.
Andre skjelettsykdommer med betydning for revmatologien:
- Histiocytose: En gruppe sykdommer som kjennetegnes av unormal proliferasjon av histiocytter (en type immuncelle). Kan føre til destruktive lesjoner i benvevet.
- Paget sykdom (Osteitis deformans): En kronisk bensykdom som kjennetegnes av unormal benomsetning, med både økt benresorpsjon og økt bennydannelse. Dette fører til deformerte og skjøre knokler..
Fibrotisk ombygging, kapsel‐ og ligamentfortykkelse
Makroskopisk kan leddkapsel kan bli tykk og stram, ligamenter og leddbånd kan forkortes eller stivne, leddrommet kan innsnevres.
Mikroskopisk:
- Proliferasjon av fibroblaster og myofibroblaster
- Økt kollagenproduksjon (spesielt type I og III) og andre matrikskomponenter
- Redusert elastisitet og økt stivhet i kapsel og ligamenter
- Små blodkar og fibrotiske endringer i karvegg
- Inngrodd fibrin og arrvevsdannelse
Dette fører til redusert mobilitet og stivhet som kan være irreversibel i fremskredne sykdommer.
Systemiske bindevevssykdommer
Systemiske bindevevssykdommer er en heterogen gruppe autoimmune sykdommer karakterisert ved kronisk inflammasjon og vevsskade i bindevevet. Patogenesen involverer en dysregulert immunrespons med autoantistoffdannelse og immunaktivering. Symptomene på bindevevssykdommer kan variere mye avhengig av typen sykdom og hvilke organer som er rammet. Typiske systemiske bindevevssykdommer inkluderer systemisk lupus erythematosus (SLE), Sjøgrens sykdom, MCTD, myositt og systemisk sklerose.
- Vennligst les mer om systemiske bindevevssykdommer i egen del av boken.
Kar‐ og vaskulære forandringer (i ledd og organsystemer). Vaskulitt.
I revmatiske sykdommer kan blodkar i og omkring ledd og annet vev også rammes:
- Endotelial aktivering og skade
- Økt karpermeabilitet, lekkasje av plasma og proteiner
- Neovaskularisering (spirende kar i synovium og pannus)
- Perivasculær infiltrasjon av betennelsesceller
- Mikrovaskulær iskemi og fibrose i alvorlige tilfeller
- I vaskulittkomplekser: vaskulær nekrose, fibrinutfelling, trombedannelse
Slike forandringer kan både være sekundære til lokal inflammasjon og direkte del av sykdomsmekanismer i systemisk revmatisk sykdom.
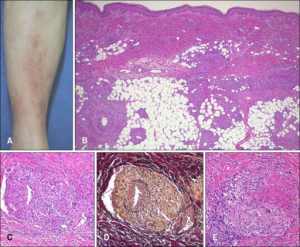
Vaskulitt kan defineres som en inflammasjon i selve karveggen. Inflammasjonen kan føre til vegg-nekrose, lumenforsnevring (stenose) og trombose. Vaskulitt kan være lokalisert overfladisk til hud (kutan vaskulitt) eller dypere hudlag og indre organer (systemisk vaskulitt). Ofte brukes betegnelsen synonymt med arterieinflammasjon (arteritt), men vaskulitt omfatter egentlig vegg-inflammasjon av alle typer kar, også vener.
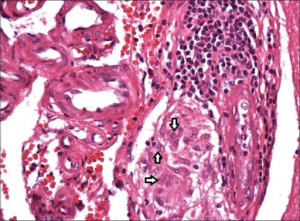
Histologiske forandringer ved vaskulitt. Karakteristisk for vaskulitt er ødematøst endotel, fibrinutfelling i karveggen, granulocytter i karveggen, kjernefragmenter perivaskuIært (leukocytoklase) og ekstravaserte erytrocytter. For diagnosen vaskulitt kreves betennelsesceller i karvegg og endotelskade. Beste bevis på endotelskade er ekstravasering. Med fibrinoid nekrose menes akkumulering av proteiner (fibrin) i karveggen som ses ved flere typer kar-skader.
-Kjempeceller er store, flerkjernede celler som kan observeres ved flere typer vaskulitt, blant annet ved temporalis arteritt (kjempecelle arteritt).
-Leukocytoklastisk vaskulitt betegner alle lesjoner hvor det kan påvises fragmenter av leukocytter (kjernestøv = nukleær dust) (leukocytoklase). Kan ha multiple årsaker (Bouiller K, 2016).
-Nekrotiserende vaskulitt kjennetegnes ved veggdestruksjon og fibrinoid degenerasjon, neutrofil infiltrasjon av celleveggen og perivaskuIær blødning og leukocytoklase.
-Granulomatøs arteritt og granulomer. Et granulom er et fokalt område med granulomatøs betennelse. Granulomatøs arteritt karakteriseres av granulomer eller granulomatøs betennelse. Sistnevnte defineres som en kronisk betennelse hvor den dominerende celletypen er aktiverte makrofager med epitelliknende utseende (epiteloide celler). Granulomatøs betennelse ses ved sarkoidose, infeksjoner, GPA (sammen med fibrinoid nekrose). Vennligst les om vaskulitt i en egen del av kompendiet.
3. Klinisk betydning og relasjon for behandling
Ved å forstå de anatomiske og histologiske forandringene kan vi bedre skjønne hvorfor tidlig behandling er viktig, og hvordan ulike terapier virker eller bør virke.
Diagnose og vurdering av vevsskade
- Bildediagnostikk (MR, ultralyd, røntgen) kan identifisere synovialfortykkelse, pannus, erosjoner og benforandringer.
- Synovialbiopsi eller vevsprøve kan gi sikre bevis for graden av synovitt, celleinfiltrasjon og pannusvitalitet.
- Histologiske vurderinger (grad av fibrose, vaskularisering, celleinfiltrasjon) kan korrelere med sykdomsaktivitet og prognose.
- Mikroskopisk funn tidlig kan være prediktive for strukturell progresjon.
Behandlingsmessig betydning
- Behandling bør målrette synovitt og hemme proliferasjon av synovialvev før pannusinvasjon blir etablert.
- Antiinflammatoriske og immunmodulerende legemidler kan begrense hyperplasi, angiogenese og celleinfiltrasjon.
- Beskyttelse av brusk: ved å hemme degraderende enzymer og støtte kondrocyttfunksjon.
- Beskyttelse av bensubstans: redusere osteoklastaktivitet og hemme erosjonsdannelse.
- Begrense fibrose: tidlig behandling hindrer overgangen til irreversibel vevsombygging.
- Behandling av vaskulære komponenter dersom karaffeksjon/vaskulitt foreligger.
Prognostiske faktorer
- Jo tidligere man klarer å stanse inflammatoriske/ proliferative prosesser, desto mindre strukturell skade.
- Tilstedeværelse av erosjoner ved diagnose er en ugunstig prognostisk faktor.
- Vedvarende aktiv sykdom gir høy risiko for fibrotiske sluttilstander og irreversibel vevsskade.
- Behandling må balansere effekt mot bivirkninger og må tilpasses sykdomsstadium.
4. Oppsummering: normal vs patologisk
| Struktur / vev | Normal tilstand (makro- og mikroskopisk) | Patologisk forandring i revmatisk sykdom | Klinisk / terapeutisk betydning |
|---|---|---|---|
| Synovium | Tynt intima, få celler, lav vaskularitet. | Hyperplasi, celleinfiltrasjon, angiogenese, dannelse av pannus | Behandling bør fokusere på å dempe synovitt før invasjon |
| Brusk | Få kondrocytter, rik matriks, ingen kar. | Nedbrytning av matriks, kondrocytt-apoptose. | Beskytt brusk før defekter blir irreversible |
| Subkondralt ben | Kompakt + trabekulært ben, balanse mellom nedbrytning og bygging. | Erosjoner, osteoklast-aktivitet, lav benmasse. | Begrens benødeleggelse ved antiresorptive tiltak |
| Kapsel, ligamenter, bindevev | Elastisk bindevev, normal kollagenstruktur. | Fibrose, fortykkelse, redusert elastisitet. | Tidlig behandling for å unngå stivhet og kontraktur. |
| Blodkar | Små kapillærer, normal permeabilitet. | Endotelial skade, lekkasje, neovaskularisering, vaskulitt. | Vurder karbeskyttelse og behandling av karinvolvering. |
