BINDEVEVSSYKDOMMER (REV 021-033)
63 Systemisk sklerose (SSc). Sklerodermi (REV 021)
Øyvind Palm and Jan Tore Gran
Kjennetegn på systemisk sklerose
Raynauds fenomen med debut i voksen alder.
Hovne/”puffy” fingre ved debut, stramhet i huden, særlig på fingre (sklerodaktyli).
Antistoff hos> 50%: CENP, Scl-70 og RNP-polymerase III er karakteristiske, men foreligger ikke hos alle.
Alvorlige organmanifestasjoner omfatter skleroderma renal krise, pulmonal hypertensjon, lungefibrose og GAVE (gastric antrum vascular ectasia).
Diffus kutan systemisk form og begrenset form har ofte ulike forløp.
Diagnosekoder ICD-10: M34.0 (diffus form), M34.1 (begrenset form/CREST). (J99.1*) Lungeaffeksjon† ; M34.9 Uspesifisert systemisk sklerose
Prosedyrekoder: 6-minutter gangtest: FYFX05. Kapillærmikroskopi: PKFT00. EKG: FPFE15
ATC koder (for legemiddelstatistikk): L04A A Immunsuppressive legemidler:
Nøkkelord for journalskriving ved systemisk sklerose
Diagnosen basert på..
- Raynauds fenomen (bi-eller trifasisk)
- Puffy/hovne fingre
- Sklerodaktyli
- Distalt eller proksimalt for MCP-ledd
- Proksimalt for albuer/knær (diffus form)
- Truncus (diffus form)
- Ulcera eller på pitting scars/arr/skorper fingerpulpa
- Telangiektasier på hud og lepper
- Kapillaroskopi patologisk
- Pulm hypertensjon (ekko, hø. kateter)
- Interstitiell lungesykdom
- Antistoff: CENP, ScL70, RNA Polymerase III)
- Dysfagi – påvist røntgenologisk
- Tendon friction rub (krepitasjoner) påvist
- Renal krise eller annen hypertensjon
- Malabsorpsjon, diare eller inkontinens
- Rodnan skin score ved siste konsultasjon
Tidspunkt for sykdomsdebut
Hensikten med konsultasjonen
Definisjon
Systemisk sklerose (SSc, systemisk sklerodermi) er en sjelden autoimmun bindevevssykdom som kjennetegnes av progredierende fibrose i hud, underhud og indre organer (Del Gado F, 2025).
Sykdommen rammer både kvinner og menn i alle aldre. Forløpet er individuelt forskjellig og dessuten avhengig av hvilken hovedtype som foreligger. SSc kan deles inn i to hovedtyper:
Begrenset kutan form (begrenset SSc). Denne typen rammer kun huden på hender, føtter og omkring munnen. Den er ofte assosiert med kalsinose, Raynauds fenomen, øsofagusdysmotilitet, sklerodaktyli og teleangiektasier (CREST syndrom), samt CENP (anti-centromer) antistoff. Lunger og hjerte er blant indre organer som også kan angripes i forløpet.
Diffus SSc (dcSSc): Denne typen kan ramme huden på hele kroppen. Den kan involvere indre organer, oftest øsofagus, lunger, hjerte og nyrer. Den er ofte assosiert med Anti-Scl70-antistoffer (anti-topoisomerase I-antistoffer) (Volkmann ER, 2023).
Dersom sykdommen den begynner hos barn, kalles den juvenil systemisk sklerose.
Systemisk sklerose skilles fra non-systemisk sklerodermi (morfea, lineær sklerodermi) som angriper huden, men ikke indre organer (Volkmann ER, 2023; Adigun R, 2024).
Historikk
I 1753 beskrev legen Carlo Curzio fra Napoli en 17 år gammel pike (Patrizia Galiera) med en tilstand som mest sannsynlig var systemisk sklerose (Mackay IR, Rose NR, 2006).
Maurice Raynaud beskrev i 1863 sammen med Jonathan Hutchinson i 1883 en sammenheng mellom Raynauds fenomen og sklerodermi. Betegnelsen sklerodermi ble foreslått i 1847.
Den første hudbiopsien ble beskrevet av Kohn (Kaposi) i 1869. Han konkluderte med at årsaken var fortykket lymfe i hudens bindevev (Kaposi M. Pathologie und Therapie der Hautkrankheiten. 4th ed. Vienna, Austria: Urban & Schwarzenberg, 1893).
Et CREST-lignende syndrom ble først beskrevet i 1910 (Thibierge-Weissenbachs syndrom). I 1957 beskrev en gruppe fra Mayoklinikken i USA ulike typer sklerodermi, inkludert systemisk sklerose. De påpekte funn av fibrosis og skleroserende kollagenfibre, samt negative tester for mucin (som ses ved differensialdiagnosen skleromyksødem) (O’leary P, 1957).
Rodnan publiserte I 1979 en skåringsmetode for manifestasjon i huden (Rodnan GP, 1979). Metoden som fortsatt er mye brukt er en “modifisert Rodnan skin score (mRSS)” (Brennan P, 1992). Norske epidemiologiske data, basert på en befolkningsbasert studie i Sør-Øst Norge, ble publisert i 2012 (Hoffmann-vold A-M, 2012).
Epidemiologi
Systemisk sklerose angriper fire ganger så mange kvinner som menn og vanligste debutalder er i 30-60 årene. Den forekommer en sjelden gang blant barn (Juvenil systemisk sklerose), og da som diffus type (dcSSc). Epidemiologiske data viser noe varierende resultater.
Prevalensen i sør-øst Norge er beregnet til 9,9 per 100 000 (begrenset form 6,9/100.000, diffus form 1,8 per 100 000) med en gjennomsnittsalder ved debut på 47 år (Hoffmann-vold A-M, 2012). Svenske registerdata fant en samlet prevalens på 22.7 per 100 000 og insidensen var 11.9 per 1 000 000 person-år (Westerling H, 2022). Den diffuse formen (dcSSc) begynner oftest blant relativt unge, mens den begrensede formen er vanligere i litt høyere alder. Gjennomsnittsalder ved sykdomsdebut er 47 år (Hoffmann-vold A-M, 2012).
Etiologi
Genetiske disponerende faktorer er undersøkt i tvillingstudier og i store, multisenter hel-genom/genome-wide association studier (GWAS). Man har identifisert flere gener som er involvert i reguleringen av inflammasjon og immunrespons og som antas å bidra til sykdomsdisposisjon. Spesifikke HLA-gener er assosiert med økt risiko og ulike kliniske fenotyper av SSc. Dette understreker kompleksiteten i den genetiske arkitekturen bak sykdommen. (Feghali-Bostwick C, 2003; Broen JCA, 2014).
Miljøfaktorer kan også være av betydning, spesielt hos genetisk disponerte individer. Flere stoffer i miljøet er assosiert med sklerodermi-lignende sykdommer eller med økt risiko for SSc. Disse inkluderer:
- Silikastøv: Yrkeseksponering for krystallinsk silikastøv (silisiumdioksid, SiO2) er assosiert med økt forekomst og alvorlighetsgrad av SSc, spesielt hos menn. Dette er observert i yrker som gruvedrift, sandblåsing og anleggsarbeid.
- Organiske løsemidler: Eksponering for visse organiske løsemidler (toluen, xylen, trikloretylen, vinylklorid) øker også risikoen for SSc. Disse stoffene finnes i ulike industrielle omgivelser.
- Medikamenter: Enkelte legemidler er også assosiert med utvikling av sklerodermi-lignende tilstander. Disse omfatter bleomycin, pentazocin og L-tryptofan (som forårsaket eosinofili-myalgi syndrom etter inntak av forurensede kosttilskudd).
- Forurensede matvarer: Den mest kjente koblingen mellom skadede matvarer og sklerodermi-lignende sykdom er “Toxic Oil Syndrome” i Spania på 1980-tallet. Denne tilstanden ble forårsaket av forfalsket olivenolje som egentlig var kjemisk modifisert rapsolje tiltenkt industriell bruk. Et sentralt giftstoff var oleoylanilid. Av de ca. 20 000 personene som ble forgiftet, døde flere hundre og 10-15% (2-3000) fikk morfea-lignende hudforandringer, ofte kombinert med polynevropati og myositt.
Andre etiologiske faktorer som har blitt foreslått, men som ikke er avklart inkluderer:
- Silikonimplantater: Det har lenge vært bekymring for en mulig kobling mellom silikonbrystimplantater og SSc, men omfattende studier har i stor grad tilbakevist denne mulige assosiasjonen.
- Infeksjoner: Visse infeksjoner (helicobacter pylori, cytomegalovirus/CMV) er under utredning for en potensiell rolle i SSc-patogenesen.
- Tobakkrøyking: Selv om røyking forverrer vaskulære symptomer (Raynauds fenomen) er det ikke etablert en direkte årsakssammenheng med initiering av SSc.
Den eksakte sykdomsårsaken er ikke funnet, men det sannsynlig at en kombinasjon av genetisk disposisjon og uheldig påvirkning av en eller flere miljøfaktorer sammen kan trigge en autoimmun respons med påfølgende fibrose og utløse sykdommen (Rosendahl A-H, 2022).
Patogenese
Typiske patofysiologiske forandringer ved systemisk sklerose kan ses allerede ved rutinemessig histologisk undersøkelse: Tidlig i forløpet ses ødematøse forandringer i endotelceller. Deretter oppstår lymfohistiocytiske inflammatoriske infiltrater rundt affiserte blodkar. Senere dannes depoter av ekstracellulær matriks med aktiverte myofibroblaster og homogene kollagen bunter (Rosendahl A-H, 2022).
Tre patologiske forandringer kjennetegner SSc:
- Fibroblast dysfunksjon fører til økt deponering av ekstracellulær matriks.
- Vaskulære forstyrrelser (vaskulopati) gir vevshypoksi.
- Immunresponsen kjennetegnes av patologisk T- og B-Iymfocytt-funksjon og produksjon av auto-antistoffer.
Sannsynligvis er den initiale hendelsen en endotelskade i mikrokar og små muskulære arterier. Dette fører til tap av kapillærer (destruktiv vaskulopati). En dysfunksjon i både angiogenese og vaskulogenese fører til sykdomsutvikling:
Angiogenese er dannelse av nye kar ved såkalt “sprouting”-dannelse med utgangs-punkt i allerede eksisterende kar.
Vaskulogenese er dannelse av nye kar utgående fra sirkulerende progenitor-celler. Denne er uavhengig av eksisterende kar. Selv om de fleste proangiogenetiske faktorene ved SSc er oppregulert (VEGF, vascular endothelial growth factor), kan de ikke oppveie økningen i angiostatiske faktorer. Således oppstår tap av kapillærer. En alternativ teori er at kapillærtapet ikke skyldes redusert mengde dannelse av nye kar, men feil i modningen av disse. Kapillærtapet gir uansett kliniske symptomer som akrocyanose og digitale ulcera, og vaskulær remodellering kan forårsake pulmonal arteriell hypertensjon og skleroderma nyrekrise. Hvilken rolle autoantistoffer som topoisomerase-1 (Slc-70) og anticentromer antistoffer (CENP) spiller for den tidlige inflammasjonen og påfølgende endotelskade er ennå ukjent.

Endotelskaden medfører vaskulær remodellering med hypertrofi av intima og media, samt fibrose av adventitia. Disse forandringene fører til gradvis forsnevring av karlumen og obliterasjon. Denne proliferative vaskulopatien medieres av for eksempel økt produksjon av endotelin, redusert NO syntetase-produksjon og nedsatt frigjøring av prostacycliner.
Økt fibrosering er karakteristisk for SSc og består av en ukontrollert fibroblast-produserte kollagen og andre ekstra-cellulære matriks (ECM)-proteiner. De kollagene fibre deponeres i den retikulære delen av dermis. Tidlige hudforandringer omfatter ødem, perivaskulære infiltrater og degenerering av kollagene fibre.
De patologiske forandringene er de samme for alle angrepne organer. Det er den akkumulerte mengden proteiner i ECM som forstyrrer vevet og kan medføre organsvikt. Prolifererende fibroblaster kan påvises i nærheten av endotelskaden. I tillegg aktiveres og differensieres mesenkymale progenitorceller, epitelceller og endotelceller til fibroblaster som forsterker den fibroserende prosessen. Fibroblastene transformeres til myofibroblaster som har kontraktile egenskaper. Det patologiske sluttresultatet er atrofi og sklerose av affisert vev (Kormann B, 2019).
Symptomer
Symptomene ved den begrensede formen av SSc/CREST skiller seg noe fra den diffuse formen (dcSSc). Den største forskjellen er utbredelsen av hudfortykkelsen. Den begrensede formen angriper huden bare distalt for albuer og knær og rundt munnen, mens den diffuse form også kan ramme huden proksimalt for albuer og knær og på truncus. Pasienter med diffus form har oftest også en raskere progresjon av hudsykdommen og en høyere risiko for tidlig og alvorlig involvering av indre organer.
Ved begrenset form debuterer organmanifestasjonene oftest i senfasen (etter fem år eller lengre tids sykdom). Samtidig preges sykdommen av stabile hudforandringer (fibrose) og lite uttalte allmennsymptomer. Ved diffus form (dcSSc) ses organmanifestasjoner ofte tidligere, særlig i de første to årene etter sykdomsdebut.
Allmenn-symptomer som tretthet/fatigue, vekttap og uspesifikke ledd- og muskelsmerter er vanlig, spesielt ved dcSSc.
Huden angripes hos nær 100 % av pasienter med systemisk sklerose. Sklerodermi sine skleroderma er et unntak. De fleste av disse ligner begrenset SSc, men uten sikker hudaffeksjon (Lescoat A, 2023; Angelis R, 2023).
Hudforandringene starter vanligvis distalt på fingrene. Ødematøse forandringer (“puffy”) er tegn på tidlige, typiske mikrovaskulære forandringer. Hudtykkelse og utbredelse av hudmanifestasjonene kan registreres ved modifisert Rodnan hudscore (mRSs). Huden blir i forløpet fortykket og stram, ofte med sprekk-dannelser og digitale ulcera kan oppstå sentralt på fingerpulpa eller over fingerleddene (Staroni A, 2021). Områder med de- eller hyperpigmentering (“salt og pepper”) kan ses i forløpet, særlig ved den diffuse formen. Ved begrenset form kan pasienten ha Raynauds fenomen i mange år før huden affiseres. Ved diffus form (dcSSc) utvikles Raynauds uker til få år før, samtidig med eller like etter hudmanifestasjonene. Raynauds fenomen forekommer hos nesten alle pasienter. Klassisk Raynauds med avblekning, cyanose og reaktiv hyperemi ved temperaturfall. To av tre symptomer skal være til stede. I løpet av sykdommen inntreffer ofte en mer permanent kompromittering av mikrosirkulasjonen. Det kliniske bildet blir da mer lik akrocyanose.
Raynauds fenomen er det klassiske første symptomet på systemisk sklerose. Imidlertid er Raynauds fenomen veldig vanlig også i befolkningen (ca. 5%) (Chen A, 2024) og således lite sykdomsspesifikt. Typisk ved SSc er imidlertid at Raynauds fenomen oppstår i voksen alder og øker gradvis i intensitet. Ved SSc begrenset form er latenstiden mellom debut av Raynauds fenomen og andre symptomer gjennomsnittlig 5 år. Tilsvarende for diffus form (dcSSc) er kortere: 1-2 år. Individuelle variasjoner er imidlertid betydelig (Walker UA, 2007; LeRoy EC, 1988). Initialt sees den klassiske triaden med avblekning, cyanose og reaktiv hyperemi. Med tiden dominerer ofte cyanosen (“blue attacks”). Ved uttalt Raynauds fenomen kan fingre og tær få iskemiske sår (ulcera, se nedenfor) med påfølgende substanstap distalt.
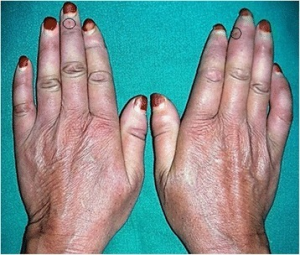
Puffy hands/fingers preges ved diffus form av raskt innsettende hudforandringer: ødem (“puffy hands”, dvs. diffus ødematøs hevelse). Ved begrenset form kan forandringene utvikle seg over flere år. Symptomene begynner gjerne distalt i hender for så å bre seg proksimalt. Vanligvis utvikles forandringene på flere fingre på begge hender omtrent samtidig. Huden føles litt stram og fingrene kan være vanskelige å strekke helt ut. “Bowed fingers” er et tidlig tegn. Årsaken er endotel dysfunksjon, slik som også ved Raynauds fenomen og kutane ulcerasjoner (Zania-Silva DC, 2021). En bør være oppmerksom på at puffy hands og Raynauds fenomen også er karakteristisk for MCTD.
–“Scleroderma neck sign” angir tilstedeværelsen av et stramt bånd over platysma ved hyperekstensjon av nakken. Forekommer ved diffus form og kan palperes hos over 90 %.
-Roman breastplate. Senere kan truncus affiseres (“Roman breastplate”) ved diffus form.
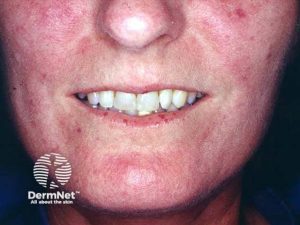
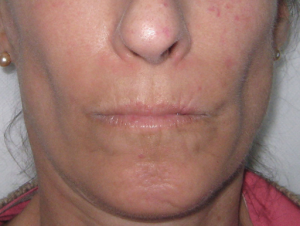
–Karpemunn utvikles ved affeksjon av munn og periorbalt vev, ofte ved begrenset form.
-Tendon friction rub palperes som “kram snø” og signaliserer alvorlig sykdom. Forekommer oftest ved aktiv, diffus kutan sykdom.
-Digitale ulcera er vevs-lesjoner som kan utvikles til nekrose og som involverer epidermis, dermis og subkutant vev. Ischemiske sår utvikles hos opptil 40 % av pasienter. De lokaliseres typisk ved benete fremspring (over PIP-ledd) og ved endearterier (fingerpulpa), men kan også sees proksimalt og distalt på underekstremitetene langt fra benete fremspring. Hyppigst på andre og tredje finger. Opp mot 11 % av slike ulcera ender med gangren eller amputasjon, og risikoen er størst for sår som varer lengre enn 6 måneder. Større iskemiske nekroser er uvanlig.
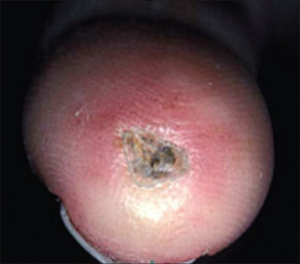
-Skorper og fissurer skyldes dermal fibrose på områder der huden er tynn og atrofisk. Små overfladiske ulcerasjoner (1-4 mm.) er oftest forårsaket av okklusjon av prekapillære arterioler. Dype sår på distale fingre og tær kommer som resultat av okklusjon av større kar eller sykdomsprosesser i kutane ekstremitetskar. Skarpt avgrensede iskemiske sår, ev. med tap av fingre eller tær, er også forårsaket av kar-okklusjon og ledsages gjerne av smerter (kritisk iskemi). Ved kritisk iskemi opptrer smerter, og proksimalt for det iskemiske området sees hyperemi.
-Pitting scars representerer vevstap og bør dermed ikke oppfattes som digitale ulcera. Lokaliseres til finger-pulpa og på lateralsiden av fingrene.
–Kalsinose ses hos ca. 25% av pasientene oftest ved begrenset form av systemisk sklerose. Vanlig lokalisering er på fingre, albuer og knær. Kalsinose ses også ved dermatomyositt og andre tilstander (Valenzuela A, 2018).
-Sår som ikke tilheler kan skyldes andre forhold enn grunnsykdommen. Det er viktig å utelukke kalsinose, ateromatose, infeksjon, diabetisk angiopati og koagulopati (inklusiv antifosfolipid syndrom). I sistnevnte gruppe bør man også utelukke Faktor V Leiden mangel som er den mest vanlige koagulopati. Biopsi vil her vise fibrinnedslag, men ingen inflammasjon. Venøse leggsår må også utelukkes. Disse gir spreng og tyngdefornemmelse i oppreist stilling, lokal kløe, parestesier og ikke sjelden nattlige kramper. Teleangiektasier, corona phlebectatica (vifte-formede teleangiektasier), brunlig hyperpigmentering og eksem er ikke uvanlig. Lipodermatosklerose kan utvikles etter noe tid (se også differensialdiagnoser nedenfor). Tegn til venøs insuffisiens med varicer sees ofte.
Sklerodaktyli. Med sklerodaktyli menes hard og noe tykk hud distalt for MCP-ledd i fingre. Begrenset form forutgås av Raynauds fenomen ofte med flere år. Mange med denne formen utvikler hud-forandringer begrenset til fingre og rundt munnen. Pre-skleroderma og tidlig systemisk sklerose er beskrevet ovenfor.
Pitting scars er substansdefekter på fingerpulpa. De oppstår spontant, ofte litt ut i sykdomsforløpet og er lokalisert ganske sentralt på fingertuppene. En må skille disse fra sår ved subkutan kalsinose som heller ikke er uvanlig ved sykdommen.
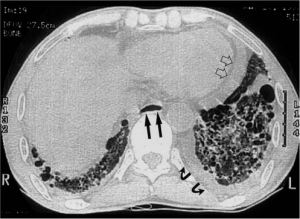
Lungemanifestasjoner merkes oftest relativt sent i forløpet. Tørrhoste eller belastningsdyspne er vanligste tegn. Forandringer kan påvises hos rundt 50% av pasientene og opptrer både som sykdom i lungevevet og vaskulær lungeskade (Hoffmann-Vold AM, 2019). Førstnevnte benevnes oftest interstitiell lunge-sykdom (ILD), selv om parenkymet representert ved alveolene ofte er angrepet.
Den raskeste utviklingen av ILD skjer ofte de første 4 årene etter diagnosen (Hoffmann-Vold A-M, 2019). Risikofaktorer inkluderer mannlig kjønn, afroamerikansk etnisitet, høy alder ved sykdomsdebut, kort sykdomsvarighet, anti-topoisomerase (a-ScL-70) -antistoffer, progredierende hudforandringer og diffus kutan sykdomsform (dc>SSc).
-Pulmonal hypertensjon (PAH). Vaskulær sykdom i lungearterier medfører pulmonal arteriell hypertensjon (PAH) hos 8-12% av pasientene (Aithala R, 2017). Symptomer kan være dyspne og utmattelse, men er ofte asymptomatisk (Morrisroe K, 2017) og trenger ikke være ledsaget av annen lungesykdom. PAH er årsaken til død hos mer enn halvparten av pasientene med systemisk sklerose (Kolstad KD, 2018) og tidlig terapi er viktig. PAH-screening er derfor sterkt anbefalt, også blant asymptomatiske pasienter (Gailie N, 2016). Tidlig behandling har best effekt på sikt. Med tidlig behandling menes at pasientene er i WHO funksjonsklasse I eller II av maksimalt IV mulige. Klasse II tilsier lett begrenset aktivitet. Ved regelmessig screening er 8-års overlevelse funnet å kunne økes fra 17% til 64% (Humbert M, 2011).
Nedsatt DLCO (gass diffusjonskapasitet) målt ved lungefunksjonstester kan predikere utvikling av både ILD og PAH. DLCO eller karbon monoksid transfer faktor måler gassutvekslingen i nivå med den alveolære membranen og tilkjennegir dysfunksjon i overføringen av CO. Dysfunksjonen kan skyldes redusert alveolær overflate eller nedsatt membranfunksjon. En FVC/DLCO ratio > 1,4 peker mer i retning av PAH enn av ILD. Vennligst les mer om PAH i eget kapittel
-Interstitiell lungesykdom (ILD) i form av fibroserende alveolitt er en interstitiell, retikulær type lungesykdom som preges av fibrose og som er lite tilgjengelig for behandling. Utprøvende antifibrotisk medikasjon med nintedanib (Ofev) kan redusere sykdomsprogresjonen mer enn placebo, men den kliniske nytten er usikker (Distler O, 2019). I enkelte tilfeller er lungetransplantasjon aktuelt (Shah RJ, 2017). Den inflammatoriske typen ILD kan derimot respondere på immunsuppresjon. Imidlertid vil det ofte foreligge en blanding av fibrose og inflammasjon. Å avgjøre hvilke av de to prosessene som dominerer hos den enkelte pasient kan være avgjørende for valg av behandling.
Histologisk er NSIP (non-specific interstitial pneumonia). NSIP er homogene forandringer som kan affisere alle lungepartier og er den hyppigste typen ILD ved SSc, fulgt av UIP (usual interstitial pneumonia). Ved UIP er deler av lungene affisert og det foreligger ofte honeycombing (radiologisk ses et bikakemønster). Vennligst les om NSIP og UIP i eget kapittel om lungemanifestasjoner ved revmatisk sykdom.
Nyresykdom med nyrekrise (scleroderma renal crisis, SRC)
Nyrekrise (“Scleroderma renal crisis”, SRC) sees nesten bare ved diffus type SSc (10-25%) og da oftest hos pasienter med anti-RNA polymerase III antistoffer (33% av dem med dette antistoffet). Symptomene omfatter ny hodepine, utmattelse, svimmelhet, neseblødninger og andre symptomer som følger av hypertoni. Omtrent 75% debuterer i løpet av de første fire sykdomsårene (median 8 måneder), men er også beskrevet (sjelden) etter 20 års sykdom. Som regel foreligger ingen forutgående hypertensjon. SRC karakteriseres av akutt stigning av blodtrykket (> 160/90), retinopati > grad Ill og raskt avtagende nyrefunksjon. SRC kan ledsages av hemoragisk alveolær kapillaritt (lungeblødning). Når både lunger og nyrer er angrepet foreligger et “pulmonalt-renalt syndrom” (Prabhakar N, 2023).
-Patogenese ved renal krise. lnitialt foreligger en endotelskade som gir fortykkelse og proliferasjon av intralobulære og arcuate kar (grener av interlobararteriene). Dette resulterer i trombocyttaggregasjon, økt kollagen- og fibrindeponering og ytterligere stenose eller okklusjon av karlumen. Resultatet er nedsatt nyreperfusjon og derav økning av renin og endothelin-1. Plasmarenin er forhøyet 10-100 x øvre normalverdi.
-Risikofaktorer. Anti-RNA polymerase III antistoffer (oftest ved dcSSc) er en disponerende faktor. Økt risiko ses også ved bruk av prednisolon (spesielt ved > 10-15 mg/d). I tillegg kan renal krise utløses av hjertesvikt (nedsatt nyreperfusjon), perikardvæske, arytmier, sepsis og dehydrering. Bruk av ciclosporin kan utløse raskt innsettende nyresvikt som minner om SRC.
-Klinisk viser nyrekrise seg i form av sterk hodepine, synsforstyrrelse eller encefalopatisymptomer som kramper, fatigue, kvalme, og konfusjon. Over 90 % har hypertensjon, 30 % har diastolisk trykk > 120 mmHg. Imidlertid forekommer også atypiske forløp: Av pasienter med SRC er omkring 10 % normotensive. Disse kan allikevel ha trykkstigning, men innenfor normalverdier.
-Laboratorieprøver viser ofte redusert Hb med mikrocytær, normokrom hemolytisk anemi. Schistocytter kan påvises i blodutstryk. Retikulocytose og trombocytopeni (< 50 000) ses hos omkring halvparten av pasientene. Andre blodprøveutslag kan være stigende LD, troponin, NTpro-BNP og haptoglobin og C3/C4 kan falle. Proteinuri forekommer, men er oftest < 2g/24t. I urinen kan også mikroskopisk hematuri og kornede sylindre ses. Serumkreatinin stiger daglig, selv etter at BT er normalisert.
-Nyrebiopsi. Biopsi tas når BT og koagulasjonsstatus er normalisert (Penn H, Howie AJ, 2007; Chrasaszcz M, 2020). Systolisk blodtrykk >160 mmHg kan være kontraindikasjon for biopsi. Histologisk ses infiltrasjon av glatt muskelceller og deponier av kollagen i intima som medfører konsentrisk fibrose (“løk-skall utseende”).
-Behandling av hypertensiv nyrekrise så snart som mulig er svært viktig for prognosen. Etter at ACE-hemmere ble tilgjengelige har ett års mortalitet falt fra 85% til 24% (Zanatta E, 2018). Likevel vil en del av pasientene få behov for nyretransplantasjon på sikt (Prabhakar N, 2023). Vennligst se mer om behandling i avsnitt senere i dette kapitlet.
–Myokardfibrose. Systemisk sklerose kan føre til fibrose i hjertet og forekomsten er høyere enn tidligere antatt. Studier har vist tegn til myokardfibrose hos så mange som 45% av pasientene med SSc (Rodriguez-Reyna TS, 2015, Ramalho AR, 2017, Ntusi NA, 2014). SSc øker dermed risikoen for alvorlige kardiale komplikasjoner, spesielt hjertesvikt og arytmier. Disse arytmiene kan manifestere seg tidlig i sykdomsforløpet. Årsaken er at fibrosen i myokardiet kan påvirke det elektriske ledningssystemet. Risikofaktorer for arytmier hos SSc-pasienter omfatter mannlig kjønn, høy alder ved sykdomsdebut og tilstedeværelse av pulmonal hypertensjon (PAH) (Bairkdar M, 2024).
Diagnostiske undersøkelser er avgjørende for tidlig deteksjon og inkluderer EKG og 24t-EKG for å vurdere hjerterytme. Ekkokardiografi er viktig for å evaluere hjertefunksjon og -struktur. Ved ultralyd Doppler av hjertet kan en se diastolisk dysfunksjon (Smiseth OA, 2019). Myokardfibrose kan også påvises ved MR-undersøkelse av hjertet som gir detaljert informasjon om myokardfibrose og ventrikkelfunksjon (Bissel L-A, 2017), men undersøkelsen er ikke alltid rutine. NT-pro-BNP og troponin-I er biomarkører som kan indikere henholdsvis hjertebelastning og myokardskade. Diagnosen kan sikres ved myokardbiopsi (Nadel A, 2024).
| Forekomst av plutselig hjertedød, rytmeforstyrrelser og behov for ICD ved systemisk sklerose (SSc) (Fairley JI, 2024; Riemekasten G, DgRh, 2024) | |||
| SSc med hjertemanifestasjon | Uselekterte SSc-pasienter | SSc uten hjertemanifestasjon | |
| Plutselig hjertedød | 3,3% årlig | 1% årlig | 2,9% årlig |
| For tidlige ventrikulære komplekser (>1000/24t) | 70% | 16,3% | 6% |
| EKG (uten belastning) | 58% unormale | 47% unormale | 30% unormale |
| Pacemaker, ICD | 3,5-27% | 0,7-5,1% | 0% |
-Pulmonal hypertensjon. Årlig ekkokardiografi anbefales for å oppdage tidlige tegn på pulmonal hypertensjon. Kardiolog bør oppgi mål på høyre atrium areal (cm2) og hastigheten på trikuspidalklaff-tilbakestrøm (TR hastighet i m/s) som inngår i DETECT–kalkulatoren. Ved mistanke om pulmonal hypertensjon kan DETECT-kalkulatoren brukes for å estimere behov for høyre-kateter-hjerteundersøkelse. Kalkulatoren benytter data fra EKG, ekkokardiografi, hjertefrekvens, blodtrykk, NT-proBNP og urat-nivå (Young A, 2021). Vennligst se også kapittel om Pulmonal hypertensjon.
Andre kardiale manifestasjoner inkluderer myokarditt, hjertesvikt, perikardvæske, cor pulmonale og patologisk ventrikulær relaksasjon/diastolisk dysfunksjon. Hjertemanifestasjoner ulike revmatiske sykdommer er beskrevet i eget kapittel
Omtrent 90% av pasientene med SSc har en form for gastrointestinal manifestasjon (McMahan ZH, 2019).
-Gastro-øsofageal refluks og øsofagus-dysmotilitet av distale 2/3 med tilhørende svelgeproblemer, samt dyspepsi og refluks er vanligst (> 80 %). Hovedsymptomet ved gastro-øsofageal refluks med sviende ubehag fra epigastriet opp mot sternum oftest få timer etter måltid. Ved dysmotilitet kan også pasientene ha følelse av en klump i halsen og smerter ved svelging. Diagnosen kan sikres med røntgenkontrast, manometri eller scintigrafi. Ved alvorlig refluks kan Barretts øsofagus utvikles (dysplastiske slimhinneforandringer), hvorav 10 % overgår i adenokarsinom. Ved mistanke er gastroskopi indisert.
–Dysfagi kan ha ulike årsaker. Pasienten føler ofte av at maten samler seg i munn og spiserør. Noen plages med hoste etter svelging og ubehag med stemmen.
-Gastroparese kan medføre forsinket tømming. Symptomene kan være metthetsfølelse, kvalme og vekttap.
-Malabsorpsjon kan føre til mangel på vitamin B12, vitamin D, kalsium, jern og kalorier.
-Kolon-sakkulasjoner er innsnevringer som kan gi obstipasjon.
-Nedsatt motilitet i hele tarmsystemet kan gi pseudoobstruksjon og disponere for bakteriell overvekst.
-Watermelon stomach (GAVE — gastric antrum vascular ectasia) kan gi akutt blødningsanemi og skyldes telangiektasi-lignende forandringer i gastrointestinalkanalen. Gastroskopi gjøres for diagnostisering og i behandlingen brukes argon laser for koagulering (Ghrenassia E, 2014).
– “Stagnant loop syndrome” og pneumatosis cystoides intestinalis med luftbobler i tarmveggen er sjeldne manifestasjoner (Koysombat K, 2018).
-Anorektal dysfunksjon forekommer hos 50-70 % og ytrer seg ved obstipasjon, prolaps og anal sfinkter-dysfunksjon med fekal inkontinens (Garros A, 2017).
-Bakteriell overvekst diagnostiseres ved Glukose-pusteprøve. Pasienten drikker glukose, og man måler sa hydrogen (H) i utåndingsluften (kun bakterier kan produsere H).
Muskel og skjelett
-Akroosteolyse (“Tuft resorption”) er en karakteristisk, men mindre vanlig skjelettmanifestasjon ved SSc. Det foreligger benresorpsjon av det distale falangeale benet, oftest i fingre og sjeldnere i tær. Akroosteolyse forekommer oftest ved den diffuse kutane formen av SSc. Symptomene inkluderer ofte smerte i fingertuppene og man kan etter hvert se en forkortning av fingrene (telescoping). Årsaken er redusert perifer blodtilførsel. Akroosteolyse ses derfor ofte i kombinasjon med digitale ulcera. Diagnosen stilles radiologisk ved påvisning av tap av benmasse i den distale falangen. En kan se “pencil-in-cup”-lignende forandringer eller en diffus resorpsjon av benvevet. Akroosteolyse er et tegn på alvorlig perifer vaskulær involvering og indikerer ofte en mer avansert og alvorlig sykdom (Sandler RD, 2020).
-Artralgier er et vanlig og uspesifikt symptom ved SSc som kan ramme mange (38-97%). Årsaken kan være fibroseutvikling omkring ledd og leddnære strukturer. I praksis kan det være vanskelig å differensiere artralgi fra symptomer som stammer fra hud, underhud, sener eller skjelett. Ekte synovitt og artritt er mindre vanlig (Sandler RD, 2020).
-Artritt kan forekomme ved systemisk sklerose (SSc), selv om det er mindre fremtredende enn de kutane og vaskulære manifestasjonene. Artritt ved SSc kan i enkelte tilfeller være erosiv, noe som indikerer en mer aggressiv leddpåvirkning. Dette skiller seg fra de vanligere artralgiene. Ved mistanke om artritt bør en grundig klinisk og radiologisk evaluering utføres for å vurdere grad av inflammasjon og eventuell erosiv sykdom.
-Myopati med lavgradig myositt ses hos 14 %. Menn med diffus type er mest utsatt. Myositten kan komme både sent og tidlig i forløpet. Noen kan klassifiseres som scleroderma-polymyositt overlapp syndrom (skleromyositt). Man forventer patologisk kapillaroskopi med karforandringer i neglesengene. Noen utvikler akroosteolyse (Lefebreve F, 2021).
-Tendon friction rub er senekrepitasjoner ved bevegelse i seneskjeden. Manifestasjonen ses hovedsakelig ved diffus form (dcSSc) og da tidlig in forløpet. Tendon friction run kan indikere et komplisert sykdomsforløp (Barbachi A, 2023).
Andre manifestasjoner
SSc kan ha en rekke andre systemiske manifestasjoner utover de klassiske kutane, vaskulære og viscerale involveringene. Disse inkluderer:
- Sekundært Sjøgrens syndrom, karakterisert av tørre slimhinner grunnet autoimmun eksokrinopati
- Primær biliær kolangitt (PBC), en kronisk autoimmun leversykdom.
- Hematologiske komplikasjoner som autoimmun hemolytisk anemi er mindre vanlig.
- Nevrologisk kan trigeminusnevralgi oppstå (Maikap D, 2022). Cerebral MR kan vise “white matter hyperintense foci” som skyldes mikrovaskulære forandringer eller iskemiske lesjoner i hjernen (Gamal RM, 2021).
Undersøkelser
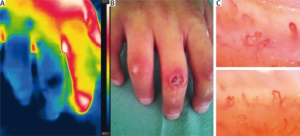
En bør få mistanke om begynnende systemisk sklerose ved nyoppstått Raynauds fenomen, spesielt i kombinasjon med påvisning av spesifikke antistoffer som CENP (centromerantistoff) eller anti-Scl70 (topoisomerase I-antistoff) i signifikante titere. Klart patologisk kapillaroskopi-funn gjør diagnosen enda mer sannsynlig (se nedenfor). Grundige supplerende undersøkelser og en vurdering av helhetsbildet sikrer diagnosen og kan ofte si noe om prognosen. Dette er igjen bakgrunnen for et individuelt tilpasset behandlings- og oppfølgingsprogram (Volkmann ER, 2023).
Anamnesen kartlegger aktuelle symptomer. Dette er ganske omfattende (se nedenfor). Men en kan ta utgangspunkt i klassifikasjonskriteriene og etterspør Raynauds fenomen med ev. tid for debut, hovne fingre, sår på fingerpulpa, stramhet i huden på hender, ansikt og ellers på kroppen. Svelgevansker, magesyre-oppstøt/refluks, fordøyelsesbesvær, vekttap, tegn til dyspne eller tegn til perifere ødemer. Tørrhetsplager fra øye eller munn (sekundært Sjøgrens syndrom).
Klinisk kan en gjøre en generell status som kan omfatter måling av blodtrykk, puls og vekt. Auskultasjon av hjerte og lunger, palpasjon av abdomen. Huden på hender inspiserer og palperes for hovenhet/puffy, sklerodaktyli, sår eller substansdefekter på fingerpulpa, kalsinose og teleangiektasier. Kontrakturer beskrives. Ekstremiteter kan undersøkes for hud-manifestasjoner og bevegelighet.
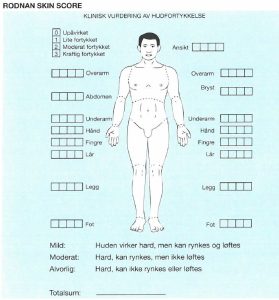
-Modifisert Rodnan Skin Score/hudskår (mRSS) har vist seg å kunne korrelere med alvorlighetsgraden av hudmanifestasjoner. Metoden er blitt en gullstandard i evaluering av hudtykkelse og utbredelsen ved systemisk sklerose. Metoden er lett å lære, men en bør følge en prosedyre. Huden løftes forsiktig mellom undersøkerens tommel og pekefinger som beskrevet av Khanna (Khanna D, 2017).
Kapillaroskopi / kapillærmikroskopi / neglefold-video-kapillaroskopi. Et viktig hjelpemiddel i diagnostikken er kapillær-mikroskopi av neglesengene. Undersøkelsen trenger ikke ta lang tid og kan integreres i en klinisk konsultasjon. Typisk vil undersøkelsen vise dilaterte kapillærer, nedsatt tetthet av kapillærer, slyngede kapillære loops, avaskulære områder og «Bushy» fenomener (neo-angiogenese). Under kapillaroskopi kan det oppstå forbigående vasospasme i enkelte kapillærer som kan forveksles med manglende kapillærer (“ghost capillaries”). Tidlige forandringer: Mega-kapillærer med lekkasje av erytrocytter. Aktivt stadium: Spontan-hemoragier. Sent stadium: Kapillærtap, busk-kapillærer, få makro-hemoragier. Vennligst les mer om kapillaroskopi i eget kapittel
6-minutter gangtest. Undersøkelsen bestemmer avstanden som tilbakelegges i løpet av 6 minutters gangtid ved maksimal, jevn, rask gange på flatt underlag (f. eks. en sykehuskorridor). Testen kan være en indikator på fysisk form og hjerte og lungefunksjon. Spesielt har den vist seg nyttig til å evaluere individuelt forløp over tid og effekt av behandling. Testen forutsetter imidlertid godt samarbeid, og at pasienten har normal eller stabil gangfunksjon (Enright PL, 2003).
Blodprøver. Rutineprøver kan omfatte CRP, SR, Hb, leukocytter med differensialtelling, trombocytter, elektrolytter, urat/urinsyre, lever-, nyre- og thyreoidea-funksjonsprøver. Glukose, kreatin kinase (CK), immunologiske prøver (se nedenfor) og urin stiks. Ved mulighet for pulmonal hypertensjon suppleres ofte med NT-pro-BNP.
–Ofte foreligger normale inflammasjonsparametere. Forhøyet SR og CRP kan indikere komplikasjoner som infeksjon, men også myositt (med høy CK). Vedvarende forhøyet CRP korrelerer med IL-6 nivå som er funnet å være en ugunstig prognostisk parameter for lungefibrose, pulmonal hypertensjon og mortalitet (Mitev A, 2019).
Immunologiske undersøkelser. Ikke alle pasienter med systemisk sklerose har påviselige autoantistoffer. Fravær av typiske antistoffer utelukker derfor ikke diagnosen, men krever en nærmere differensialdiagnostisk vurdering. Utenom de klassiske antistoffene har forskning vist en lang rekke andre antistoffer ved sykdommen (Murunganadam M, 2023).
- Antinukleære antistoff (ANA) er positive hos mer enn 90 % av pasientene med systemisk sklerose og fungerer ofte som en initial screeningtest. Et positivt ANA-resultat krever videre differensiering med spesifikke systemisk sklerose-assosierte antistoffer for å bekrefte diagnosen og klassifisere subtype.
- Subgruppene Anti-Scl 70 (Anti-topoisomerase I) antistoffer påvises hos 20-30 % av pasientene med SSc og er sterkt assosiert med diffus kutan systemisk sklerose (dcSSc) og økt risiko for lungefibrose. Tilstedeværelsen av disse antistoffet indikerer derfor en mer alvorlig sykdomsprognose (Steen V, 2003).
- Anti-centromer antistoff/CENP ses hos 25-50 % med SSc og er typisk for begrenset type (CREST).
- Anti-RNA polymerase III forekommer hos en undergruppe av pasienter, særlig ved dcSSc, og øker risikoen for raskt progredierende hudsykdom og en betydelig risiko for systemisk sklerose renal krise (SRC). Tidlig identifisering er viktig for aktiv monitorering og behandling av denne alvorlige komplikasjonen.
- Mer sjeldne auto-antistoffer som anti-Th/To, anti-U3RNP, U1RNP og anti-Ku har lav sensitivitet (< 10 %) (SSc-assosierte antistoff), men kan bidra til diagnosen i spesifikke tilfeller. Disse antistoffene kan være assosiert med distinkte kliniske fenotyper og prognoser, men krever mer forskning for fullstendig forståelse.
- Primær biliær kolangitt (PBC) assosierte autoantistoffer. Opp mot 20% av pasientene med systemisk sklerose kan ha primær biliær kolangitt (PBC) assosierte autoantistoffer, som anti-mitokondrieantistoff (AMA) og AMA-M2. Dette indikerer en overlapping mellom de to autoimmune sykdommene og tilsier at man bør være oppmerksom på eventuell underliggende leversykdom hos disse pasientene. Alternativt kan de foreligge to separate autoimmune sykdommer (SSc og PBC).
Oversikt over antistoff, deres prevalens og kliniske betydning ved systemisk sklerose (SSc) (modifisert etter Fritzler MJ, 2023).
| Antigen | Prevalens | Klinisk betydning | |
|---|---|---|---|
| SSc-spesifikke antistoff Inkludert i ACR/EULAR klassifikasjonskriterier |
Topoisomerase I (Scl-70) | 20–30% | DNA topoisomerase I. Viktig markør for dcSSc og assosieres med økt risiko for alvorlig lunge- og nyreaffeksjon. |
| Centromer (CENP) | 25–50% | CENP-A, CENP-B. assosiert med begrenset form/CREST-syndrom og en lavere risiko for alvorlig intern organaffeksjon enn dcSSc. | |
| RNA Polymerase III (RNAP3) | 10–20% | Nukleært mønster er usikkert for å påvise RNA polyisomerase-3, flekket mønster dominerer. sterkt assosiert med dcSSc og indikerer en høyere risiko for sklerodermi renal krise og raskt progredierende hudfortykkelse. | |
| SSc-Spesifikke antistoff | Fibrillarin | 3–20% | U3 RNP (ribonucleoprotein). Assosieres med en mer alvorlig dcSSc med lungefibrose, pulmonal hypertensjon, myositt, hjerte- og nyrekomplikasjoner, samt en mulig kobling til malignitet. |
| Th/To | 3–10% | Rpp25, Rpp38. Ses ofte ved begrenset kutan form/CREST og gir en høyere risiko for pulmonal hypertensjon og gastrointestinal involvering. | |
| RuvBL1/2 | 1–3% | Double hexamer av RuvBL1 og RuvBL2 proteiner. Høyere risiko for pulmonal arteriell hypertensjon. | |
| SSc-assosierte antistoff (ses ofte også ved andre tilstander) | U1 RNP | 5–15% | U1-RNP 70 kDa, U1 RNP-A og U1 RNP-C. Primære serologiske markøren for Mixed Connective Tissue Disease (MCTD), men kan også kan finnes hos pasienter med systemisk lupus erythematosus (SLE) og SSc. |
| Ku | 3–10% | 80- og 70-kDa bindende dimerisk protein. Ses ved SSc, polymyositt/dermatomyositt , SLE og overlappssyndromer og indikerer ofte en kompleks klinisk presentasjon. | |
| PM/Scl | 5–10% | PM/Scl-100 protein fra human exosom. Markør for overlappssyndromer mellom polymyositt/dermatomyositt og SSc og assosieres ofte med fibrotisk interstitiell lungesykdom. | |
| Ro52 (SSA) | 15–25% | Ro52/tripartite motif (TRIM) 21. assosiert med flere autoimmune sykdommer: Sjøgrens syndrom, SLE, inflammatoriske myopatier og kan indikere en økt risiko for alvorlig organsykdom og neonatal lupus. | |
| Antistoff som kan være assosiert med SSc | U11/U12 RNP | 3–5% | U11/U12 RNP kompleks av spliceosom. RNPC-3 is the 65 kDa hovedmål. Indikerer en høyere risiko for alvorlig interstitiell lungesykdom (ILD) og gastrointestinal dysmotilitet, samt en mulig assosiasjon med malignitet. |
| TERF-1 | 3–5% | Shelterin protein. Assosieres med en subgruppe av pasienter med SSc, ofte med affeksjon av lungefibrose. | |
| eIF2B | 1–3% | Eukaryotic initiation factor 2B. Sterkt assosiert med dcSSc og interstitiell lungesykdom (ILD). Ofte funnet hos pasienter som er negative for andre kjente systemisk sklerose-spesifikke autoantistoffer (ANA-negative). | |
| NOR 90 | <5% | human upstream binding factor (hUBF). Ofte i den begrensede kutane formen/CREST. Kan indikere en mer gunstig prognose med mildere organinvolvering. | |
| B23 | <5% | Nucleophosphmin. Rapportert i enkelte tilfeller av SSc og andre autoimmune tilstander. Uklar klinisk signifikans. |
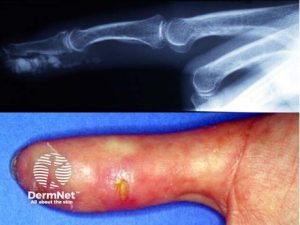
Lungefunksjonstester gjøres for å kartlegge om lungene er affisert og i oppfølging for eksempel 1-2 ganger årlig for å avdekke ev. progresjon.
Alvorlighetsgrad estimert ved lungefunksjonstester:
- Intermediær: FVC > 70 = mild sykdom.
- Alvorlig: FVC < 70 = utbredt sykdom.
Lungefunksjonstester er beskrevet i et eget kapittel.
Bildediagnostikk er viktige metoder for diagnostisk og i oppfølgingen av SSc (Rutka K, 2021):
-CT (ev High Resolution /høyoppløsnings CT, HRCT) viser mest detaljert lungevevet og luftveiene (se også avsnittet Organmanifestasjoner nedenfor i dette kapitlet). Metoden (HRCT) gir også stråledose enn vanlig CT.
–Et infiltrat (“consolidation”) kan defineres som utvisking av karstrukturer og luftveisvegger. Årsaken er at alveole-luften erstattes av væske og celler ved ILD.
–Ved mattglass-fortetning (“ground glass opacities”) fremstår det affiserte lungevevet som tåket eller uskarpt, mens de underliggende bronkiale og vaskulære strukturene fortsatt er synlige. Mattglass-forandringer skyldes fortetninger intraalveolært og interstitielt. Arkitekturen er bevart. På et HRCT bilde skal man kunne skimte karstrukturene gjennom slike matte fortetninger. Dessverre er bare 20 % av slike forandringer reversible (resten er mikrofibrose). Imidlertid er ikke mattglass-forandringer alltid ensbetydende med pågående inflammasjon. Stadium-inndeling av CT forandringer (a.m. Athol Wells, Brompton Hospital):Utbredelse i lungevev omfatter < 20% mild sykdom. Utbredelse i lungevev > 20 % utbredt sykdom.
–Bikake-forandringer (honeycombing) representerer endestadiet av en rekke lungesykdommer. Forandringene skyldes at intraalveolære septa er fortykket, ødelagt eller fortrengt.
–PAH. CT kan også gi mistanke om pulmonal (arteriell) hypertensjon (PAH) ved at diameter av pulmonalarterien er tydelig utvidet og videre enn aortas diameter.
-Røntgen av øsofagus kan gjøres dynamisk med kontrastmiddel som pasienten svelger. En forventer redusert funksjon i distale 2/3 del av øsofagus på grunn av dysmotilitet ved SSc. I blant påvises også (stenoser som kan blokkes) eller funksjonssvikt av musculus cricophayngeus i form av krikofaryngeal dysfunksjon som i noen tilfeller opereres (ØNH).
-Røntgen av hender gjøres for å vurdere om erosiv artritt, kalsinose eller akroosteolyse foreligger. Ved kliniske mistanke og behov undersøkes også andre kroppsdeler.
Bronko-alveolær lavage (BAL). Metoden brukes ofte får å utelukke eller påvise infeksjon, men kan også v ære annen diagnostisk verdi ved SSc: Dersom en i bronko-alveolær lavagevæske påviser neutrofile som overstiger 2.7 x 100 000/ml eller eosinofile over 2.3 % taler det for inflammasjon. Noen har funnet at eosinofil alveolitt har en dårligere prognose enn neutrofil alveolitt. Den diagnostiske verdi av BAL er imidlertid omstridt. Vennligst les mer om BAL i kapittel om bronkoskopi.
EKG. Undersøkelsen kan avdekke tegn til kardial svikt eller pulmonal hypertensjon, arytmi eller iskemi.
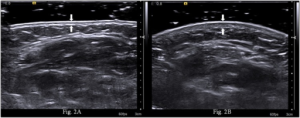
Ekkokardiografi/ultralyd Doppler gjøres ofte årlig over en lang periode ved SSc. Hovedindikasjonen er å utelukke tegn til pulmonal arteriall hypertensjon (PAH). Tilstanden er overrepresentert både ved systemisk begrenset og diffus form for systemisk sklerose og behandlingsmulighetene klart bedre når en begynner behandlingen tidlig. Ved ekkokardiografi kan man også påvise tegn til myokardfibrose (Nadel A, 2024).
Ultralyd av huden kan benyttes for å estimere hudaffeksjonen. Metoden har vist seg å korrelere med hudtykkelse, stivhet og Rodnan skin score (mRSS) (Liu H, 2017), men er ikke mye brukt i klinisk hverdag.
Hjertekateterundersøkelse gjøres hvis ekkokardiografi tyder på pulmonal hypertensjon (PAH). PAH diagnostiseres hvis høyresidig hjertekateter-måling viser mPAP ≥ 20mmHg i ro og motstanden i pulmonalarterien (PAR) er ≥ 3 Woods. Forutsetning er eksklusjoner: PCWP ≤15 mmHg (utelukker venstresidig hjertesvikt). Dessuten skal følgende utelukkes: kronisk lungesykdom med hypoksemi, venøse tromber (tromboembolier) eller (sjelden) obstruktiv lungearterie-sykdom (tumorer, stenoser, parasitter), kronisk nyresvikt, sarkoidose, noen blodsykdommer og metabolske sykdommer som påvirker lungene. Undersøkelsen og tolkning av resultater er beskrevet i kapitlet om pulmonal hypertensjon.
Andre undersøkelser:
- Fibrillin-1. Enkelte (ikke rutine) undersøker også økt fibrillin-1 som en biomarkør og et aktivitetstegn på alveolitt ved SSc.
- 18FDG PET/CT scan kan brukes for å skille mellom inflammasjon og fibrose. Denne benytter seg av en isotop som ikke tas opp av fibroblaster. Positivt opptak tyder på inflammasjon i lungevev (tilstedeværelse av celler som metaboliserer glykose). Undersøkelsen er imidlertid ikke rutine.
- Transbronkial biopsi via bronkoskopi kan vurderes ved progredierende lungesykdom av uklar årsak.
- Termografi kan vise nedsatt temperatur på fingre Raynauds fenomen, men metoden er lite brukt i praksis.
Ulike typer systemisk skleroser
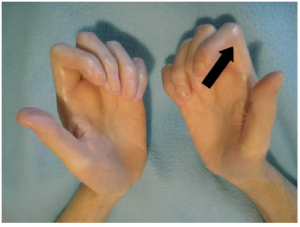
Begrenset Kutan Systemisk Sklerose. Hudaffeksjon distalt for albuer og knær er typisk. Ansiktet angripes ofte, men oftest begrenset til området omkring munnen. I forløpet ses hyppig ILD (Interstitiell lungesykdom) og en risiko for PAH (pulmonal hypertensjon). Nyreaffeksjon sjelden. Mangeårig Raynauds fenomen før utvikling av så på fingerpulpa er vanlig. Sår kan også oppstå som følge av subkutan kalkinnlagring, ofte på fingre. Vanligst antistoff er CENP (anti-centromer antistoff). CREST (Calcinosis/kalsinose, Raynauds, Esophagus/øsofagus-dysmotilitet, Sklerodaktyli og Teleangiektasier) er en ganske vanlig form for begrenset SSc.
Diffus kutan systemisk sklerose (dcSSc). Hudaffeksjon på ekstremiteter, truncus og ansikt, samt hyppige organmanifestasjoner. Vanligste antistoff er Scl-70 (topoisomerase-I). Risiko for hypertensiv renal krise og GAVE (gastric antrum vascular ectasia), særlig de første to årene fra sykdomsdebut.
Juvenil systemisk sklerose er omtalt i et eget kapittel.
Pre-skleroderma og tidlig systemisk sklerose. “Udifferensiert systemisk bindevevssykdom med risiko for systemisk sklerose (UCTD-risk-SSc)/veldig tidlig systemisk sklerose” kan defineres ved Raynauds fenomen og enten autoantistoff forenelig med systemisk sklerose eller kapillaroskopi med sklerodermi-mønster uten at kriterier for SSc er oppfylt. Aktuelle antistoff omfatter anti-ScL 70, anti-CENP, anti-RNA-polymerase III, anti-fibrillarin, anti-Th/To eller anti PM-Scl 70/100. Fordi 2013-ACR/EULAR kriterier for SSc ikke skal oppfylles, skal den udifferensierte tilstanden ikke ha puffy/hovne fingre, sklerodaktyli, teleangiektasier, interstitiell lungesykdom eller pulmonal hypertensjon. Risikoen for å utvikle typisk systemisk sklerose i denne gruppen er estimert til 54% (Valentini G, 2020). Ved kombinasjonen av “puffy hands” og anti-Scl 70 eller anti-CENP antistoff er risikoen for utvikling av SSc særlig høy.
«Very early SSc»
Tidlige symptomer på systemisk sklerose som inngår i kriterier for tidlig SSc Avouac J, Fransen J, ARD 2010:
- Raynauds fenomen
- «Puffy» / hovne fingre
- Typiske antistoff (Scl 70, CENP)
- Kapillaroskopi viser mikrovaskulær patologi
Ikke alle med «very early SSc» utvikler typisk SSc. En studie av 66 pasienter viste utvikling til SSc hos 32% etter 31 måneders oppfølging. Kapillaroskopisk megakapillærer var en risikofaktor (Vasile M, 2018;. Cutolo M, 2010).
Systemisk sklerose sine skleroderma. Typisk systemisk sklerose, men uten manifestasjoner i huden. SSc-hudaffeksjon tilkommer hos 60% i løpet av 0,5-7 år. Pasientene har ofte kliniske trekk som ved CREST syndrom. Disse pasientene kan utvikle pulmonal arteriell hypertensjon og asymptomatisk perikardsykdom, lunge, nyre, mage-tarm og ledd/muskel-manifestasjoner (LeRoy EC, 2001; Lescoat A, 2023; Angelis R, 2023).
| Forskjeller mellom begrenset kutan systemisk sklerose og diffus kutan systemisk sklerose (Tilpasset etter Hinchliff M, 2008) | ||
| Kjennetegn | Begrenset form | Diffus form |
| Fibrose i huden | Fra distalt og opp til albuer og knær, kan affisere ansikt (rundt munnen) | Områder også proksimalt for albuer og knær. Kan affisere truncus, hals og ansikt |
| Typiske lunge-manifestasjoner | Pulmonal arteriell hypertensjon (PAH) | Interstitiell lungesykdom (ILD) |
| Karakteristiske indre organ-manifestasjoner | Alvorlig gastro-øsofageal refluks og Raynauds fenomen | Skleroderma renal krise |
| Kliniske funn | Teleangiektasier, kutan kalsinose, sklerodaktyli, digitale iskemiske komplikasjoner (sår, nekroser) | “Tendon friction rub” (sene-krepitasjoner), pigmentforandringer |
Skleromyositt. Skleroderma-myositt overlapp. Dette er en egen sykdomsenhet. Hovedsymptomer er Raynauds, sklerodermi-forandringer i hud i ansikt og på hender, artralgi eller arteritt, myositt og interstitiell lungesykdom (nær 100%). Andre organer angripes sjelden og forløpet er med godartet enn systemisk sklerose diffus form. Påvisning av anti-PM Scl 75 eller 100 er typisk. Myokarditt, ofte asymptomatisk er ikke helt sjelden (18%) (Lilleeker JB, 2017). Behandlingen kan ved behandlingskrevende myositt bestå i lave doser prednisolon, høyere doser unngås på grunn av risiko for renal krise. Litteratur: Bhansing KJ, 2014; Pope JE, 2002.
Barnetts klassifikasjon (Alfred J. Barnett i 1978): Noen foretrekker fremdeles denne klassifikasjonen av SSc: Type I: affeksjon av utelukkende fingre. Type II: affeksjonen rammer også underarmer. Type III: diffus affeksjon.
Diagnosen systemisk sklerose (systemisk begrenset- eller diffus form) stilles på bakgrunn av typisk anamnese, sykdomsbilde med Raynauds fenomen, sklerodaktyli, eventuelt også kalsinose teleangiektasier og auto-antistoffer. Typiske forandringer ved kapillaroskopi forventes også. Hudbiopsi er sjelden nødvendig. ANA forventes å slå ut i blodprøver (90%), og CENP eller a-Scl70 er typiske subklasser.
Klassifikasjonskriterier
ACR/EULAR-kriteriene av 2013 for klassifikasjon krever enten proksimal skleroderma eller to av følgende: sklerodaktyli, digital iskemi eller pulmonal fibrose (se tabellen nedenfor)
| Klassifikasjonskriterier. 2013 (van den Hoogen F). Sum-score på minst 9 for diagnose: | Score (vekting): |
| Sklerodaktyli på fingre og proksimalt for MCP bilateralt | 9 |
| Puffy fingre | 2 eller |
| Sklerodaktyli av minst en hel finger distalt for MCP | 4 (velg høyeste skår) |
| Ulcera på fingerpulpa | 2 eller |
| Pitting scars/arr/skorper på fingertupp | 3 (velg høyeste skår) |
| Telangiektasi | 2 |
| Kapillaroskopi patologisk | 2 |
| Pulm hypertensjon eller/og interstitiell lungesykdom | 2 |
| Raynauds fenomen | 3 |
| Antistoff relatert til systemisk sklerose (CENP, ScL70, RNA Polymerase III) | 3 |
Differensialdiagnoser
- Acrodermatitis chronica atrophicans (kronisk borreliose): Sen manifestasjon av borrelioseinfeksjon med hudatrofi, ofte på ekstremitetene. Kan gi hudforandringer og Raynauds fenomen som ved SSc.
- Amyloidose: Avleiring av amyloidprotein i vev, kan affisere hud og indre organer. Kan gi fortykket hud og karpaltunnelsyndrom som ved SSc.
- Buschkes syndrom (sklerødema adultorum Buschke): Sjelden tilstand med fortykket hud, hovedsakelig på trunkus og proksimalt på ekstremitetene. Hudfortykkelsen kan ligne på SSc, men uten Raynauds fenomen eller indre organaffeksjon.
- Diabetisk hånd: Fortykket hud på hender hos pasienter med langvarig diabetes. Kan gi hudfortykkelse som ved SSc, men uten Raynauds fenomen.
- Eosinofil fasciitt: Inflammatorisk sykdom i fascia med eosinofili. Kan gi hudfortykkelse og kontrakturer, men hendene er vanligvis spart.
- Fasciitt-pannikulitt syndrom. Tidligere oppfattet som subgruppe av eosinofil fasciitt, Inflammatorisk sykdom i fascia og subkutant fettvev, ofte assosiert med malignitet. Kan ligne på hudforandringene ved SSc.
- GVHD Kronisk graft versus host disease: Immunologisk reaksjon etter transplantasjon, kan affisere hud og indre organer. Kan gi hudfortykkelse, Raynauds fenomen og indre organaffeksjon som ved SSc.
- Huriez syndrom (palmoplantar keratodermi med sklerodaktyli): Arvelig tilstand med fortykket hud på håndflater og fotsåler, samt sklerodaktyli. Sklerodaktyli kan ligne på SSc.
- Kjemisk indusert sykdom
-
- Acro-osteolyse kjennetegnes ved Raynauds fenomen og smertefull nedbrytning av benvev i fingertuppene med hevelse i de distale falangene, subkutan kalsifikasjon, evt. sakroiliitt og assosiasjon til vinylklorid eksposisjon. Likhet med SSc: Raynauds fenomen og kalsifikasjoner kan forekomme ved SSc.
- Eosinofili myalgi syndrom: Inntak av 1-tryptofan. Epidemi i Mexico i 1989. Ingen Raynauds. Systemisk sykdom med muskelsmerter og eosinofili, utløst av forurenset tryptofan. Likhet med SSc: Kan gi hudfortykkelse og muskelsmerter, men uten Raynauds fenomen.
- Erasmus syndrom. SSc etter eksposisjon for silika (brukes i betong-produksjon). Likhet med SSc: Har samme symptomer som SSc.
- Kjemisk / medikament / rusmiddel -induksjon ved vinylklorid, bleomycin, pentacozin, Vitamin B12, Vitamin K, kokain, penicillamin, methyrsergid: Ulike stoffer kan utløse SSc-lignende symptomer. Likhet med SSc: Kan gi hudfortykkelse, Raynauds fenomen og lungefibrose som ved SSc.
- Nefrogen fibroserende syndrom: Systemisk fibrose utløst av gadoliniumholdig kontrastvæske hos pasienter med nyresvikt. Likhet med SSc: Kan gi hudfortykkelse og indre organfibrose som ved SSc.
- Toxic oil syndrome (inntak av rapsolje kontaminert av fenylamino propanediol). Epidemi i Spania i 1981. Ingen Raynauds, men ellers lik SSc. Systemisk sykdom utløst av forurenset rapsolje. Likhet med SSc: Kan gi hudfortykkelse og indre organaffeksjon som ved SSc, men uten Raynauds fenomen.
-
- Lichen sclerosus et atrophicus kan affisere alle deler av kroppen, men oftest genitalier (vulva, penis). Hvite hyperkeratotiske flekker som kan klø, blø og medføre smerter. Kan gi hudforandringer, men vanligvis ikke systemiske symptomer.
- Lipodermatosklerose: Pannikulitt subkutant i begge legger. Harde legger proksimalt for ankler. Eldre personer. Ukjent årsak.
- Lokalisert sklerodermi (Morfea: ulike typer): Begrenset hudfortykkelse uten systemisk affeksjon. Hudforandringene kan ligne på SSc, men uten Raynauds fenomen eller indre organaffeksjon.
- Nefrogen systemisk fibrose (NSF). Systemisk fibrose utløst av gadoliniumholdig kontrastvæske hos pasienter med nyresvikt. Kan gi hudfortykkelse og indre organfibrose som ved SSc.
- Mediastinal fibrose / fibroserende mediastinitt: Fibrose i mediastinum, kan gi kompresjon av organer i brysthulen. Lungefibrose kan forekomme ved SSc.
- Melorheostosis. Begynner i barnealder. Fortykket, lokalisert benstruktur. Kan medføre smerte, fysisk deformitet, hud og sirkulasjons-problemer, kontrakturer og redusert fysisk funksjon. Kan gi hudforandringer og kontrakturer, men skyldes en annen patofysiologi.
- Morfea (lokalisert skleroderma)
- Lineær sklerodermi (“coup de sabre”).
- Keloid morfea (irregulære smertefulle noduli).
- Generalisert morfea
- Andre typer
- Nodulær sklerodermi. En meget sjelden tilstand som gir seg til kjenne ved multiple keloid-liknende lesjoner. Pasientene har ofte artralgier, sklerodaktyli, Raynauds fenomen, digital pitting, kalsinose og lungesykdom. Mer sjelden er pulmonal arteriell hypertensjon, nyresykdom. SR ofte normal. Kan ha mange likhetstrekk med SSc, men er en distinkt entitet.
- Peyronies sykdom (fibromatose i penis): Fibrose i penis som kan gi krumning og erektil dysfunksjon. Kan ligne på fibrose i hud og indre organer ved SSc.
- POEMS syndrom (polynevropati, organmegali, endokrinopati, monoklonal gammopati, hyperpigmentering og hudfortykkelse): Multisystem sykdom med nevropati, organforstørrelse, endokrine forstyrrelser og hudforandringer. Kan gi hudfortykkelse som ved SSc.
- Poikilodermi (inflammatorisk eksem fra barnealder, non-cyklisk neutropeni, luftveissymptomer, negledystrofi, hyperkeratose, kalsinose, kortveksthet). Sjelden hudsykdom med pigmentforandringer, atrofi og telangiektasier. Kan gi hudforandringer som ved SSc (Wang L, 2017).
- Porfyri (curana tarda). Arr-forandringer etter multiple hudskader på lys/sol-eksponerte områder. Metabolsk sykdom som gir økt lysfølsomhet og hudskader. Kan gi hudforandringer, men skyldes en annen patofysiologi.
- Progeria (Hutchinson-Gilford syndrom, Werners syndrom) begynner i to års alder. Sjelden genetisk sykdom med prematur aldring. Fugle-ansikt, tynne ben. Kan gi hudforandringer, men skyldes en annen patofysiologi.
- “Puffy hands” av andre årsaker: Psoriasisartritt, MCTD, amyloidose
- Retroperitoneal fibrose og multifokal idiopatisk fibrosklerose (IgG4 relatert sykdom). Fibrose i retroperitoneum eller andre organer. Kan ligne på fibrose i indre organer ved SSc.
- Raynauds fenomen av andre årsaker: Andre systemiske bindevevssykdommer. Primær Raynauds
- Skleromyksødem (papulær mucinose): Hudsykdom med papler som inneholder mucin. 2-4mm store papler, til dels med flat overflate. Inneholder mucin, ikke puss. Grupper og lineær utbredelse over dorsalside av hender, ansikt, albuer og ekstensor-sider er typisk. Utbredelse over større deler av kroppen kan gi et systemisk sklerose/sklerodermi-lignende bilde med reduserte bevegelsesutslag (Hummers LK 2014).
- Sklerødem Buschke: Se Buschke ovenfor.
- “Stiff skin syndrom”: Sjelden tilstand med fortykket hud uten inflammasjon. Starter ofte i barne- og ungdomsårene. Ingen organaffeksjon. Histologi viser ingen inflammasjon (Guiducci S Rheumatology 2009). Kan ligne på hudfortykkelse ved SSc.
- Venøs insuffisiens, kronisk med sekundær dermato-sklerose. Hudfortykkelse i legger pga. venøs sirkulasjonssvikt. Kan ligne på hudfortykkelse i legger ved SSc.
Svangerskap ved SSc
Svangerskap kan ofte gjennomføres ves systemisk sklerose, men bør generelt frarådes ved alvorlig organmanifestasjon som alvorlige manifestasjoner i lunger, nyrer eller hjerte. Pasienter med aktiv progredierende diffus form har størst risiko for svangerskapsrelaterte komplikasjoner, til tross for tett, multidisiplinær oppfølging (Braun J, 2022).
Data er usikre fordi aktuelle studier er små med risiko for seleksjonsbias, men generelt vil sykdomsaktiviteten i løpet av svangerskapet forbli uendret hos omtrent 60 %. Omtrent 25 % vil oppleve bedring, 15 % forverring og 35 % forverring postpartum.
Det er økt risiko for preeklampsi, intrauterin veksthemming, prematuritet og spontane aborter. En av årsakene kan være vaskulopati i placenta (Ibba-Manneschi L, 2010).
Renal krise kan ses i ca. 2% av svangerskap ved systemisk sklerose. Det er essensielt å skille denne fra preeklampsi og eklampsi. Renal krise kan opptre når som helst, men særlig ved diffus form av systemisk sklerose og de første to årene fra diagnose. Behandling med ACE-hemmere kan gi fosterskader, oftest hvis de brukes i tredje trimester. På vital indikasjon kan ACE-hemmere likevel være nødvendig ved renal krise (Samaritano LR, 2020). Alternativer er andre antihypertensiva. Uansett bør fosteret kontrolleres for utvikling av oligohydramnion. Generelt om svangerskap ved revmatisk sykdom i eget kapittel. Vennligst se også info fra NKSR.
Sjekkliste når svangerskap ved systemisk sklerose blir planlagt:
- Forbudte medikamenter seponeres.
- Tegn til organskader må bli vurdert før graviditet.
- Pulmonal hypertensjon er en kontraindikasjon.
- Lungefunksjon (spirometri, CT).
- Hjertefunksjon (EKG), ekkokardiografi.
- Nyrefunksjon (blod og urinprøver).
- Sjekk vitamin D og jern-status (25-OH vit-D, transferrin-reseptor). Mulig redusert opptak fra tarmen ved systemisk sklerose kan føre til for lavt vitamin D i blodet.
- Antistoff mot ScL-70 og RNA-polymerase III øker komplikasjonsfaren ved graviditet.
- Antifosfolipid-antistoff bør sjekkes selv om økt forekomst ikke forventes ved systemisk sklerose.
- Gynekologisk vurdering overveies.
- Generell informasjon om sykdommen og om graviditet.
Sjekkliste under svangerskap ved systemisk sklerose:
- Følges opp som et «risikosvangerskap» i samarbeid med fødepoliklinikk (fosterets vekst og blodsirkulasjon, sjekker tegn til for tidlig fødsel).
- Medikamenter som tillates (om nødvendig): Protonpumpehemmere (mot magesyreoppstøt), kalsium-antagonister (Adalat) (mot høyt blodtrykk eller Raynauds fenomen), antihistaminer (mot allergi og sterk klør), lav dose acetylsalisylsyre (Albyl-E 75-160mg, fra svangerskapsuke 12) (Forebyggende mot preeklampsi). Prednisolon eller andre kortikosteroider unngås eller brukes i lavest mulig dose.
Sjekkliste ved fødsel og systemisk sklerose:
- Informer fødestuen dersom huden er preget av sykdommen; Kan gi problemer for anestesi og for å finne venøs tilgang.
- Regional anestesi (spinal/epidural) foretrekkes fremfor narkose (intubasjon).
- Etter fødsel: Følg blodtrykket.
- Episiotomi eller sår etter sectio gror vanligvis ukomplisert.
Behandling
Behandlingsstrategier ved systemisk sklerose (SSc):
SSc forløper svært forskjellig og krever individualisert behandling. Behandlingen må tilpasses sykdomsprogresjon, behandlingsintoleranse og komorbiditeter. Malnutrasjon og økt infeksjonsrisiko må en også ta hensyn til. Øsofagusdysmotilitet og depresjon kan påvirke compliance/etterlevelse (Thoms BD, 2007; Volkmann ER, 2023).
Hvis en vurderer å starte systemisk immunsuppressiv eller antifibrotisk behandling ved SSc, er det viktig å ta hensyn til at den forventede behandlingseffekten er begrenset og risikoen for bivirkninger er betydelig. I praksis er det bare en liten andel av pasientene som vil ha nytte av denne behandlingen. Spesielt er en tilbakeholden ved den begrensede formen/CREST og ved langsomt progredierende eller stabil diffus form. Samarbeid med spesialiserte sentre anbefales (Christopher P Denton, Dinesh Khanna, Lancet 2017).
Behandlingen består av:
- Generelle tiltak for å forebygge progresjon og komplikasjoner (artritt, myositt, fibrose).
- Behandling av organspesifikke komplikasjoner.
- Immunsuppressiv behandling.
Behandling av spesifikke komplikasjoner
Digitale sår/ulcera:
- Varmehjelpemidler.
- Kalsiumblokkere (nifedipin) ved truende sår.
- Fosfodiesterase-5-hemmere (PDE5 hemmer; sildenafil) ved utilstrekkelig effekt eller
- Intravenøs iloprost (Ilomedin) ved sår
- Endotelinreseptorantagonister (bosentan) for å redusere antall nye sår (Del Gado F, 2025).
- Topikal nitroglyserin og botulinumtoksininjeksjoner som tilleggsbehandling.
- Forebyggende tiltak: Infeksjons- og kuldeforebygging, bruk av termiske hansker.
- Fysioterapi, inkludert oral og manuell trening, samt aerob trening. Spesialisert henvisning anbefales (Liem SIE, 2022).
Gastrointestinale manifestasjoner:
- Refluksøsofagitt (SSc-GERD): Protonpumpehemmere (esomeprazol/Nexium 20-40 mg/d), pantoprazol/Somac), hevet hodeleie og kostholdsmodifikasjoner: unngå måltider sent på kvelden.
- Motilitetsforstyrrelser: Vurder indikasjon for prokinetiske legemidler (metoklopramid (Afiprn), domperidon (Motilium), erytromycin) som symptomatisk behandling.
- Strikturer: Kirurgisk konsultasjon.
- GAVE, bakteriell overvekst, anal inkontinens, malabsorpsjon og pseudoobstruksjon: Gastroenterologisk samarbeid.
- Bakteriell overvekst: Skiftende antibiotikabehandling (se tabellen nedenfor).
- Obstipasjon: Kostholdsmodifikasjoner, eventuelt prokinetika.
- Fekal inkontinens: Gastroenterologisk utredning og oppfølging.
| Skiftende medikamentell behandling av bakteriell overvekst (etter Quinlivan A, 2023) | ||
| Medikament | Dosering | Bivirkninger |
| Rifaximin | 1200-1600mg/d i 10-14 dager | |
| Neomycin | 500 mg to ganger daglig i 10 dager | Nefrotoksisitet, irreversibel hørselstap og vestibulære forstyrrelser |
| Ciprofloxacin | 500 mg to ganger daglig i 7-10 dager | Forlenget QT-tidsintervall (i EKG) |
| Metronidazol | 500 mg to-tre ganger daglig eller 250 mg tre ganger daglig i 7-10 dager | Forvirring, encefalopati |
| Amoxicillin/clavulansyre i kombinasjon eller amoxicillin | 875/125 mg to ganger daglig eller 500 mg tre ganger daglig i en uke | Clostidium difficile. Hypersensitivitetsreaksjon. Hepatotoksisitet |
- Kardiologisk samarbeid.
- Kardial svikt: Diuretika (bumetanid/Burinex).
- Pulmonal hypertensjon er omtalt i eget kapittel.
- Ved pulmonal arteriell hypertensjon (PAH) vurderes en kombinasjon av PDE5-hemmere og endotelinantagonister (ambrisentan, bosentan) som førstelinjebehandling.
- Antikoagulantia (warfarin/Marevan) anbefales generelt ikke i denne sammenhengen (Del Gado F, 2025).
Hudmanifestasjoner:
- Fuktighetskremer og fysioterapi/øvelser for å opprettholde elastisitet (fleksjon- og ekstensjon av fingre, smile- og grimase-øvelser for ansikt).
- Mykofenolatmofetil ved progressiv hudinvolvering og diffus form. Utprøvende kombinasjon med rituksimab kan vurderes i alvorlige tilfeller.
- Antihistaminer ved pruritus.
- Laserbehandling av teleangiektasier.
- Kirurgisk fjerning av kalsinose (hyppig residiv).
- Kosmetisk bruk av Restylane ved “carpfjes”.
- Hudfibrose:
- Metotrexat (MTX), mykofenolat (MMF), tocilizumab eller rituksimab bør vurderes i tidlig fase av diffus form, spesielt hvis prognostiske faktorer er ugunstige (Pope JE, 2023; Del Gado F, 2025).
Pulmonale manifestasjoner (interstitiell lungesykdom, SSc-ILD):
- DMARDs: Mykofenolatmofetil (MMF), cyklofosfamid eller rituksimab (biologisk) kan vurderes.
- Antifibrotika: Nintedanib (Ofev) alene eller kombinert med MMF kan være aktuelt (Del Gado F, 2025)
- Tocilizumab i refraktære tilfeller (Mankikian J, 2023; Raghu G, 2024)
- Høydose kjemoterapi med autolog stamcellestøtte (HMAS) ved raskt progredierende lungesykdom hos utvalgte pasienter med dårlig prognose og fravær av kardiologiske- og andre kontraindikasjoner (Hoffmann-Vold A, 2022).
- Oksygenbehandling (f. eks ved fysisk aktivitet og under flyreise) vurderes via lungelege ved hypoksemi (SpO2 < 95%).
- Pulmonal rehabilitering (Castro AAM, 2013).
- Lungetransplantasjon i utvalgte tilfeller med avansert sykdom.
- Glukokortikoider brukes sjelden ved SSc-ILD fordi de vanligvis ikke er effektive og øker risikoen for infeksjoner, osteoporose og diabetes mellitus. De øker også risikoen for renal krise, spesielt hos anti-RNAPIII-positive pasienter med tidlig aktiv diffus kutan systemisk sklerose (dcSSc).
Tabell. Behandlingsforslag ved ILD ved systemisk sklerose (Pope JE, 2023)
| Behandlingstype | Medikament og dose |
| Immunsuppresjon | Oral MMF (2–3 g per dag) eller azatioprin (150 mg per dag) |
| Intravenøs cyklofosfamid (600 mg/m²) eller oral cyklofosfamid 100–150 mg per dag | |
| Rituksimab to intravenøse infusjoner med 2 ukers mellomrom, deretter én infusjon hver 6. måned | |
| Tocilizumab 162 mg subkutant én gang per uke eller 4–8 mg/kg intravenøst månedlig | |
| Andre immunsuppressiva kan forbedre lungefunksjonen eller redusere debut av ILD (f eks metotreksat), men det foreligger færre data enn for MMF | |
| Vurder egnethet for kliniske studieprotokoller | |
| Anti-fibrotisk terapi | Nintedanib 150 mg to ganger daglig; reduser til 100 mg to ganger daglig hvis tolereranseproblemer |
| Man kan vurdere pirfenidon (færre data og ikke over alt godkjent for denne indikasjonen); øk til 801 mg tre ganger per dag etter toleranse; hvis tolereranseprobelmer, reduseres dosen | |
| Vurder egnethet for kliniske studieprotokoller | |
| Anti-refluks behandling og behandling av dysfagi | Protonpumpehemmer som førstelinjebehandling, ofte over maksimal godkjent dose |
| H2-antagonist, prokinetiske legemidler, sukralfat, antacida | |
| Livsstilsendringer: hev hodeenden av sengen, ingen mat etter kveldsmat, tygg maten godt, spis sakte, drikk vann under måltider, unngå matvarer som utløser refluks eller forverrer dysfagi | |
| Øsofagusdilatasjon ved behov | |
| Fundoplikasjon-kirurgi ved alvorlig refluks med aspirasjon | |
| Andre intervensjoner | Røykeslutt |
| Vaksinasjoner (influensa, COVID-19, pneumokokk) | |
| Oksygen ved hypoksi eller desaturasjon ved anstrengelse eller liggende | |
| Treningsprogram, lungerehabilitering | |
| Tidlig intervensjon ved infeksjon | |
| Antibiotikaprofylakse; f eks. azitromycin 250 mg tre ganger per uke ved residiverende lungeinfeksjoner eller alvorlig bronkiektasi | |
| Pneumocystis jirovecii pneumoni-profylakse ved betydelig immunsuppresjon; trimetoprim pluss sulfametoksazol dobbelt styrke tre ganger per uke. | |
| Identifisering og behandling av samtidig pulmonal hypertensjon | |
| Vurder henvisning for lungetransplantasjon |
- Skleromyositt (med muskelaffeksjon) kan behandles med lavdose glukokortikoider (prednisolon) og metotreksat. En case-report indikerer effekt av mykofenolat og rituksimab (Amaranta I, 2025).
Renalkrise (SRC)
- ACE-hemmere (ramipril, captopril) bør brukes umiddelbart, også til pasienter i dialyse.
- Sirkulatorisk stabile pasienter kan bruke f. eks. ramipril initialt 5 mg, med økende dose til 10 mg/d. Et alternativ er captopril, initialt 6,25 mg – 12,5 mg
- Mål: Blodtrykk 120/70-80 mmHg.
- Regelmessig blodtrykkskontroller er spesielt vikt hos Ssc-pasienter som bruker glukokortikosteroider.
- Nyretransplantasjon vurderes etter 18 måneder.
- Kalsiumblokker (nifedipin -Adalat® Oros, amlodipin -Norvasc® ) er førstelinjebehandling (OBS! hypotoni).
- PDE5-hemmere (sildenafil) er et alternativ.
- Ved alvorlig Raynauds fenomen med truende gangren eller behandlingssvikt er ilioprost (Ilomedin) iv. et aktuelt alternativ (Del Gado F, 2025).
- Kirurgisk fjerning ved smerter eller funksjonsnedsettelse.
- Natriumtiosulfat-injeksjoner eller krem (Gauffenic A, 2023).
- Vasoaktive medikamenter (nifedipin, sildenafil).
Medikamenter
- NSAIDs: Forsiktighet med bruk av NSAIDs er nødvendig på grunn av bivirkningsrisikoen hos pasienter med svelgevansker, og det gjelder mange med SSc. Tablettene kan da feste seg til øsofagusveggen og lage sår. Gastrointestinale vaskulære ektasier (GAVE) og mageblødning som komplikasjon kan forverres ytterligere med NSAIDs.
- Glukokortikoider: Høye doser øker risikoen for renal krise, spesielt ved diffus systemisk sklerose. Doser over 15 mg/dag er assosiert med en signifikant økning i denne risikoen, og nøye monitorering av nyrefunksjonen er avgjørende.
- Immunsuppressiva:
- -csDMARDs: Mykofenolat anvendes i utvalgte tilfeller for å bremse progresjon av hudfibrose og interstitiell lungesykdom. Metotreksat er et alternativ ved prominent artritt, hvor det kan bidra til å redusere leddinflammasjon og hevelse (Pope JE, 2023).
- -bDMARDs (rituksimab, tocilizumab). Disse biologiske medikamentene er utprøvende behandling for kutane og pulmonale manifestasjoner av systemisk sklerose. Forskning pågår for å avklare deres effekt og sikkerhetsprofil i denne pasientgruppen (Pope JE, 2023).
- JAK-hemmer og TGF-β hemming. Begge disse medikamentklassene representerer eksperimentell behandling for systemisk sklerose. De retter seg mot spesifikke signalveier involvert i patogenesen av sykdommen, og kliniske studier utføres for å evaluere deres terapeutiske potensial (Sener S, 2025).
- -HMAS (Høydose kjemoterapi med autolog stamcellestøtte). For detaljert informasjon om denne behandlingsmetoden, vennligst referer til eget kapittel om HMAS. Denne intense behandlingen er reservert for selekterte pasienter med alvorlig og progredierende systemisk sklerose.
- –CAR T-cellebehandling. Dette er en eksperimentell behandlingsform som er under utforskning for systemisk sklerose (Bergmann C, 2023). Den involverer genmodifisering av pasientens egne T-celler for å påvirke spesifikke cellepopulasjoner som bidrar til sykdommen.
- Per juni 2025 er det rapportert 22 behandlede pasienter. Effekten har vært god etter en observasjonstid på 1-13 måneder. En observerte stabilisering eller bedring i lungefunksjon og bedring i Rodnan skin Score (mRSS). Rapporterte bivirkninger var to tilfeller av autoimmun nevrotoksisitet (ICANS), samt noen infeksjoner. Bivirkningene lot seg behandle og det er ikke rapportert behandlingsrelatert mortalitet (Khanna D, EULAR 2025).
Anbefaling: Norsk Revmatologisk forening / legeforeningen har utarbeidet en detaljert veileder for behandling ved systemisk sklerose.
Kontroll og oppfølging av SSc
| Et forenklet kontroll-opplegg (minimum) er foreslått for pasienter med tidlig sykdomsform (se ovenfor). Ved patologiske organ-funn ved diagnose skal disse følges opp i tillegg (Gonzalez-Garcia A, 2022). |
|
| Ved diagnose | Årlig kontroll |
| Røntgen øsofagus eller manometri | |
| Lungefunksjonstester inklusiv DLCO
HRCT NT-ProBNP Doppler sonografi/ekko cor |
Lungefunksjonstester inklusiv DLCO |
| EKG | Doppler sonografi/ekko cor |
Regelmessig kontroll, for eksempel årlig, bør gjøres av følgende:
Hud. Forløpet kan følges med Rodnan hudscore (mRSS).
Nyrer. Nyrefunksjonen måles ved kreatinin eller GFR. Blodtrykk.
Hjertet. Ekkokardiografi for å utelukke pulmonal arteriell hypertensjon gjøres ofte årlig de første årene fra sykdomsdebut. PRO-BNP i blodet er også en nyttig parameter (øker ved pulmonal hypertensjon).
Lunger: Ikke stol på pasientens angivelse av manglende funksjons-dyspné. Mange av disse pasientene er såpass funksjonshemmet at de ikke belaster seg tilstrekkelig.
- HRCT av lunger regelmessig i en begrenset periode for a avdekke ILD og lungecancer kan være aktuelt (Distler O, 2020). Det er imidlertid holdepunkter for at pasienter med normal HRCT og normale lungefunksjonstester de første sykdomsårene har liten risiko for å utvikle ILD senere.
- Lungefunksjonstester kan delvis erstatte HRCT i forløpet (Gouellec N, 2017).
- 6-minutter gangtest viser om den fysiske kapasiteten holder seg (Rizzi M, 2018).
Malignitet-screeninger ikke rutine ut over det som anbefales befolkningen generelt. Generelt disponerer heller ikke systemisk sklerose for kreft. Et unntak kan gjelde pasienter som nylig er diagnostisert og har anti-RNA polymerase 3 antistoffet (Lazzaroni M-G, 2017).
Prognose
Individuelle forskjeller i sykdomsforløp og prognose er betydelige ved SSc. En grundig klinisk vurdering og biomarkører er viktige for å vurdere den individuelle prognosen. .
Den diffuse kutane formen (dcSSc) har generelt økt mortalitet sammenlignet med andre systemiske bindevevssykdommer. En tidlig diagnose og forbedret oppfølging forventes imidlertid å gi en bedre langtidsprognose.
Faktorer som påvirker prognosen:
- dcSSc er generelt assosiert med dårligere utfall og høyere risiko for alvorlig organinvolvering.
- Graden av proksimal hudaffeksjon korrelerer med dårligere prognose. Ti-års overlevelse synker fra 71% ved isolert sklerodaktyli til 58% ved hudinvolvering proksimalt for MCP-leddene og 21% ved truncus-involvering.
- Sekvens av symptomer: Utvikling av hudfortykkelse før Raynauds fenomen er uvanlig, men indikerer et alvorlig forløp. Langvarig Raynauds fenomen før kutane manifestasjoner kan derimot tyde på et mer benignt forløp.
- Dødsårsaker: Historiske data viser at den underliggende sykdommen bidrar til over 50% av dødsfallene ved diffus SSc og 35% ved begrenset SSc (Korelainen S, 2024). Av disse skyldes omtrent 35% interstitiell lungesykdom (ILD), 26% pulmonal arteriell hypertensjon (PAH) og 26% annen kardial involvering.
- Ved PAH med 6-minutters gangtest under 330 meter er prognosen dårlig. Stigende Pro-BNP er assosiert med høy mortalitet. Overlevelsesrater etter PAH-diagnose er henholdsvis 86% (1 år), 59% (2 år), 39% (3 år) og 22% (4 år).
- Interstitiell lungesykdom (ILD): 1-, 3- og 5-års overlevelse ved SSc-ILD er henholdsvis 100%, 90% og 77% (Tyndall AJ, 2009).
- Kardiale og renale manifestasjoner: Bidrar også vesentlig til økt morbiditet og mortalitet.
- Biomarkører: CRP og IL-6: Vedvarende forhøyet C-reaktivt protein (CRP) korrelerer med interleukin-6 (IL-6), og begge er ugunstige prognostiske markører for lungefibrose, PAH og mortalitet (Mitev A, 2019).
- Malignitet: Tidligere studier har rapportert økt insidens av lunge-, bryst-, tunge- og hematologisk malignitet (Szekanecz E, 2012). Det er imidlertid usikkert om dette skyldes miljøfaktorer, tidligere cyklofosfamidbehandling eller en predisposisjon fra grunnsykdommen (Sargin G, 2018).
Retningslinjer, anbefalinger og prosedyrer
EULAR 2023: Del Galdo F, 2024 (Behandling)
EULAR: Parodis I, 2023 (non-farmakologisk behandling)
2013 ACR/EULAR klassifikasjonskriterier for systemisk sklerose (van den Hoogen, I, 2013
Kanada: Pope J, 2012 (Management)
Norsk Revmatologisk forening / legeforeningen
Litteratur
Teksten er basert på aktuell faglitteratur. Den er skrevet og gjennomgått av forfatterne. I bearbeidelsen har vi brukt kunstig intelligens i noen avsnitt.
