VASKULITT (REV 034-052)
105 Takayasus Arteritt (TAK) (REV 034)
Takayasus arteritt
Jan Tore Gran; Birgir Mar Gudbrandsson; and Øyvind Palm
Kjennetegn på Takayasus arteritt
Angriper oftest unge kvinner.
Systemisk inflammasjon med høy senkningsreaksjon (SR) og CRP.
Karotidyni (smerter over a. carotis).
Sykdommen fører til arterielle stenoser og okklusjoner, sjeldnere aneurismer i store arterier, oftest i aorta og dens avgangsgrener.
Prosedyrekoder: EKG: FPFE15
ATC koder (for legemiddelstatistikk): Prednisolon: H02A B06 Immunsuppressive legemidler: L04A A.
Nøkkelord for journalskriving
Diagnosen baseres på:
- Debutalder <40 år, oftest kvinner, afrikansk eller asiatisk opprinnelse disponerer.
- Karotidyni (iskemisk smerte over carotider på halsen).
- CRP og SR forhøyet (noter maksimale og aktuelle verdier).
- Symptomer på iskemi (klaudikasjon, særlig i armer), svimmelhet, TIA, slag, myokardinfarkt.
- Redusert puls i en eller begge armer (a. radialis bilateralt, fotpulser bilateralt).
- Blodtrykksforskjell >10mmHg (systolisk) mellom armene.
- Stenoselyd over aorta (hovedpulsåren), hals-arterier, a. pulmonalis eller abdominale kar.
- MR- eller CT angiografi: Avsmalning av aorta, dens primære grener eller proksimale arterier i over- eller under-ekstremiteter.
- PET/CT med typisk opptak av 18FDG glukose i store kar.
Gjennomgått immunmodulerende behandling og kortikosteroider.
Årsak til konsultasjonen.
Definisjon
Takayasus artritt (TAK) er en vaskulitt-sykdom som angriper store og mellomstore kar. Den rammer oftest unge kvinner. Sykdommen medfører stenoser og okklusjoner i store arterier som aorta og de nærmeste arteriegrenene Sykdommen kalles også “pulseless disease” fordi pulsen i armene kan være svak eller ikke målbar (Esatoglu SN, 2022).
Historie
Mikito Takayasu (1860-1938) som var professor i oftalmologi ved universitetet i Kanazawa i Japan presenterte et sykdomstilfelle i 1908. Pasienten var en 22 år gammel kvinne med symptomer fra øyne, men også store kar, forenelig med Takayasus arteritt som sykdommen senere er kalt.
Etter Takayasus presentasjon rapporterte to av hans kolleger, Dr. Onishi og Dr. Kagoshima, om lignende tilfeller. De hadde også observert unge kvinner med de samme øyeforandringene, men la i tillegg merke til at disse pasientene hadde en påfallende svak eller helt fraværende puls i håndleddene.
Imidlertid foreligger tidligere rapporter som indikerer samme sykdom. Giovanni Battista Morgagni, en Italiensk anatom, beskrev en 40-år gammel kvinne med “pulseless disease” allerede i 1761 (Terao C, 2015).
I Norge beskrev Rødevand i 2001 seks tilfeller fra St Olavs Hospital (Rødevand E, 2001). I en epidemiologisk studie fra Rikshospitalet ble sykdommen nærmere beskrevet av Gudbrandsson i 2017 (Gudbrandsson B, 2017).
Epidemiologi
TAK defineres som en sjelden sykdom, selv om bedre undersøkelsesteknikker avdekker sykdommen oftere nå enn tidligere. Yngre kvinner affiseres hyppigst (2-3. dekade). Debutalderen er noe høyere hos kaukasiere i forhold til sorte og asiater.
Selv om sykdommen har en verdensomspennende utbredelse, antas den generelt å være mye vanligere blant asiatiske befolkninger. Insidensen av TAK er anslått til 1-2 per million i Japan og 2,2 per million i Kuwait.
En høy prevalensen av TAK er anslått med 40 per million i Japan og en lav på 0,9 per million i USA. Den rapporterte prevalensen i europeiske befolkninger varierer mellom 4,7 og 33 per million (Onen F, 2017).
I Norge er prevalensen av TAK blant nordeuropeere funnet å være 22.0 per million, blant kaukasiske asiater 78.1 per mill. og hele 108.3 per mill. blant afrikanere (Gudbrandsson B, 2017).
Genetikk
Den mest kjente arvelige disposisjonen er HLA-B52 (Renauer P, 2017) som også disponerer for ulcerøs kolitt. Også en helgenomstudie (GWAS) har vist et genetisk slektskap med inflammatorisk tarmsykdom (Ortiz-Fernandez L, 2020).
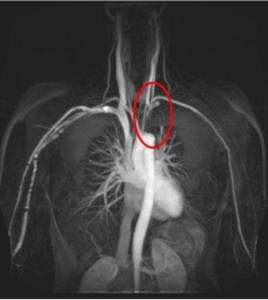
Patogenese
Inflammasjonen i arterier resulterer i veggfortykkelse, fibrose, stenose, okklusjoner og trombedannelse og evt. dannelse av aneurismer. Den vaskulære fibroseutviklingen er mye mer utpreget enn ved arteritis temporalis (Misra DP, 2023).
Årsaken til at aortaroten og dens avgangsgrener så ofte affiseres er ukjent. Man vet imidlertid at embryologisk stammer disse karene og pulmonale kar fra ektodermen. Alle andre kar er endodermale. De embryologisk ulike karene har forskjellige responser på immunologiske stimuli, ulik besetning av adhesjonsmolekyler og aldersforandringer utvikles forskjellig.
Strukturelt finnes det også forskjeller. Aorta thoracalis kjennetegnes ved velutviklet vasa vasorum og høyt antall elastiske fibre, mens mengden kollagene fibre er redusert i forhold til mange andre kar. Dette kan kanskje forklare noen av de ulike sykdommenes preferanser for visse organavsnitt.
Sammenlignet med arteritis temporalis er det forskjeller i sammensetningen av immuncellene som infiltrerer karveggene. I Takayasus arteritt omfatter disse en betydelig mengde CD8+ T-celler, samt naturlige “killer cells”. Dette indikerer forskjellige mekanismer for vevsskade og remodullering av karveggene (Watanabe R, 2020).
Symptomer
Sjeldenhet og mangel på spesifikke tester bidrar til at symptomene på Takayasus arteritt ofte blir gjenkjent sent i sykdomsforløpet, noe som er uheldig, fordi tidlig behandling kan hindre at varige skader oppstår (Kim ESH, 2018).
Tidlige symptomer omfatter:
- Utmattelse
- Nattesvette
- Feber-tendens
- Artralgi og myalgi.
- Carotidyni. Noen merker også smerter over angrepne pulsårer på halsen (carotidyni), i brystet eller abdominalt (Maita H, 2023).
- Hudforandringer i form av erythema nodosum er relativt sjelden (Gupta M, 2013).
Senere i forløpet tilkommer klaudikasjon i form av smerter i en (oftest venstre-) eller begge armer, særlig ved arbeid med armene hevet. Smerten gir seg raskt når armene tas ned og i hvile. Klaudikasjon skyldes iskemi til muskler. Dette oppstår ved arterielle stenoser og okklusjoner til armene (Ceasar-Peterson S, 2023). Utviklingen skjer imidlertid såpass langsomt at kollateralformasjon oftest hindrer nekroser.
Smerter i brystet kan skyldes betente arterier, men også angina pectoris dersom hjertets koronarårer er angrepet og stenotiske, selv blant hos unge mennesker (Dzhus M, 2023). Myokardinfarkt forekommer sjelden, men er observert (Wang Y, 2020), tilsvarende for thorakale aneurismer (Jena A, 2024).
Hjerneslag. Redusert sirkulasjon i halsarterier, oftest karotidene, kan medføre vertigo og flimring for øynene under fysisk aktivitet. Bevissthets-tap eller hjerneslag er sjelden. Størst risiko foreligger hvis blodårer på halsen er angrepet over tid og før sykdomsbehandlingen har begynt (Roy AT, 2022).
Synsforstyrrelser kan omfatte plutselig synstap og blindhet ved redusert blodtilførsel til netthinnen eller synsnerven. Gradvis redusert syn kan oppstå som følge av uskarp linse/grå stær (katarakt), særlig etter mye kortison/prednisolon i behandlingen (Szydełko-Paśko A, 2023).
Undersøkelser
Anamnesen. En grundig sykehistorie og klinisk undersøkelse er avgjørende for å vurdere om pasienten har symptomer som er typiske for Takayasus arteritt, spesielt hos unge kvinner.
Klinisk undersøkelse.
- Perifer arteriell sirkulasjon kan kartlegges ved å palpere puls distalt i ekstremitetene og på halsen. Svake eller fraværende pulser, spesielt i armene, sees hos 90 % i sykdomsforløpet.
- Blodtrykk måles bilateralt. Nedsatt eller ikke målbart i blodtrykk i armene er ikke uvanlig i senere stadier. Hypertensjon, ofte forårsaket av nyrearteriestenose, forekommer hos 30-80 % av pasientene. OBS! Blodtrykksmåling på underekstremiteter er nødvendig dersom det er affeksjon av arterier til begge armer.
- Ved auskultasjon kan stenoselyder etter hvert påvises hos 85 % og høres best over karotidene, subcalvia og abdominale kar. Aortainsuffisiens forekommer hos 22 %, og i noen tilfeller kan hjertesvikt og kardiomyopati oppstå.
- Pulmonal arteriell hypertensjon med ukarakteristiske symptomer og funn er uvanlig, men forekomsten er ikke godt kartlagt.
- Sentralnervøs (CNS) affeksjon med nevrologiske utfall er sjelden, men kan skyldes iskemisk hjerneslag (Zhou J, 2021).
- Øyelege-vurdering ved synsforstyrrelser kan være aktuelt (Szydełko-Paśko A, 2023).
Laboratorieprøver. Rutineprøver kan omfatte CRP, SR, Hb, leukocytter med differensialtellinger, trombocytter, lever-, nyre- og thyreoidea-funksjonsprøver, glukose, totalkolesterol, LDL- og HDL-kolesterol, ANA, ANCA og antifosfolipid antistoff (lupus antikoagulant, kardiolipin- og beta-2-glykoprotein antistoff) og urin stiks.
-Omtrent 80-93 % har forhøyet CRP og SR ved diagnose, men de korrelerer ikke alltid med sykdomsaktiviteten eller progredierende fibrotiske karstenoser. Under eventuell utprøvende behandling med tocilizumab (RoActemra) er CRP og SR imidlertid mindre nyttige. -Immunologiske prøver: Det forventes ingen utslag i immunologiske tester/antistoff (Tombetti E, 2019).
Bildediagnostikk
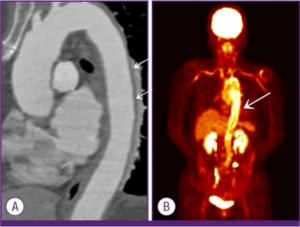
-Konvensjonell CT kan vise tegn til fortykket karvegg i de store arteriene, oftest a. subclavia, a. carotis, a. brachiocephalicus og aorta. Typisk er det fravær av arteriell kalsinose (som ses ved aterosklerose).
-CT-angiografi påviser stenoser, okklusjoner og sjeldnere aneurismer. Stenosene er vanligvis relativt langstrakte. CT-undersøkelser medfører imidlertid strålebelastning. Hos unge pasienter med antatt behov for gjentatte kontroller foretrekkes derfor andre undersøkelser over tid. Sensitivitet og spesifisitet på hhv 95% og 100% er utmerket (Yamada I, 1998).
-MR-angiografi fremstiller store arterier med stenoser og okklusjoner. Ødem i karvegg kan også visualiseres. EULAR anbefaler MR (eventuelt PET/CT) som initial undersøkelse ved mistanke om TAK for begrense røntgenstråler (Dejaco C, 2023).
-Ultralyd Doppler av halskar har høy oppløsning og god spesifisitet for påvisning av inflammasjon. Metoden kan vise veggfortykkelse som omgir karotidene (halo-Iignende”) og med langstrakte stenoser (“makaroni-tegn”). Vertebralisarterier med eventuell retrograd blodstrøm (ved subclavian steal-fenomen) kan også fremstilles.
18FDG PET/CT kan kartlegge utbredelse av vaskulitten og gi informasjon om inflammatorisk aktivitet. Imidlertid ved reparasjonsprosesser også medføre FDG-opptak i PET/CT, noe gjør metoden mindre egnet til å vurdere effekt av behandling og progresjon. PET/CT er best på blodkar med diameter over 4 mm.
-EULAR anbefaler PET/CT som alternativ til MR-angiografi som initial undersøkelse ved mistanke om Takayasus arteritt (Dejaco C, 2023). Imidlertid vil prednisolon redusere mulighetene for å påvise inflammatoriske forandringer. Prednisolon dosen må ved undersøkelsen være lavest mulig, helst lavere enn 15 mg/døgn. Dårlig kontrollert diabetes mellitus kan også vanskeliggjøre tolkningen av resultatene. Funnene ved PET skanning må derfor tolkes med forsiktighet.
Ved hjelp av PET Vascular Activity Score (PETVAS) kan man estimere sykdomsaktivitet (Grayson PC, 2017). Utviklingen innen PET/CT går raskt. Bedre oppløsing og nye tracere vil sannsynligvis gi enda bedre anvendelse inne får år (Peverelli M, 2025).
Bildediagnostikk ved vaskulitt er også omtalt i et eget kapittel
Biopsi
Biopsi er sjelden aktuelt ved Takayasus arteritt. De histologiske forandringene fra store kar kan kan omfatte kjempeceller som ved temporalis arteritt, men nærmere immunologiske undersøkelser viser forskjeller mellom disse sykdommene. Vaskulær fibrose er mer fremtredende ved TAK (Misra DP, 2023). (vennligst se også avsnittet om “patogenese” ovenfor).
Diagnosen
Mistanke om Takayasus arteritt oppstår vanligvis hos unge kvinner med tegn på systemisk inflammasjon (forhøyet CRP og SR) og kliniske symptomer på vaskulær iskemi, som karotidyni og brystsmerter. Relativt sene manifestasjoner i ekstremiteter, abdomen, sentralnervesystemet og/eller hjertet er heller ikke sjelden foranledning til diagnosen. Diagnosen bekreftes ved hjelp av bildediagnostikk som CT- eller MR-angiografi, PET/CT eller ultralyd av precerebrale kar. Det finnes ingen spesifikke biokjemiske markører/tester for sykdommen og biopsi er sjelden aktuelt.
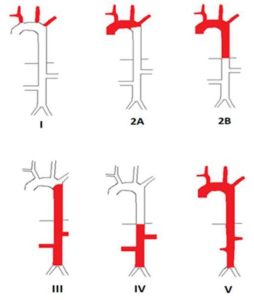
Sykdomsutbredelse (Hata A, 1996). (Se også illustrasjonen ovenfor).
Pre-stenotisk sykdom kan defineres ved påvist inflammasjon i arterieveggene ved PET/CT, uten at stenoser eller okklusjoner foreligger (Gudbranssson B, 2017).
Type I: Aortabuens grener
Type IIa: Aorta ascendens, aortabuen og aortagrenene)
Type IIb: Aorta ascendens, aortabuen og aortagrenene og thorakale aorta descendens
Type III: thorakale aorta descendens og abdominal aorta og/eller affeksjon av nyrearterier
Type IV: abdominal aorta og/eller affeksjon av nyrearterier
Type V: Kombinasjon av Type IIb og IV
Klassifikasjonskriterier (ACR 1990)
3 eller flere av disse 6 skal oppfylles:
- Debutalder <40 år
- Symptomer på redusert sirkulasjon (klaudikasjon)
- Redusert puls i en eller begge armer
- Blodtrykksforskjell >10mmHg (systolisk) mellom armene.
- Bilyd over aorta (hovedpulsåren) eller a. Pulmonalis (lungepulsåre)
- Angiografi: Avsmalning av aorta, dens primære grener eller proksimale arterier i over- eller under-ekstremiteter.
- Ikke andre årsaker (arteriosklerose, dysplasi)
- Sensitivitet 90.5%, spesifisitet 97.8
| ACR/EULAR klassifikasjonskriterier (2022) (Grayson PM, 2022)
Kriteriene baseres på vekting og av poeng-score og krever følgende:
|
|||
| Kliniske kriterier | pkt | Bildediagnostikk | pkt |
| Kvinnelig kjønn | +1 | Antall affiserte arterier (stenose, okklusjon, aneurisme) i områdene: thorakal aorta, abdominal aorta, mesenterica, ve. eller hø. carotider, ve. eller hø. subclavia, ve. eller hø. nyrearterier. VELG EN AV FØLGENDE TRE: | |
| Angina eller iskemisk cardial smerte | +2 | -Ett av arterie-områdene (se ovenfor) | +1 |
| Klaudikasjon i arm eller ben | +2 | -To av arterieområdene | +2 |
| Vaskulær stenoselyd ved auskultasjon av aorta, carotider, subclavia axillaris renalis eller iliofemoralis | +2 | -Tre av arterieområdene | +3 |
| Pulsreduksjon i arm i a. axillaris, brachialis eller radialis | +2 | Symmetrisk affeksjon av arterie-par (stenose, okklusjon eller aneurismer påvist ved angiografi eller ultralyd) | +1 |
| Carotis-ømhet eller redusert/fraværende puls | +2 | Abdominal affeksjon (stenose, okklusjon eller aneurisme påvist ved angiografi eller ultralyd av abdominal aorta , nyre eller mesenterial-arterier) | +3 |
| Systolisk blodtrykksforskjell ≥ 20 mmHg | +1 | ||
| For klassifikasjon av diagnosen Takayasus arteritt kreves ≥ 6 punkter. Sens. 93,8%, spes. 99,2% | |||
Skåring av sykdomsaktivitet (NIH-kriterier, Litteratur: Kerr GS, 1994)
Aktiv sykdom kan defineres som minst 2 av:
- Systemiske manifestasjoner (feber, artralgi, myalgi)
- Forhøyet SR
- Vaskulær iskemi eller inflammasjon (klaudikasjon, reduserte eller manglende pulser, stenoselyder, vaskulær smerte (karotidyni), asymmetrisk BT)
- Typiske angiografiske funn
Differensialdiagnoser
Tilstander som kan ligne på Takayasus arteritt inkluderer:
Arteritis temporalis: En annen storkarsvaskulitt som hovedsakelig rammer de kraniale arteriene, men kan også involvere aorta og gi symptomer som ligner på TAK. Utvikling av stenoser og okklusjoner er mindre uttalt, og pasientene er over 50 år gamle med median alder ca. 72 år.
Aterosklerose: Kjennetegnes av plakkdannelse i arteriene, noe som kan føre til redusert blodtilførsel og symptomer som ligner på Takayasus arteritt. Oftest rammes imidlertid eldre pasienter og aterosklerose har en annen fordeling av karforandringer. Risikofaktorer er alder, hyperkolesterolemi, diabetes og nikotin.
Carotidyni av annen årsak: Kan være en isolert tilstand, men da med et kortere sykdomsforløp på 2-4 uker. Slike smerter kan skyldes arteriedisseksjon, cervikal skivesykdom og halslidelser.
Fibromuskulær dysplasi: Rammer arterieveggen og kan føre til innsnevringer og utvidelser av arteriene, noe som kan gi symptomer som ligner på Takayasus arteritt, men som oftest rammer yngre kvinner og har en annen fordeling av karforandringer.
Koarktasjon av aorta: En medfødt hjertefeil som kjennetegnes av en innsnevring av aortabuen. Symptomer kan ligne på TAK, men sykdommen er uten systemisk inflammasjon og oppdages i barndommen eller tidlig voksen alder (Julien IEH, 2017).
Infeksjoner. Salmonella, tuberkulose og syfilis kan forårsake betennelse i aorta og gi symptomer som ligner på TAK, men som vanligvis har et mer akutt forløp og ledsages av andre tegn på infeksjon. Mykotiske aneurismer
Marfans syndrom og Ehlers-Danlos syndrom: Arvelige tilstander som kan medføre aneurismer, men som vanligvis ikke gir de langstrakte stenosene eller okklusjonene som er typiske for TAK. Fravær av systemisk inflammasjon.
Non-kranial storkarsvaskulitt (uspesifisert): En uspesifisert form for vaskulitt som kan ramme de store arteriene, inkludert aorta, og som kan gi symptomer som ligner på TAK, men som ikke involverer de kraniale arteriene. Oftest noe eldre pasienter.
Segmental arteriell mediolyse (SAM) er en ikke-inflammatorisk degenerasjon av muskulære arteriers media, evt. også nærliggende vener. Hyppigst affiseres en eller to viscerale arterier. MR-angiografi viser dilatasjon, aneurisme eller stenose. Stenosene er vanligvis kortere enn ved TAK.
Vennligst les mer om differensialdiagnoser til vaskulitt i store arterier i eget kapittel.
Svangerskap
Det er økt risiko for komplikasjoner i svangerskap ved TAK. Basert på 27 studier med totalt 825 svangerskap i en metaanalyse var forekomsten av spontanabort 16 %, hypertensjon 37 % og preeklampsi 14 %. Gravide kvinner med TAK bør derfor overvåkes nøye (Partalidou S, 2023). Fertiliteten er vanligvis ikke affisert hos kvinner med TAK (Gudbrandsson B, 2016).
Før konsepsjon bør omfanget av vaskulær involvering kartlegges grundig. Redusert arteriell perfusjon i det intraabdominale karnettet, inkludert nyrearteriene, samt eventuelle aneurismer kan være spesielle risikofaktorer for alvorlige svangerskapskomplikasjoner.
For ytterligere informasjon om svangerskap og Takayasus arteritt henvises til informasjon fra Norsk kompetansesenter for revmatologisk rehabilitering, NKSR.
Behandling
Behandlingsmålet ved Takayasus arteritt er å hindre progresjon av arterielle manifestasjoner. Selv om normalisering av inflammasjonsmarkører kan oppnås, kan angiografisk kontroll avdekke at sykdommen likevel utvikler seg hos noen pasienter.
Kortikosteroider, vanligvis som prednisolon i tablettform, er hjørnesteinen i behandlingen og gir respons hos over 50 %. Det er ikke belegg for at intravenøs glukokortikoidbehandling i puls-doser er mer effektivt enn høye doser med orale glukokortikoider. Puls med intravenøse glukokortikoider kan vurderes for pasienter med sykdom som er livstruende eller truer organer (Maz M, 2021).
Det er vist at glukokortikoider virker hemmende på proinflammatoriske interleukiner IL-6 og IL-17 som er sentrale mediatorer ved vaskulitt (Hill CL, 2017). Ulempen med kortikosteroider er risikoen for bivirkninger ved langvarig bruk, som infeksjoner, osteoporose, overvekt og diabetes (Buttgereit F, 2018). Initial prednisolondose varierer opptil 1 mg/kg/dag, avhengig av graden av inflammasjon og forventet toleranse. Optimal varighet av glukokortikoidbruk ved TAK er ukjent. Generelt bør sykdommen ha vært i remisjon i minst 6-12 måneder før seponeringsforsøk. Prednisolondosen skal da i forkant reduseres gradvis over tid, men det er vanlig med tilbakefall når dosen nærmer seg 5-10 mg/dag. Likevel bør målet være å redusere prednisolondosen til 5 mg/dag eller lavere (Shirai T, 2021). Ved aktiv TAK anbefales vi vanligvis å bruke et ikke-glukokortikoid immunsuppressivt middel i tillegg til glukokortikoider fremfor glukokortikoider alene (Maz M, 2021).
DMARDs (sykdomsmodifiserende antirevmatiske legemidler) Valget av DMARDs til pasienter med TAK er ofte empirisk, basert på observasjonsdata og klinisk erfaring. Metotreksat er vanligvis førstevalget, men TNF-α hemmer kan også vurderes. Azathioprin (Imurel) er alternativ til metotreksat ved intoleranse/kontraindikasjon.
-Metotreksat. Prednisolon kombineres vanligvis med metotreksat (10-25 mg én gang ukentlig sammen med 1 mg daglig folsyre) for å redusere behovet for kortikosteroider.
-Andre csDMARDS. Et alternativ til metotreksat er azathioprin hvis metotreksat ikke kan brukes (Hellmich B, 2019). Cyclofosfamid er sjeldent alternativ på grunn av potensielle bivirkninger, inkludert infertilitet og økt kreftrisiko.
Biologiske legemidler (bDMARDs). Ved utilstrekkelig effekt av kortikosteroider kan biologisk behandling med TNF-hemmere eller tocilizumab være aktuelt som tillegg. Selv om medikamentgruppene er nevnt i både EULAR- og ACR-behandlingsanbefalinger er behandlingen utenfor godkjent indikasjon og bør håndteres deretter (Gudbrandsson B, 2017; Hellmich B, 2019). Behandling med IL-6-hemmere (tocilizumab) har vist lovende resultater i flere kasusrapporter, men en placebokontrollert studie fra 2017 viste ikke at tilbakefall ble hindret, selv om tiden til tilbakefall var noe lengre i behandlingsgruppen sammenlignet med placebo (Nakaoka Y, 2017; Kaymakci MS, 2024). En metaanalyse som sammenlignet effekt av TNF-hemmere og tocilizumab ved TAK konkluderte med at effekten var lik (Mistr DP, 2023). I praksis foretrekkes likevel f eks. adalimumab fremfor tocilizumab (Maz M, 2021).
Janus Kinase Inhibitorer (JAK-hemmere) er utprøvende behandling som ser ut til å være lovende for de mest alvorlige tilfellene som ikke har respondert tilstrekkelig på prednisolon, metotreksat og TNF-hemmer (Li J, 2025; Esatoglu SN, 2022).
Kirurgisk intervensjon er sjelden nødvendig, men kan være aktuelt ved alvorlige komplikasjoner eller manglende effekt av medikamentell behandling. Aorta ascendens, aortaklaff, carotis- og renalis-arterier opereres oftest. Inngrep foretrekkes i perioder med lav sykdomsaktivitet for å redusere risikoen for komplikasjoner som reststenose, anastomosesvikt, blødning, trombose og infeksjon. Operasjoner på store kar gir vanligvis best resultat (Ergi D, 2025). Pasienter bør være under steroidbehandling ved kirurgisk intervensjon. Omtrent en tredjedel av pasientene trenger reoperasjon (Soto ME, 2024).
Stentbehandling. Bruk av stenter (metallnett som utvider trange blodårer) gir ofte ikke tilfredsstillende resultater på grunn av hyppige restenoser, og mange foretrekker derfor konvensjonelle bypass-operasjoner (Zhang X, 2024).
Oppfølging
Klinisk oppfølging og CRP. I den innledende fasen anbefales tett klinisk oppfølging for å overvåke pasientens respons på behandlingen, utelukke bivirkninger og sikre at behandlingen har ønsket effekt. CRP er den mest nyttige laboratorieprøven, spesielt hos pasienter der CRP tidligere har vist seg å korrelere med sykdomsaktivitet.
Vurdering av sykdomsaktivitet/måleinstrumenter. Man kan definere klinisk stabil sykdom som:
- Fravær av nye symptomer og funn.
- Ingen akutt fase respons.
- Ingen klaudikasjon eller karotidyni.
Vurdering av sykdomsaktivitet ved Takayasus arteritt er utfordrende, da det mangler gode biomarkører utover akutt fase-reaktantene. Selv om SR og CRP vanligvis normaliseres raskt under induksjonsbehandling, kan lavgradig inflammasjon i arterieveggen fortsatt føre til sykdomsprogresjon (Kerr GS, 1994). Mål for sykdomsaktivitet f eks. Kerr/NHI-score er ikke særlig sensitive eller validerte på samme måte som BVAS-score ved ANCA-assosiert vaskulitt. Et nyere komposittskjema er Takayasu’s Arteritis Integrated Disease Activity Index (TAIDAI). Dette kan egne seg spesielt for forskning/studier, men ennå er erfaringene begrenset (Marvisi C, 2024).
Bildediagnostikk er derfor fortsatt spesielt viktig for å utelukke sykdomsprogresjon ved TAK. Imidlertid er PET/CT mindre nyttig i oppfølgingen enn ved diagnostisering. Bruk av Vascular Activity Score (PETVAS) kan likevel være supplerende, men bredere erfaring ved TAK utestår (Grayson PC, 2017).
MR-angiografi kontroller. Fibrotisk progresjon som forårsaker arterielle stenoser og okklusjoner kan utvikle seg uavhengig av systemisk inflammasjon (Misra DP, 2023). Bildediagnostikk (f eks. MR-angiografi) er derfor aktuelt også i oppfølgingen, selv om CRP er lav eller normal.
Det optimale intervallet mellom bildeundersøkelser er ikke godt etablert og varierer (f. eks. hver 3.–6. måned eller lenger). Et forslag er at MR-angiografi kan gjentas ved første 6-månederskontroll. Deretter kan årlige kontroller med bildediagnostikk være aktuelt. Ved høy, vedvarende sykdomsaktivitet, kan kortere intervaller være aktuelt.
For generell informasjon om oppfølging av revmatiske sykdommer, se eget kapittel.
Undersøkelser som ofte gjøres ved oppfølging av Takayasus arteritt
- Måling av BT i alle fire ekstremiteter. Puls også i halskar
- Auskultasjon av ev. stenoselyder over halskar, prekardialt/subclavia, abdomen og lysker
- Blodprøver CRP, ev også SR
- MR-angiografi av affiserte regioner
- UL-Doppler av halskar
- Ekkokardiografi
Prognose
Femårs overlevelse for pasienter med TAK er 80-90 %, og over 10 år er overlevelsen 60-87 %. Pasienter med type I sykdom (kun aortabuen affisert) har en femårs overlevelse på 100 %.
Imidlertid viser oppfølgingsstudier at varige karskader oppstår tidlig hos 80% av pasientene. Det rådes derfor til å være påpasselig med optimal immunsupprimerende behandling og monitoriering av sykdomsaktiviteten (Kermani TA, 2024). Alvorlig sykdom kjennetegnes ved retinopati, betydelig hypertensjon, uttalt aortainsuffisiens og aneurismedannelse. Det er også en økt risiko for å utvikle aterosklerose over tid.
Retningslinjer
EULAR 2023: Dejaco C, 2023 (bildediagnostikk)
ACR/EULAR klassifikasjonskriterier (Garyson PC, 2022)
EULAR 2018: Hellmich B, Ann Rheum Dis 2019
Litteratur
EULAR 2018: Hellmich B, Ann Rheum Dis 2019
Teksten er skrevet og gjennomgått av forfatterne. I bearbeidelsen har vi brukt kunstig intelligens i noen avsnitt.
